МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ УКРАИНЫ
ГОСУДАРСТВЕННОЕ ВЫСШЕЕ УЧЕБНОЕ ЗАВЕДЕНИЕ
„УКРАИНСКИЙ ГОСУДАРСТВЕННЫЙ ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ УНИВЕРСИТЕТ"
Кафедра ТОВФП
ИНДИВИДУАЛЬНОЕ ЗАДАНИЕ
ТРАВА ХВОЩА ПОЛЕВОГО
Выполнила
Студентка группы 4-Ф-75
Фоменок Т.Е.
Проверил
Поляков Е.В.
Днепропетровск 2009
ОПИСАНИЕ РАСТЕНИЯ
Хвощ полево́й, или Хвощ обыкнове́нный (лат. Equis é tum arv é nse )
Русские названия : хвощ полевой, сосонка, хвойка, елка, земляные орехи.
Белорусские : хвошч палявы, скрып, земляные apaxi, стукь
Украинские : хвощ польовий, сосонка польова, яличка.
Царство : Растения
Отдел : Хвощевидные
Класс: Хвощёвые
Порядок : Хвощёвые
Семейство : Хвощёвые
Род : Хвощ
Вид : Хвощ полевой
Хвощ полевой - многолетнее травянистое споровое растение семейства хвощевых (Equisetaceae), высотой до 60 см, с длинным (до 5-7 м) ползучим, буровато-черным корневищем, с черными шаровидными клубеньками. Основная масса корневищ расположена на глубине 60-100 см. Стебли двух видов: весенние - спороносные и летние - бесплодные. Спороносные стебли (высотой до 20 см) появляются ранней весной, простые, прямостоячие, лишенные зеленой окраски, буроватые, несущие на верхушке крупный колосок спорангий, густо покрытые зубчатыми влагалищами. После созревания спор эти стебли засыхают и отмирают, а из корневища вырастают летние зеленые стебли - членистые, большей частью 4-5-гранные, ветвистые. Ветви располагаются мутовками по 8-16 по всему стеблю. Стебли и ветви жесткие, шершавые на ощупь из-за образующихся в них кристаллов кремниевой кислоты. Листья недоразвитые, срастаются на стебле в цилиндрические трубчатые влагалища. Спороносит в апреле - мае. Споры шаровидные, зеленые. Размножается спорами и вегетативно - отрезками корневищ. Распространен почти на всей территории СНГ, за исключением Крайнего Севера и пустынь. Растет на рыхлых супесчаных и суглинистых свежих почвах на полях, в посевах, на железнодорожных насыпях, лесных полянах, на песчаных берегах рек, в песчаных и глинистых карьерах иногда образует чистые заросли. Является индикатором, указывающим на повышенную кислотность почв. Растение ядовито.
В качестве лекарственного растения хвощ полевой известен с давних пор. Авиценна использовал сок для лечения ран и язв, а настои на вине - для лечения опухолей печени и желудка, водянки и кишечных расстройств.
Сбор и сушка сырья. Заготавливают всю надземную часть (Herba Equiseti) летом, в юне - августе, срезая серпами, ножами или скашивая косами на высоте 5 см от поверхности почвы.
Сушат на чердаках, под навесами, раскладывая слоем толщиной 5-7 см, или в сушилках при температуре 40-50 °С. В сухую погоду сырье можно сушить в тени строений. Срок годности сырья 4 года. Цвет сырья серовато-зеленый. Запах слабый, своеобразный, вкус слегка кисловатый. Основные районы заготовок находятся в Беларуси, на Украине, в Ставропольском и Краснодарском краях, Пермской, Псковской, Липецкой, Воронежской областях России.
Кроме хвоща полевого, часто встречаются другие виды, не подлежащие заготовке, некоторые из них ядовиты. Хвощ лесной (Equisetum sylvaticum L.) имеет вторично ветвящиеся ветви, которые горизонтальны или загнуты вниз. Хвощ луговой (Equisetum pratense Ehrh.) имеет горизонтальные, неразветвленные, трехгранные ветви. Хвощ болотный (Equisetum palustre L.) имеет неразветвленные ветви большей частью пятигранные, неправильные, как и у хвоща полевого идущие косо вверх. Основание члеников ветвей черного цвета, зубчики ветвей с черно-бурой окраиной. Ядовит. Хвощ речной (топяной; Equisetum fluviatile) имеет стебель высотой до 1 м, толстый, с большой полостью внутри. Ветви простые или вообще отсутствуют.
Химический состав. Трава хвоща полевого содержит аскорбиновую кислоту (до 0,19 %), каротин, сапонин эквизетонин (около 5 %), флавоноиды (кверцетин, изокверцитин, кемпферол, лютеолин, эквизетрин), жиры, никотин, кремниевую (до 25 %), аконитовую, яблочную, щавелевую кислоты, жирное масло (до 3,5 %), горечи, дубильные и смолистые вещества, минеральные соли, фенолкарбоновые кислоты, ситостерол. В плодоносных побегах много сахара, в клубеньках - крахмала.
В надземной части содержатся: зола - 17,70 %; макроэлементы (мг/г): К - 33,50, Ca - 17,70, Mn - 2,70, Fe - 0,10; микроэлементы (КБН): Мg - 0,09, Cu - 0,15, Zn - 0,32, Mo -15,20, Cr - 0,02, Al - 0,04, Se - 30,00, Ni - 0,06, Sr - 0,35, Pb -0,003, I - 0,09. В - 2,00 мкг/г. Не обнаружены Со, Cd, V, Ba, Li, Ag, Au, Br. Концентрирует Mo, Se,
Фармакологические свойства. Галеновые препараты растения по диуретическому действию превосходят почечный чай. Кроме того, хвощ полевой обладает кровоостанавливающими и противовоспалительными свойствами. Выделенный из растения 5-глюкозидлютеолин проявляет антимикробные и противовоспалительные свойства. Экспериментами установлено, что хвощ полевой может оказывать дезинтоксикационное действие, в частности способствует выведению свинца из организма. Кремниевые соединения, содержащиеся в большом количестве в растении, играют важную роль в процессах метаболизма и функциональной деятельности соединительной ткани, слизистых оболочек, стенок кровеносных сосудов; особенно важны они для развития костной ткани.
Применение в медицине . Надземная часть. Жидкий экстракт, настой, отвар - как мочегонное, кровоостанавливающее и гипотензивное средство; при заболеваниях сердца и почек (особенно при отеках и других застойных явлениях на почве недостаточности кровообращения при плеврите, воспалительных процессах мочевого пузыря и мочевыводящих путей, при некоторых формах туберкулеза легких, связанных с нарушением силикатного обмена веществ; как кровоостанавливающее при геморрое, маточных, легочных, носовых, кишечных и желудочных кровотечениях; при остром и хроническом отравлении свинцом. В народной медицине - при туберкулезе легких, дизентерии, поносе, ревматизме, водянке, подагре, желтухе, заболеваниях печени, бронхите, атеросклерозе, при заболеваниях почек и мочевого пузыря (в том числе мочекаменной болезни); наружно в виде ванн, примочек и компрессов - при экземе, фурункулах, стригущем и зудящем лишаях; в виде полосканий - при стоматитах и других воспалительных процессах слизистой оболочки полости рта; в виде присыпок - для лечения ран и язв (как кровоостанавливающее и дезинфицирующее средство). Сок (внутрь) - как противовоспалительное, дезинфицирующее, вяжущее, мочегонное средство при болезнях почек и мочевого пузыря. Используют в качестве средства, улучшающего кровообращение при застойных явлениях, сопровождающих сердечные и другие заболевания, в особенности при плевритах с большим количеством экссудата, отеках. Показан как кровоостанавливающее средство при различных внутренних и наружных кровотечениях, в том числе геморроидальных, и обильных менструациях. Принимают при подагре, ревматизме. Наружно применяют в виде полосканий при афтозном и язвенном стоматитах, хроническом тонзиллите; в виде примочек и ванн - при хронических язвах, гнойных, вялотекущих ранах, фурункулах, экземах, свищах; в виде спринцеваний - при белях; в виде обмываний - при повышенной потливости. Помогает при себорейном дерматите.
Эссенция из свежего растения используется в гомеопатии.
Трава хвоща полевого входит в состав противоастматической микстуры по прописи Траскова, микстуры Здренко и мочегонных чаев.
Противопоказания и возможные побочные эффекты: хвощ полевой нельзя применять при нефритах и нефрозах, так как может вызвать раздражение почек. Принимать препараты из хвоща полевого необходимо под наблюдением врача, строго соблюдая назначенный режим лечения.
ОСНОВНЫЕ ВЕЩЕСТВА ТРАВЫ ХВОЩА ПОЛЕВОГО
(HERBAEQUISETIARVENSIS)
| № п/п | Наименование | Формула | Количество |
| 1 | Аскорбиновая кислота | 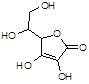 |
До 0,19% |
| 2 | Каротин |
α-каротин
|
|
| 3 | Сапонин | ||
| - эквизетонин | около 5 % | ||
| 4 | Флавоноиды | ||
| - кверцетин | 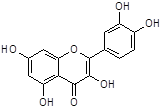 |
||
| -изокверцитин | |||
| - кемпферол | |||
| - лютеолин | 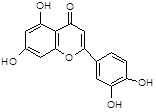 |
||
| - эквизетрин | |||
| 5 | Жиры | 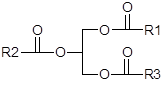 |
|
| 6 | Никотин | 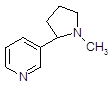 |
|
| 7 | Кислоты | ||
| - кремниевые | nSiO2 3mН2 O | ||
| -аконитовая | 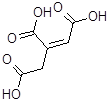 |
||
| - яблочная | 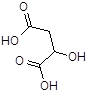 |
||
| - щавелевая | 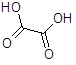 |
||
| 8 | Жирное масло | До 3,5% | |
| 9 | Горечи | ||
| 10 | Дубильные вещества | ||
| 11 | Смолистые вещества | ||
| 12 | Минеральные соли | ||
| 13 | Фенолкарбоновые кислоты | ||
| 14 | Ситостерол | 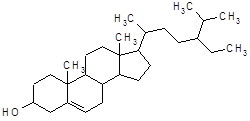 |
|
| 15 | Силикаты | Около 10% |
РАСТВОРИТЕЛИ
Аскорбиновая кислота
Аскорбиновая кислота - это белые кристаллы с резким кислым вкусом. Температура плавления аскорбиновой кислоты составляет 192 °С (при нормальных условиях). Аскорбиновая кислота устойчива в твердом состоянии.
Растворимость аскорбиновой кислоты (грамм на 100 мл растворителя): 33,3 H2 O, 2 EtOH. Аскорбиновая кислота нерастворима в диэтиловом эфире, CHCl3 , бензоле, петролейном эфире. Водные растворы аскорбиновой кислоты имеют pH ~ 3; действует как моноосновная кислота. Аскорбиновая кислота мощный восстановитель, легко окисляется многими окислителями.
Водные растворы аскорбиновой кислоты устойчивы при отсутствии кислорода. На воздухе растворы аскорбиновой кислоты устойчивы при pH 5-6, очень неустойчивы при щелочном pH.
Аскорбиновая кислота используется как донор H (водород) в биологических системах при изучении электронного транспорта и для защиты других легко окисляющихся веществ.
Каротин
Каротин (от лат. carota — морковь) — желто-оранжевый пигмент, непредельный углеводород из группы каротиноидов. Нерастворим в воде, но растворяется в органических растворителях. Содержится в листьях всех растений, а также в корне моркови, плодах шиповника и др. Является провитамином витамина А. Зарегистрирован в качестве пищевой добавки Е160a.
Сапонины
Сапонины (от лат. sapo-мыло), группа растительных гликозидов, водные растворы которых образуют стойкую мыльную пену; обладают гемолитической активностью и являются ядами для животных, дышащих жабрами. К сапонинам также относят гликозиды стероидов и тритерпеноидов морских организмов.
Сапонины - бесцветные или желтоватые кристаллиты, или аморфные вещества с высокой температурой плавления (плавятся с разложением); хорошо растворимы в воде, плохо - в холодном этаноле, лучше - в горячем и в метаноле, не растворимы в бензоле, хлороформе и диэтиловом эфире.
При кислотном или ферментативном гидролизе сапонины расщепляются на углеводную составляющую и агликон (сапогенин).
Сапонин эквизетонин при гидролизе расщепляется на эквизетогенин, фруктозу и арабинозу.
Флавоноиды
Флавоноиды — наиболее многочисленная группа как водорастворимых, так и липофильных природных фенольных соединений. Представляют собой гетероциклические кислородсодержащие соединения преимущественно желтого, оранжевого, красного цвета. Они принадлежат к соединениям С6 -С3 -С6 ряда — в их молекулах имеются два бензольных ядра, соединенных друг с другом трехуглеродным фрагментом. Большинство флавоноидов можно рассматривать как производные хромана или флавона.
Флавоноиды играют важную роль в растительном метаболизме и очень широко распространены в высших растениях. Многие флавоноиды — пигменты, придающие разнообразную окраску растительным тканям. Так, антоцианы определяют красную, синюю, фиолетовую окраску цветов, а флавоны, флавонолы, ауроны, халконы — жёлтую и оранжевую.
Они принимают участие в фотосинтезе, образовании лигнина и суберина, в качестве защитных агентов в патогенезе растений, вовлечены в регуляцию процессов прорастания семян, а также пролиферации и отмирания (путем апоптоза) клеток удлиняющихся растущих частей растений. Их многообразие объясняется тем, что в растениях большинство из них присутствует в виде соединений с сахарами — гликозидов. Сахарные остатки могут быть представлены моносахаридами — глюкозой, галактозой, ксилозой и др., а также различными ди-, три- и тетрасахаридами. К сахарным остаткам нередко присоединены молекулы оксикоричных и оксибензойных кислот. Катехины и лейкоантоцианы бесцветны. Они являются родоначальниками конденсированных дубильных веществ.
Большинство флавоноидов - твердые вещества, хорошо растворимые в полярных растворителях, в метаноле и бутаноле, в растворах гидроксида или карбоната натрия. Большинство флавоноидных гликозидов растворимо в воде, но их агликоны обычно плохо растворяются в ней. Агликоны растворимы в этилацетате, хлороформе, бензоле и эфире.
Кверцетин (3,3',4',5,7 - пентагидроксифлавон, мелетин, софоцетин) - лимонно-желтые кристаллы; температура плавления 313-314 °С (с разложением); слабо растворим в воде, диэтиловом эфире, этаноле, хлороформе, растворим в уксусной кислоте и щелочах. Растворы в концентрированной серной кислоте флуоресцируют зеленым цветом.
Кемпферол немного растворим в воде, растворим в горячем спирте, эфире.
Жиры
Жиры, или триглицериды — природные органические соединения, полные сложные эфиры глицерина и одноосновных жирных кислот; входят в класс липидов. Наряду с углеводами и белками, жиры — один из главных компонентов клеток животных, растений и микроорганизмов. Жидкие жиры растительного происхождения обычно называют маслами — так же, как и сливочное масло.
Жиры гидрофобны, практически нерастворимы в воде, хорошо растворимы в органических растворителях и обычно плохо растворимы в спирте.
Никотин
Никотин — бесцветная маслянистая жидкость (т. кип. 247,6 °С), быстро темнеющая на воздухе. При температурах ниже 60 °С и выше 210 °С никотин смешивается с водой, а в интервале температур от 60 °С до 210 °С он ограниченно растворяется в воде. Никотин хорошо растворяется во многих органических растворителях. Он экстрагируется органическими растворителями как из кислых, так и из щелочных водных растворов. Однако большие количества никотина экстрагируются из щелочных растворов. Никотин с водой образует азеотропную смесь. Поэтому он перегоняется с водяным паром.
Кислоты
Кремниевые кислоты - производные кремниевого ангидрида SiO2 ; очень слабые кислоты, малорастворимые в воде.
Растения некоторых семейств (хвощевых, бурачниковых и злаков) в большом количестве извлекают из почвы кремниевую кислоту и откладывают ее в своих клеточных оболочках или цитоплазме. Дело в том, что некоторые ее соли (силикаты) растворимы в воде. А так как кремниевая кислота - необходимая составная часть и человеческого организма (особенно соединительной ткани, кожи, волос и ногтей), можно с помощью содержащих кремниевую кислоту трав добиться улучшения состояния этих органов.
Аконитовая кислота легко растворима в воде и еще легче в спирте, а также и в абсолютном эфире; при 187 °С кристаллы ее плавятся, при чем происходит уже и распадение на угольный ангидрид (СО2 ) и итаконовую кислоту. Аконитовая кислота трехосновна, дает три ряда солей, представляющих собою продукт замещения металлами одного, двух или всех трех водородов карбоксильных групп, обусловливающих кислые свойства, т. е. основность всякой органической кислоты. Соли аконитовой кислоты большею частью растворимы в воде, хорошо кристаллизуются; средние соли свинца, серебра и окиси железа в воде не растворяются. Средний этиловый эфир аконитовой кислоты образуется при пропускании хлористого водорода через раствор кислоты в абсолютном спирте; он представляет тяжелую маслянистую жидкость, кипящую при 275° С (или 117° С при 14 т. т.) без разложения.
Яблочная кислота (2-гидроксибутановая кислота, гидроксиянтарная кислота) существует в виде двух стереоизомеров и рацемата. D, L-яблочная кислота- бесцветные кристаллы, температура плавления - 130,8 °С; растворимость (г в 100 г растворителя): в воде - 144 (26 °С), 411 (79 °С), в этаноле -35,9 (20 С), в диэтиловом эфире - 0,6 (20 °С), не растворима в бензоле.
Щавелевая кислота - относительно сильная органическая кислота (3 класс опасности), представляет собой бесцветные гигроскопичные кристаллы, легко растворима в воде, ограниченно - в этиловом спирте и диэтиловом эфире, нерастворима в хлороформе, петролейном эфире и бензоле. Образует дигидрат состава С2 Н2 О4 *2Н2 О. Горючее вещество, в осевшем состоянии пожароопасна. Обладает сильным раздражающим действием на кожу, слизистые оболочки глаз и верхних дыхательных путей.
Дубильные вещества
Дубильные вещества — группа весьма разнообразных и сложных по составу растворимых в воде органических веществ ароматического ряда, содержащих гидроксильные радикалы фенольного характера. Дубильные вещества широко распространены в растительном царстве, обладают характерным вяжущим вкусом. Они способны осаждаться из водного или водно-спиртового раствора раствором клея, а с солями окиси железа давать различных оттенков зелёные или синие окрашивания и осадки (чернильного свойства).
Дубильные вещества в основном аморфны, имеют более или менее ясно выраженный кислотный характер и обладают замечательным свойством (по преимуществу физиологические дубильные вещества) дубить кожу (шкуры), то есть отнимать у них в значительной мере способность к гниению и затвердеванию при высыхании.
Будучи веществами легко окисляющимися, они в присутствии щелочей буреют, поглощая кислород воздуха, и во многих случаях действуют восстановительно, напр., на соли благородных металлов, а некоторые и на Фелингову жидкость.
Для получения дубильного вещества в чистом состоянии природные дубильные материалы экстрагируют водой или другими растворителями: крепким или слабым спиртом, чистым эфиром или в смеси со спиртом, уксусным эфиром и т. п.; экстракты выпаривают, и получаемые в остатке дубильные вещества очищают с помощью обработки их теми или другими из указанных растворителей. Чаще, приготовив водный или водно-спиртовый экстракт, извлекают из него дубильное вещество взбалтыванием с уксусным или простым эфиром или с их смесью или же осаждают (лучше фракционированно) уксуснокислым свинцом и, отфильтровав, разлагают осадки свинцовых соединений сернистым водородом. Пользуются иногда для осаждения дубильных веществ из водных экстрактов уксуснокислым хинином, уксуснокислою медью, рвотным камнем, поваренною солью, соляной кислотой и др. Для очищения прибегают иногда к помощи диализа, дающего с таннином хорошие результаты.
Силикаты
Силикаты - это соли кремниевых кислот, а также минералы, содержащие кремний. Силикат образуется путем соединения диоксида кремния и оксида другого химического элемента. Большинство силикатов представляют собой тугоплавкие, химически пассивные материалы, практически не растворяющиеся в воде. При различной температуре они могут находиться в твердом, жидком (расплавленном) или газообразном состоянии, а также способны образовывать коллоидные системы.
ЛИТЕРАТУРА
1. Лекарственные растения луга. — М.: Изобразительное искусство, 1993. — С. 56-57.
2. http://lekmed.ru/lekarstva/lekarstvennye-rasteniya/hvosch-polevoi.html
3. http://www.herbarius.info/special/classificators/alpha_rus.phtml
4. http://fito-ter.ru/archives/334
5. http://ru.wikipedia.org/wiki/Кверцетин
6. http://ru.wikipedia.org/wiki/Аскорбиновая_кислота
7. Каррер П. Курс органической химии. 2 изд. - Л. - 1962.
8. http://www.xumuk.ru/toxicchem/98.html
9. http://www.xumuk.ru/encyklopedia/2170.html
10. http://www.xumuk.ru/encyklopedia/2/2987.html
11. http://ru.wikipedia.org/wiki/Малат
12. http://ru.wikipedia.org/wiki/Щавелевая_кислота
13. http://ru.wikipedia.org/wiki/Фитостерол
14. http://ascorbinka.x51.ru/index.php?mod=text&selected&uitxt=421&sw=%F0%E0%F1%F2%E2%EE%F0%E8%F2%E5%EB%E5
15. http://www.xumuk.ru/encyklopedia/2/3961.html
16. http://www.xumuk.ru/encyklopedia/1954.html
17. http://russian.alibaba.com/product-cgs/kaempferol-98--252127793.html
18. http://ru.wikipedia.org/wiki/Флавоноиды
19. http://www.oxbow.ru/?page_id=196
20. http://ru.wikipedia.org/wiki/Жир
21. http://www.xumuk.ru/toxicchem/98.html
22. http://be.sci-lib.com/article001595.html
23. http://www.xumuk.ru/encyklopedia/2/5456.html
24. http://chemical.technohim.ru/catalog/special/sorrel/
25. http://ru.wikipedia.org/wiki/Дубильные_вещества
26. http://www.compass-kazan.ru/information/silikaty/
8-09-2015, 19:32

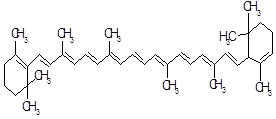
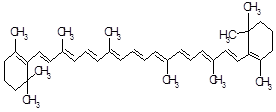 β-каротин
β-каротин