Содержание
Введение
1. Становление науки о силикатах
2. Кристаллохимическая систематика силикатов
3. Процессы образования силикатов в земной коре
4. Яркие представители группы силикатов
5. Применение и искусственное происхождение силикатов
Заключение
Список используемой литературы
Введение
Силикаты и алюмосиликаты представляют собой обширную группу минералов. Для них характерен сложный химический состав и изоморфные замещения одних элементов и комплексов элементов другими. Главными химическими элементами, входящими в состав силикатов, являются O, Si, Al, Fe2+ , Fe3+ , Mg, Mn, Ca, Na, K, а также Li, B, Be, Zr, Ti, F, H, в виде (OH)1- или H2 O и др.
Общее количество минеральных видов силикатов около 800. По распространённости на их долю приходится более 90% минералов литосферы. Силикаты и алюмосиликаты являются породообразующими минералами. Из них сложена основная масса горных пород: полевые шпаты, кварц, слюды, роговые обманки, пироксены, оливин и др. Самыми распространёнными являются минералы группы полевые шпаты и затем кварц, на долю которого приходится около 12% от всех минералов.
1. Становление науки о силикатах
Хотя история развития человеческого общества тесно переплетена с использованием силикатов как природного, так и искусственного происхождения, научный подход к изучению этих соединений сформировался относительно поздно – в конце XVIII – начале XIX столетия вместе со становлением химической науки. Это объясняется и специфическими особенностями силикатов: сложностью строения, вариациями химического состава, нерастворимостью и химической пассивностью, способностью к переходу в нестабильные состояния и высокой температурой плавления.
Первой научной теорией по систематике силикатов была так называемая поликремневая теория силикатов, которая на протяжении длительного времени (конец первой половины XIX ‑ 20-е годы XX века) играла важную роль в химии силикатов. Согласно этой теории, силикаты рассматривались как соли кремниевых кислот общей формулы nSiO2 " mH2O (n, m – целые числа). Значениям n > 1 соответствовали поликремневые кислоты. Простейшими представителями кремниевых кислот являются метакремневая H2SiO3 (n = 1, m = 1), ортокремневая Н4SiO4 (n = 1, m = 2), двуметакремневая H2Si2O5 (n = 2, m = 1), пирокремневая H6Si2O7 (n = 2, m = 3). Соли этих кислот получили названия мета-, двумета-, орто- и пиросиликатов соответственно. Для простых силикатов такие названия общеприняты и в настоящее время. Невозможность выделения кремниевых кислот в чистом виде из-за их коллоидного характера оставляла открытым вопрос о солеобразной природе силикатов. Более того, многообразие силикатов не укладывалось в рамки этой теории. Например, минералы жадеита NaAlSi2O6 и лейцита KAlSi2O6 относятся, казалось бы, к солям метакремниевой кислоты, но по своим свойствам сильно отличаются друг от друга. В приведенном случае поликремневая теория не смогла дать ответ о связи между химическим составом силикатных соединений и их строением, что является основной задачей любой систематики. Однако при формировании поликремневой теории была высказана гениальная догадка о полимеризации атомов кремния через атомы кислорода.
В своих трудах, посвященных природе силикатов, Д.И. Менделеев указывал на противоречия поликремневой теории. Он высказал идею об изоморфном замещении в силикатах не только оксидов одинакового типа, но и разных, таких, как SiO2 и Al2O3. Это наводило на мысль о сходстве и химических свойств этих оксидов. Далее на основании достаточно широкой вариации соотношения между основными и кислотными оксидами в силикатах Д.И. Менделеев отмечал, что нельзя объяснить все многообразие силикатов только существованием полимерных форм кремниевых кислот. По его мнению, силикаты представляют собой не соли, а «неопределенные соединения», такие, например, как сплавы, но не простых тел, а близких по своим свойствам оксидов. Д.И. Менделеев объяснял особенности силикатных «неопределенных соединений» не существованием различных видов поликремневых кислот, а полимеризацией большинства соединений кремния. Учение Д.И. Менделеева сыграло большую роль в дальнейшем понимании природы силикатов. В конце XIX века химические методы исследования (аналитические и синтетические) исчерпали свои возможности в познании силикатов. Исследователи начали искать новые пути решения проблем силикатов. Наиболее значительные результаты были достигнуты в физико-химическом и геохимическом направлениях.
Метод физико-химического анализа, созданный Н.С. Курнаковым в 20-е годы XX столетия, представляет собой синтез идей химической термодинамики и топологии. В рамках этого метода наиболее информативным оказалось рассмотрение диаграммы температура-состав (диаграмма состояния). Диаграммы состояния позволяют судить о температурно-концентрационных интервалах существования кристаллических и жидких силикатов, их превращениях (плавление, кристаллизация, разложение или соединение). Результаты многочисленных исследований диаграмм состояния (бинарных, тройных и более компонентных систем) обобщаются в соответствующих справочниках, в компьютерных банках данных, монографиях и учебных пособиях. Особенный интерес диаграммы состояния представляют для понимания процессов минералообразования, в материаловедении и технологии силикатов. В настоящее время использование термодинамического метода позволяет корректировать экспериментально полученные диаграммы состояния, предсказывать диаграммы состояния неизученных систем, судить о возможности протекания тех или иных процессов превращений силикатов, рассчитывать энергоемкость этих процессов, сравнивать устойчивость образовавшихся соединений по отношению к распаду на близлежащие по диаграмме состояния. Эти выводы делаются как на базе экспериментальных данных, так и с помощью разнообразных модельных представлений. В этой области автором и его сотрудниками получены интересные результаты, касающиеся устойчивости силикатных соединений, определения областей кристаллизации из расплавов тех или иных силикатов.
Видным представителем геохимического направления является В.И. Вернадский, который интересовался именно строением силикатов. Он создал свою теорию строения алюмосиликатов (1891–1937 годы). В.И. Вернадский так же, как и Д.И. Менделеев, говорил о близости химических функций SiO2 и Al2O3 и отвергал мысль о том, что алюмосиликаты есть соли кремниевых кислот. По его мнению, алюмосиликаты являются производными сложных алюмосиликатных радикалов, «каолиновых ядер». Гипотеза о «каолиновом ядре» как о замкнутой группировке атомов Si, Al и O оказалась актуальной при расшифровке структуры полевых шпатов.
2. Кристаллохимическая систематика силикатов
По хим. природе С. и в особенности С. сложного состава и строения (в т.ч. цементные гидросиликаты, цеолиты, С. с добавочными анионами и комплексными катионами) относятся к типичным гетеродесмич. соединениям, в к-рых реализуются одновременно разл. типы хим. связи-ионная, ковалентная, ионно-ковалентная, координационная, водородная и др. многоцентровые связи.
Структурная классификация С. базируется на рентгено-структурных расшифровках кристаллич. строения важнейших породообразующих силикатных минералов (преим. с мелкими катионами Be, Mg, Al, Zn, Fe, отчасти Na и К), выполненных начиная с кон. 20‑х гг. У. Брэггом, Л. Полин-гом, Нараи Сабо. В основу структурной систематики С. (Брэгг, Ф. Махачки) было положено строение анионных группировок-способ сочленения между собой элементарных звеньев-правильных кремнекислородных тетраэдров ![]() (рис. 1) в анионные радикалы конечных размеров или же в бесконечные одно-, двух- и трехмерные группировки. С 1950 в рентгеноструктурных исследованиях преим. школы Н.В. Белова были расшифрованы мн. кристаллич. структуры С. и их неорг. аналогов с крупными катионами Na, К, Са, Ва, РЗЭ и др. В основе систематики кремнекислородных группировок по Брэггу лежит размерное соответствие ребер тетраэдров SiO4
и октаэдров MgO6
. По Белову для кристаллохимии С. характерно стерич. соответствие ребра октаэдра СаО6
с расстоянием между вершинами диорто-группы
(рис. 1) в анионные радикалы конечных размеров или же в бесконечные одно-, двух- и трехмерные группировки. С 1950 в рентгеноструктурных исследованиях преим. школы Н.В. Белова были расшифрованы мн. кристаллич. структуры С. и их неорг. аналогов с крупными катионами Na, К, Са, Ва, РЗЭ и др. В основе систематики кремнекислородных группировок по Брэггу лежит размерное соответствие ребер тетраэдров SiO4
и октаэдров MgO6
. По Белову для кристаллохимии С. характерно стерич. соответствие ребра октаэдра СаО6
с расстоянием между вершинами диорто-группы![]() . Это наиб. наглядно иллюстрируется сочленением кремнекислородных цепочек с октаэдрич. колонками Са- и Mg‑октаэдров в структурах пироксена энстатита Mg2
(Si, O6
),
(рис. 2, а) и пироксеноида волластонита Са3
(Si3
O9
),
(рис. 2, б).
. Это наиб. наглядно иллюстрируется сочленением кремнекислородных цепочек с октаэдрич. колонками Са- и Mg‑октаэдров в структурах пироксена энстатита Mg2
(Si, O6
),
(рис. 2, а) и пироксеноида волластонита Са3
(Si3
O9
),
(рис. 2, б).
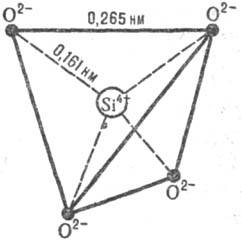
Рис. 1. Элементарный правильный кремне-кислородный тетраэдр SiO4 4-
Для кристаллохимии С. по Белову определяющим критерием конструирования или формирования типа кристаллич. структуры С. и их неорг. аналогов явился принцип «приспособляемости» кремнекислородных анионных группировок к существенно более крупным полиэдрам катионов. При классификации С. выделяют элементарное звено, участвующее в построении кремнекислород-ного![]() анионного каркаса, – орто-, диорто- и триортогруппы.
анионного каркаса, – орто-, диорто- и триортогруппы.
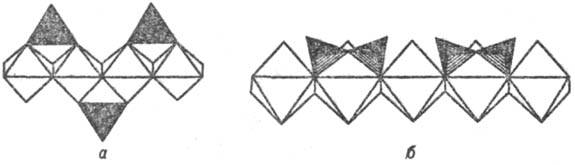
Рис. 2. Элементарные кремнекислородные единицы-ортогруппы![]() в структуре Mg‑пироксена энстатите (а) и диортогруппы
в структуре Mg‑пироксена энстатите (а) и диортогруппы![]() в Са-пироксеноиде волластоните (б).
в Са-пироксеноиде волластоните (б).
В целом С. могут быть подразделены на два класса: соединения с конечными размерами кремнекислородных группировок (островные структуры) и с бесконечными повторениями кремнекислородных тетраэдров при самых разл. способах их сочленения (полимерные, или конденсир., структуры). Причем анионный остов кристаллич. решетки, наряду с кремнекислородными анионами, может включать И дополнит. анионы-О2-
, ОН-
, Cl-
, F-
, ![]() ,
,![]() и нек-рые др.
и нек-рые др.
Островные С. делятся на соед. с одиночными кремнекислородными тетраэдрами – ортосиликаты (рис. 3, а) и со сдвоенными тетраэдрами – диортосиликаты (рис. 3, б). К таким С. относятся оливины (MgFe)2
SiO4
, циркон ZrSiO4
, гранаты ![]() , где МII
= Mg, Ca, Fe(II), Mn(II), МIII
= Al, Fe(III), Сr(III), V(III) и др. Соед. со сдвоенными тетраэдрами-минералы группы тортвейтита Sc2
Si2
O7
, ме-лилита и обширный класс пиросиликатов РЗЭ (рис. 3, б). По сравнению с орто- и диортосиликатами значительно менее распространены С. с открытыми линейными три- и тетраор-тогруппами, напр. киноит Cu2
Ca2
Si3
O10
·2H2
O.
, где МII
= Mg, Ca, Fe(II), Mn(II), МIII
= Al, Fe(III), Сr(III), V(III) и др. Соед. со сдвоенными тетраэдрами-минералы группы тортвейтита Sc2
Si2
O7
, ме-лилита и обширный класс пиросиликатов РЗЭ (рис. 3, б). По сравнению с орто- и диортосиликатами значительно менее распространены С. с открытыми линейными три- и тетраор-тогруппами, напр. киноит Cu2
Ca2
Si3
O10
·2H2
O.
Среди природных и искусственных С. широко распространены соед. с циклич. (замкнутыми) кремнекислородными группировками из трех-, четырех-, шестизвенных (рис. 3, в, г, д) и более сложных (восьми-, девяти-, двенадцатичленных) колец. К данной группе островных метасиликатов относится, напр., псевдоволластонит -Ca3 Si3 O9 (рис. 3, в). В берилле Ве3 Al2 Si6 O18 реализуется шестичленный кольцевой анион (рис. 3, д) с двумя мостиковыми Si‑О–Si связями, приходящимися на каждый тетраэдр, как и в др. циклич. анионах.
Известны кристаллич. структуры островных С. со сдвоенными, конденсированными «двухэтажными» трех-, четырех-и шестизвенными кольцевыми анионами. Напр., в минерале эканите ThK (Ca, Na)2 Si8 O20 реализуется сдвоенный четы-рехзвенный кольцевой анион. Аналогичный кремнекисло-родный анион обнаружен в С. с комплексными катионными группировками, напр. тетраметиламмониевыми в соед. [N(CH3 )4 ]8 Si8 O20 . Сдвоенное «двухэтажное» шестизвенное кольцо обнаружено, в родственном бериллу С. миларите K(Be2 Al) Ca2 Si12 O30 . В «двухэтажных» циклич. кремнекислородных группировках число мостиковых связей на каждый тетраэдр повышается соотв. до трех. Для мн. сложных по составу островных С. характерно сочетание в анионном остове одновременно неск. разл. кремнекислородных группировок, чаще всего орто- и диортогрупп.
Класс полимерных, или конденсированных, С. подразделяют на 4 подкласса. 1) Цепочечные С. с бесконечными цепочками из одиночных кремнекислородных тетраэдров, каждый из к-рых с соседними имеет по две мостиковые связи. Данный структурный тип метасиликатов охватывает большую группу породообразующих минералов и их синте-тич. аналогов, моноклинных и ромбич. пироксенов и пиро-ксеноидов широкого диапазона составов: энстатит (MgFe)2 (Si2 O6 ), диопсид CaMg(Si2 O6 ), сподумен LiAl(Si2 O6 ), волластонит – Са3 (Si3 O9 ), родонит CaMn4 (Si5 Oi5), и мн. др. представители пироксен-пиро-ксеноидных С. (рис. 4) с периодом повторяемости из 2, 3, 5 кремнекислородных тетраэдров и более вдоль оси цепочки.
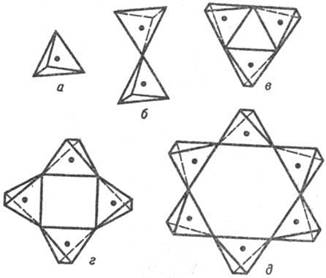
Рис. 3. Простейшие типы островных кремнекислородных анионных группировок: а-SiO4 , б-Si2 O7 , в-Si3 O9 , г-Si4 О12 , д-Si6 O18 .
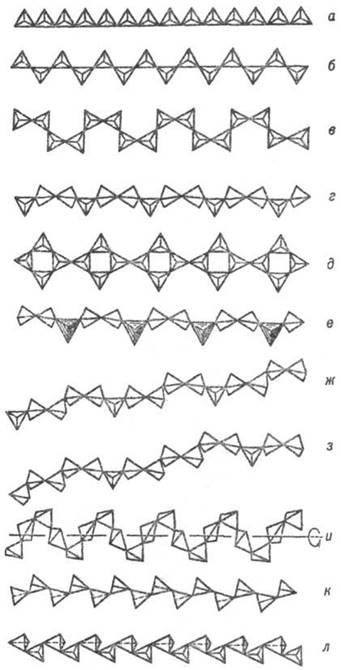
Рис. 4. Важнейшие типы кремнекислородных цепочечных анионных группировок (по Белову): а-метагерманатная, б – пироксеновая, в-батиситовая, г-вол-ластонитовая, д-власовитовая, е-мелилитовая, ж-родонитовая, з-пирокс-мангитовая, и-метафосфатная, к-фторобериллатная, л – барилитовая.
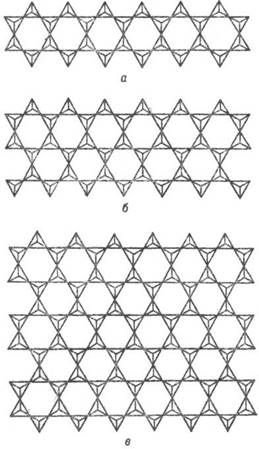
Рис. 5. Конденсация пироксеновых кремнекислородных анионов в ленточные двухрядные амфиболовые (а), трехрядные амфиболоподобные (б), слоистые тальковые и близкие им анионы (в).

Рис. 6. Структурно-гомологический ряд кремнекислородных анионных группировок ксонотлита (а) и тоберморита (б); волластонит-см. рис. 4, г.
2) С. с ленточными кремнекислородными анионами из двух-, трех- и n‑рядных цепочек, сконденсированных между собой по боковым связям перпендикулярно цепочке (рис. 5). В природе наиб. распространены в данном подклассе в-в амфиболовые и амфиболоподобные асбесты – волокнистые С. с двухрядными ленточными анионами, важнейшие представители – минералы тремолит Ca2 Mg5 (Si8 O22 XOH)2 и роговые обманки (Na, Ca)2 (MgAl)5 (Al, Si)8 O22 (OH)2 . Ленточный анион цементного минерала ксонотлита Ca6 (Si6 O17 ) (OH)2 (рис. 6, а) – продукта конденсации волластонитовых цепочек (рис. 2, б или 4, г) – состоит из восьмичленных колец, в отличие от шестизвенных гексагон. колец амфиболовых лент (рис. 5, а, 6,7).
3) С. с двухмерными слоистыми или листовыми анионами характеризуются широким разнообразием возможных сочленений кремнекислородных тетраэдров в правильные или же в низкосимметричные шести-, четырех- и восьмичленные кольца с тетрагон. и ромбич. симметрией слоя, восьми-, шести- и четырехчленные кольца, воедино связанные в слоистом анионе, и т.д. (рис. 5, в, 6, б).
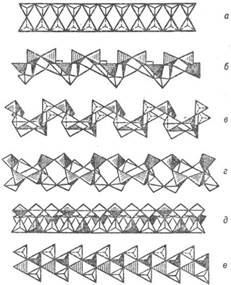
Рис. 7. Важнейшие типы ленточных кремнекислородных группировок (по Белову): а – силлиманитовая, амфиболовая-см. рис. 5, а, ксонотлитовая-см. рис. 6, а; б-эпидидимитовая; в-ортоклазовая; г-нарсарсукитовая; д-фенаки-товая призматическая; е-эвклазовая инкрустированная.
В прир. – слоистых С. группы слюд (мусковит ![]() , биотит
, биотит![]() тальк, пирофиллит и др.), глинистых
тальк, пирофиллит и др.), глинистых![]() минералов [каолинита Al4
(Si4
O10
) (OH)8
и др.] кремнекислородные сетчатые анионы образованы правильными шестичленными кольцами из тетраэдров SiO4
. Эти сетки являются продуктом конденсации пироксеновых или же амфиболовых лент (рис. 5). Строение слоистых С. предопределяет их отчетливую спайность по базальной плоскости (параллельно слоям), наиб. отчетливо проявляющуюся в слюдах (рис. 8). При конденсации в плоскости волластонитовых цепочек (Si3
О9
),
(рис. 2, б или 4, г) или же ксонотлитовых лент (Si6
O17
),
(рис. 6, а) образуются тетрагон, тоберморитовые сетки Ca5
(Si6
O16
) (OH)2
·4H2
0 (рис. 6, б).
минералов [каолинита Al4
(Si4
O10
) (OH)8
и др.] кремнекислородные сетчатые анионы образованы правильными шестичленными кольцами из тетраэдров SiO4
. Эти сетки являются продуктом конденсации пироксеновых или же амфиболовых лент (рис. 5). Строение слоистых С. предопределяет их отчетливую спайность по базальной плоскости (параллельно слоям), наиб. отчетливо проявляющуюся в слюдах (рис. 8). При конденсации в плоскости волластонитовых цепочек (Si3
О9
),
(рис. 2, б или 4, г) или же ксонотлитовых лент (Si6
O17
),
(рис. 6, а) образуются тетрагон, тоберморитовые сетки Ca5
(Si6
O16
) (OH)2
·4H2
0 (рис. 6, б).
4) К С. каркасного строения относятся многочисл. группы алюмосиликатов (в меньшей степени – боросиликаты), вязаный каркас к-рых образован четырьмя мостиковыми связями и имеет общую ф-лу (Alm Sin _m O2n )m- Избыточный отрицат. заряд анионного остова из (Аl, Si) – теграэдров электростатически компенсируется щелочными и щел.-зсм. катионами, располагающимися в полостях каркасной структуры. Среди каркасных алюмосиликатов более всего в природе распространены щелочные полевошпатовые С.: твердые р-ры альбита NaAlSi3 O8 и ортоклаза KAlSi3 O8 , а также альбита и анортита CaAl2 Si2 O8 , известные под назв. плагиоклазов. Каркасные С. цеолиты характеризуются большими внутр. полостями и входными окнами, в к-рых могут абсорбироваться крупные молекулы диаметром 0,3–0,5 нм и более (рис. 9).
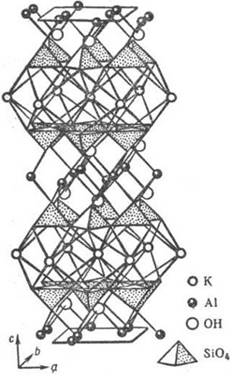
Рис. 8. Фрагмент (элементарный пакет) слоистой кристаллич. структуры мусковита KAl2 (AlSi3 O10 XOH)2 , иллюстрирующий переслаивание алюмокремне-кислородных сеток с полиэдрич. слоями крупных катионов Аl и К.
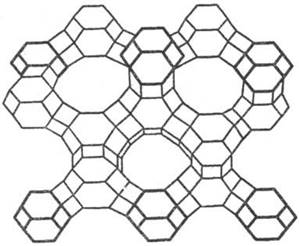
Рис. 9. Проекция фрагмента пористой кристаллич. структуры цеолита фошазита (фожазита) с широкими входными каналами эллиптич. сечения.
3. Процессы образования силикатов в земной коре
Теперь рассмотрим минеральный состав земной коры с позиций строения кремнекислородных радикалов. За счет внутренней энергии Земли магма – расплав, состоящий из основных пород (ортосиликаты магния и железа и их твердые растворы), поднимаясь по трещинам на поверхность, обогащается кремнеземом, глиноземом, водой. При этом с понижением температуры из него кристаллизуются сначала тугоплавкие минералы, а оставшийся расплав снова взаимодействует с встречающимися на его пути породами, образующиеся кристаллы взаимодействуют с гидротермальными водами. Из образовавшихся растворов выкристаллизовываются минералы, содержащие воду. Безусловно, это очень упрощенная картина сложных геохимических процессов, происходящих в действительности. К основным минералам относятся оливины – ортосиликат магния Mg2SiO4, в котором часть катионов магния может быть замещена на Fe2 +. Поэтому для оливинов принимается общая формула [Mg, Fe] 2 [SiO4], а их структура образована изолированными тетраэдрами [SiO4] 4 -, соединенными между собой катионами. При увеличении содержания SiO2 образуются пироксены – метасиликаты натрия, магния, кальция, железа, содержащие бесконечные метасиликатные цепочки (SiO3)?. В зависимости от природы катиона найдены различные виды изолированных и более сложных цепочек. Минерал жадеит NaAl[Si2O6], о котором шла речь, также относится к группе пироксенов, то есть к минералам с цепочечной структурой. Ионы натрия и алюминия образуют катионную составляющую структуры.
Следующей ступенью полимеризации являются соединения, содержащие ленточные кремнекислородные радикалы. Некоторые виды этих радикалов, зависящие от природы катионов, представлены на рис. 3. Во времена У.Л. Брэгга такие соединения еще не были известны. К ленточным силикатам относятся амфиболы – гидросиликаты Ca, Mg, Fe, содержащие группы [Si4O11] 6 – К амфиболам относится и один из древнейших минералов, используемых человеком, – нефрит – Ca2 (Mg, Fe) [Si4O11] (OH) 2, и асбесты.
Дальнейшая конденсация приводит к образованию слоистых силикатов. К их числу относятся слюды и глины, содержащие в своей структуре группировки [Z4O10], где Z=Si и Al в четверной координации относительно кислорода. В слюдах слои состоят из шестичленных колец, построенных из алюмо- и кремнекислородных тетраэдров. Слоистых силикатов существует множество: слои могут быть построены из пяти- и шестичленных колец (см. рис. 1); состоять из чередующихся в определенном отношении восьми- и пятичленных колец; могут существовать слои, в которых кремнекислородный тетраэдр необязательно имеет три мостиковых атома кислорода, и др.
И наконец, последней ступенью полимеризации являются силикаты с каркасным строением, которых тоже существует великое множество. Примером каркасных силикатов могут служить кремнезем и полевые шпаты. Полевые шпаты делятся на плагиоклазы (непрерывный ряд твердых растворов в системе альбит-анортит (NaAlSi3O8‑CaAl2Si2O8)) и калиевый полевой шпат K[AlSi3O8]. Их структура представляет собой бесконечный объемно-увязанный каркас из тетраэдров SiO4 и AlO4, в пустотах которого расположены ионы Na, Ca, K (рис. 4). Сам же кремнезем – это вязь из кремнекислородных тетраэдров. К разряду каркасных силикатов, но не полевых шпатов относится и упоминаемый ранее минерал лейцит K[AlSi2O6], казалось бы, метасиликат калия и алюминия. В действительности это каркасный алюмосиликат, в котором атомы алюминия выполняют структурную функцию атомов кремния. Каркас состоит из тетраэдров AlO4 и SiO4 (все атомы кислорода мостиковые), в пустотах которого расположены ионы калия. Полевые шпаты, в свою очередь, в результате процессов выветривания превращаются в
29-04-2015, 00:36
