РЕФЕРАТ НА ТЕМУ:
ГЕРПЕС. ЭТИОЛОГИЯ И ПАТОГЕНЕЗ.
Общая характеристика герпетическоЙ инфекции
Вирусы (от лат.virus — яд) — мельчайшие доклеточные живые образования, основным условием осуществления жизненного цикла которых является паразитирование в клетке, предоставляющей свои структуры, ферменты, материалы и энергию для репродукции вируса.
Вирусные заболевания могут иметь различное клиническое течение, в связи с чем инфекцию классифицируют как очаговую и генерализованную , каждая из которых может быть острой или персистентной (схема 1). Острая инфекция может протекать без клинических симптомов (инаппарантная инфекция) или иметь характерные клинические симптомы (манифестная инфекция). К персистентной инфекции относят истинно латентную (вирус остается в организме хозяина в скрытой форме), латентную с периодическими абортивными рецидивами , хроническую (с постоянным воспроизводством и выделением вируса) и медленную (с многодневным циклом удвоения вируса и инкубационным периодом, продолжающимся годами).
Семейство Herpesviridae (от греч. h é rp е s — лишай) объединяет 80 вирусов, 8 из которых связаны с патологией человека. Герпесвирусы этого семейства вызывают различные заболевания, в том числе с проявлениями в полости рта (табл. 1).
Все описанные герпесвирусы имеют сходные структурные характеристики. С точки зрения патологии человека, герпесвирусы объединены способностью персистентной инфекции, характер которой и определяет широкой спектр проблем эпидемиологического контроля, клинической и лабораторной диагностики, этиотропной и патогенетической терапии.
| Очаговая инфекция | Генерализованная инфекция | |||||||||||||||||
| острая | персистентная | острая | персистентная | |||||||||||||||
| манифестная | истинно латентная |
манифестная | истинно латентная |
|||||||||||||||
| инаппарантная | латентная с рецидивами |
инаппарантная | хроническая | |||||||||||||||
| хроническая | медленная | |||||||||||||||||
Схема 1. Классификация вирусной инфекции
Особенности каждой нозологической формы герпетической инфекции определяются влиянием многих факторов, таких как: тип вируса, локализация входных ворот инфекции, способ распространения вируса в тканях организма, компетентность иммунной системы, первичный или вторичный характер инфекции и т. д.
Таблица 1
Герпесвирусы и патология человека
| Герпесвирусы | Заболевания, ассоциируемые с первичной инфекцией | Заболевания, возникающие при активации латентной инфекции | ||
| Подсемейство и его свойства |
Тип | |||
| α | – тропность к эктодермальным тканям; – короткий репродуктивный цикл; – быстрое распространение; – литический цикл размножения; – латенция преимущественно в нервных ганглиях |
вирус простого герпеса 1 типа (син.: ВПГ-1, herpes simplex virus 1, HSV-1) | – врожденный и неонатальный герпес; – острый герпетический стомататит; – герпес кожи лица и верхних конечностей; – офтальмогерпес; – менингоэнцефалит |
– герпетический стоматит; – многоформная эксссудативная эритема; – офтальмогерпес; – менингоэнцефалит |
| вирус простого герпеса 2-типа (син.: ВПГ-2, herpes simplex virus 2, HSV-2) | – врожденный и неонатальный герпес; – генитальный герпес; – герпес кожи нижних конечностей; – менингоэнцефалит |
– герпес гениталий; – герпес кожи бедер, ягодиц, нижних конечностей; – миелит, энцефалит |
||
| вирус ветряной оспы (син.: вирус герпеса человека 3-го типа, HHV-3, herpes zoster, varicella zoster virus , VZV) |
– ветряная оспа; – пре- и перинатальная инфекция |
– опоясывающий лишай |
||
| Герпесвирусы | Заболевания, ассоциируемые с первичной инфекцией | Заболевания, возникающие при активации латентной инфекции | ||
| Подсемейство и его свойства | Тип | |||
– тропность к лимфоидным и железистым тканям; – длительный репродуктивный цикл; – увеличение зараженных клеток; – длительная персистенция; – латенция |
цитомегаловирус (син.: вирус герпеса человека 5-го типа, HHV-5, cytomegalovirus , CMV) | – тератогенные эффекты; – врожденная инфекция; – иммунодефицит; – патология органов дыхания; – язвенно-некротичес-кий гингивостоматит; – диссеминированная инфекция |
– ретинит; – колит; – стоматит; – энцефалит |
|
| γ | – лимфотропность (специфичность к Т- или В-лимфо-цитам); – пролиферация тканей и онкогенез; – латенция |
вирус герпеса человека 6-го типа (син.:HHV-6) | – кофактор ВИЧ; – синдромом хронической усталости; – оральная карцинома; – цервикальная карцинома |
– системная патология при пересадке органов и тканей; – гистиоцитоз из клеток Лангерганса |
| вирус герпеса человека 7-го типа (син.: HHV-7) | -синдром хронической усталости; -экзантема новорожденных |
системная патология при пересадке органов и тканей | ||
| вирус Эпштейн–Барра (син.: вирус герпеса человека 4-го типа, HHV-4, Epstein– Barr virus , EBV)- | – инфекционный мононуклеоз; – В-лимфопролифера-тивные заболевания; – карцинома; – лимфоэпителиома слюнной железы |
– назофарингеальная карцинома; – лимфома Беркитта; – идиопатическая лимфоцитарная пневмония; – лейкоплакия |
||
| вирус герпеса человека 8-го типа (син. HHV-8) | неизвестно | – Сакома Капоши, – первично распространяющаяся лимфома |
||
ПАТОГЕНЕЗ ОСТРОЙ ГЕРПЕТИЧЕСКОЙ ИНФЕКЦИИ
Патологические эффекты при вирусных заболеваниях являются совокупным результатом прямого воздействия вирусов на организм хозяина и повреждения тканей при иммунном ответе.
Ниже схематически представлены основные «клеточные» и «хозяйские» стадии взаимодействия герпесвирусов и человека. Этот перечень подробно раскрывает содержание классических стадий развития инфекционного заболевания: заражения, инкубационного периода, продромального периода, стадий разгара и разрешения клинических симптомов.
«Хозяйские» стадии вирусного патогенеза 1) проникновение вируса в организм; 2) первичное воспроизведение вируса в клетках в области входных ворот; повреждение клеток; 3) распространение вируса внутри хозяина; 4) распределение вируса в тканях в соответствии с клеточным и тканевым тропизмом; 5) воспроизведение в восприимчивых клетках; повреждение клеток; 6) иммунный ответ и другие защитные реакции хозяина; 7) персистенция, латенция инфекции |
«Клеточные» стадии вирусного 1) адсорбция на поверхности клетки; 2) слияние оболочек вируса и клетки; 3) проникновение «голого» вириона в клетку; 4) проникновение нуклеоида вируса в клеточное ядро; 5) использование вирусного генома и ферментов клеточного ядра для синтеза вирусных белков, необходимых для воспроизводства вируса; 6) репликация вирусного генома; 7) синтез капсомеров; 8) упаковка генома в капсид; 9) выведение нуклеокапсида из ядра; 10)дозревание вириона (создание внутренней и внешней оболочек); 11) выведение вириона из клетки |
Клеточные стадии патогенеза
Репликативный цикл вирусов простого герпеса
Вирусы семейства Herpesviridae , в том числе ВПГ-1 и ВПГ-2, представляют собой сферические образования диаметром 100–300 нм со сложной структурой, в которой различают как минимум 4 компонента:
а) нуклеоид — центральная часть вириона, представленная двумя нитями ДНК, намотанными на цилиндрический белковый стержень;
б) капсид (от лат. capsa — вместилище, футляр) — белковая капсула, в которую заключен нуклеоид; капсид имеет вид правильного двадцатигранника, собранного из сотен одинаковых белковых призматических полых капсомеров;
в) внутренняя оболочка (в англ. языке tegumen — покров) — суперкапсидная структура, представляющая собой трехслойную мембрану с неправильными очертаниями;
г) внешняя оболочка (в англ. языке envelope — чехол, обложка, конверт) — липо- и гликопротеидная структура неправильной формы с обращенными вовне выступами, покрывающая один или несколько нуклеокапсидов герпеса с их индивидуальными внутренними оболочками.
Заражение начинается с того, что вирус простого герпеса (ВПГ) прикрепляется гликопротеидами внешней оболочки (gB, gC и gD) к специфическим рецепторам мембраны клетки, чувствительной к ВПГ.
Как только устанавливается стабильное прикрепление, другие гликопротеиды внешней оболочки вируса (gH и gL) организуют слияние внешней оболочки вируса и клеточной мембраны.
Проникновение вирусного капсида, окруженного внутренней оболочкой, в клетку происходит путем почкования, без повреждения целостности клеточной мембраны. Продвижению вирусной частицы внутрь клетки способствует вирус-индуцированная микрофиламентная активность цитоскелета. Затем клеточные ферменты растворяют внутреннюю оболочку вируса, и «голый» капсид направляется к ядру клетки. Здесь ДНК вируса под контролем вирусных факторов выходит из капсида и через ядерную пору проникает в ядро клетки.
В ядре клетки происходит транскрипция вирусной ДНК.
ДНК ВПГ — крупная двухцепочечная молекула, в которой различают два ковалентно связанных компонента — длинный и короткий. Встречаются четыре варианта взаиморасположения компонентов, а также различные сочетания повторов и разрывов в нуклеотидных последовательностях, что обеспечивает многочисленность штаммов ВПГ (их известно более 120).
ДНК ВПГ содержит 84 различных гена, кодирующих белки для выполнения трех основных функций:
· ферменты для репликации вирусного генома: данные белки практически полностью обеспечивают процесс репликации, так что вирус на этом этапе нуждается лишь в нескольких клеточных белках. Следствием такой самодостаточности является высокая инфекционность герпевирусов;
· белки для упаковки воспроизведенного вирусного генома в капсид (клеточные белки к этому процессу не привлекаются вовсе) и гликопротеиды для синтеза оболочек вируса;
· белки для изменения структуры и/или функции зараженных клеток в интересах вируса (для этой цели служат не менее 47 генов из 84).
Транскрипция ДНК ВПГ происходит в клеточном ядре с участием клеточной ДНК-зависимой РНК-полимеразы (поэтому репликация ВПГ возможна лишь в клетках, способных к размножению, и маловероятна в нервных клетках).
Трансляция, синтез и процессинг белков вируса простого герпеса происходит в основном в цитоплазме клетки с участием как клеточных, вирусиндуцированных и вирусных ферментов, синтезированных на ранних этапах репродукции.
Синтез белков осуществляется в той же последовательности, что и их транскрипция.
Для сборки вириона синтезированная в цитоплазме ДНК ВПГ возвращается в ядро и претерпевает некоторые изменения конфигурации, необходимые для предстоящей упаковки в капсид. Здесь же накапливаются капсомеры (белки для их создания синтезируются в цитоплазме, а затем избирательно транспортируются в ядро), из капсомеров собираются пустые капсиды, внутри которых размещается ДНК ВПГ.
Сформированный нуклеокапсид прикрепляется к ламеллам внутренней мембраны ядра и «почкуется» в цитоплазму.
Судьба зараженной клетки
Репродукция ВПГ наносит прямой вред пораженной вирусом клетке:
· вирус качественно изменяет мембраны зараженных клеток, чем провоцирует их слияние и образование гигантских многоядерных клеток-симпла-стов еще до того, как начинает размножаться;
· вирусиндуцированные изменения клеточной мембраны приводят к нарушению транспорта электролитов и утечке макромолекул клетки через плазматическую мембрану;
· вирус избирательно воздействует на синтетический аппарат клетки:
– выключает синтез белков клетки («вирусная блокада белков») и метаболизм других ее макромолекул (вирус производит белок ICP47, который инактивирует и разрушает клеточную и-РНК и, таким образом, прекращает транскрипцию клеточной ДНК);
– искажает митотический режим клетки (замедляется темп деления клеток, растет доля патологических митозов).
Клетки, в которых ВПГ активно реплицируется (в одной клетке может быть синтезировано до 200 вирионов!), не выживают, поэтому ВПГ считают литической инфекцией.
Помимо прямого негативного воздействия на клетку, ВПГ провоцирует иммунное разрушение клетки: встраивая гликопротеиды своей внешней оболочки в клеточную мембрану, ВПГ передает ей свои антигенные свойства и превращает клетку в мишень для иммунных сил.
Хозяйские стадии патогенеза
Механизмы распространения вируса в организме
Внедрение ВПГ в организм чаще всего происходит через поврежденную кожу или неповрежденный эпителий. Клетки кожи эпителия роговицы, эпителия слизистых оболочек гениталий и полости рта имеют рецепторы к ВПГ, поэтому являются высокочувствительными к герпетической инфекции, что позволяет им играть роль входных ворот.
Контакт ВПГ в области входных ворот происходит не только с эпителиоцитами, но и с расположенными здесь нервными окончаниями (они тоже имеют рецепторы для ВПГ), а также клетками миелоидного и лимфоидного ряда.
Распространение ВПГ по организму происходит несколькими способами — как по поверхности, так и вглубь тканей организма:
· со слюной, пищей при глотании;
· при переносе инфицированной слюны на кожу пальца, лица, головы (аутозаражение);
· при делении инфицированной клетки;
· по межклеточным мостикам;
· через межклеточное пространство;
· с током лимфы и крови;
· в связи с клетками крови (эритроцитами, лифоцитами, макрофагами, тромбоцитами);
· в нервных тканях — по периневральному пространству или по цепочке делящихся шванновских клеток, или с током аксоплазмы.
Первичное распространение ВПГ от входных ворот по организму проявляется в т. н. первичной вирусемии — ВПГ в течение нескольких дней накапливается в кровеносном русле (при этом плотность вирионов достигает 103 в 1 мл крови) и приносится в ткани-мишени, в частности, в слизистую оболочку полости рта.
Активная репликация ВПГ в эпителиоцитах и иммунный ответ на инфекцию приводит к разрушению клеток, нарушению целостности тканей и таким образом формирует местные проявления герпетического стоматита .
Высвободившиеся из клеток вирусы-потомки (и продукты распада тканей) попадают в ток крови — наступает период вторичной вирусемии , когда плотность ВПГ достигает 106 частиц в 1 мл крови. С периодом вторичной вирусемии связаны явления интоксикации, поражение тканей экто-, мезо- и энтодермального происхождения во внутренних органах: в печени, селезенке, легких, желудочно-кишечном тракте и т. д. С вирусным поражением стволовых клеток, участвующих в процессах синтеза коллагена, связывают нарушения в синтезе соединительной ткани стенок мелких капилляров и, соответственно, геморрагические явления в области герпетического поражения.
Для прекращения острых проявлений заболевания необходимо установить контроль над репродукцией ВПГ при помощи иммунных сил и/или лекарственных препаратов.
Иммунная защита от герпетической инфекции
Защита организма от острой вирусной инфекции обеспечивается последовательным включением нескольких взаимодействующих систем:
· врожденной (неиммунной) резистентности;
· неспецифического гуморального и клеточного иммунитета;
· адаптивного (специфического) гуморального и клеточного противогерпетического иммунитета.
Организация иммунной защиты соответствует особенностям паразитирования вирусов в организме: иммунитет направлен как против свободных вирионов, находящихся вне клеток, так и против собственных клеток, продуктивно зараженных ВПГ (схема 2.).
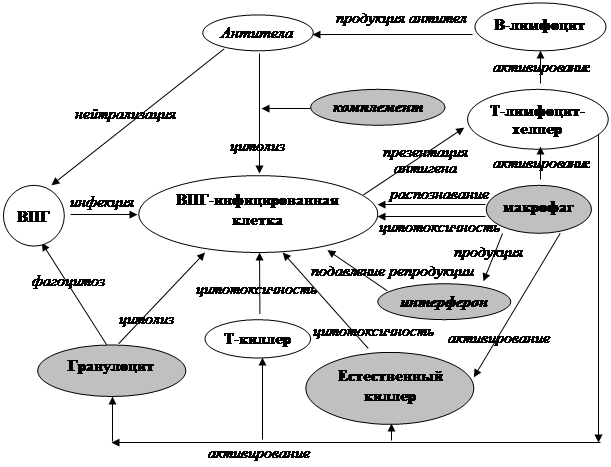
Схема 2. Основные этапы и факторы иммунного ответа на первичную инфекцию ВПГ
Врожденная (неиммунная) резистентность
Многие ткани организма невосприимчивы к ВПГ потому, что клеточные мембраны составляющих их клеток не имеют рецепторов для адгезии вириона.
Для кожи важным фактором безопасности является сохранность целостности, так как неповрежденный роговой слой является механическим барьером, устойчивым к инвазии ВПГ. Поверхность кожи и СОПР покрыта секретом желез, обладающими защитными свойствами.
На стадиях развернутой инфекции для борьбы с вирусом мобилизуются силы врожденной резистентности,проявляющейся на уровне всего организма: создаются условия, неблагоприятные для репродукции вируса (гипертермия, гипоксия, ацидоз) и способствующие скорейшему выведению вируса из организма (слюнотечение, кашель, полиурия).
Неспецифическая противовирусная иммунная защита
При внедрении вируса в ткани в действие вступают факторы неспецифического иммунитета — гуморального (интерфероны и другие цитокины, лизоцим, естественные антитела, белки системы комплемента) и клеточного (естественные киллеры, макрофаги, полиморфно-ядерные лейкоциты).
· Неспецифический гуморальный иммунитет.
Интерфероны — гликопротеиды, синтезируемые иммунными клетками под влиянием чужеродных индукторов. Различают около 20 разновидностей интерферонов, распределенных в три основных класса:
– интерферон-α — вырабатывается лейкоцитами, активен против вирусной инфекции;
– интерферон-β — вырабатывается фибробластами, активен против вирусной инфекции;
– интерферон-γ — вырабатывается Т-лимфоцитами (хелперами), естественными киллерами и макрофагами. Предназначен для обезвреживания любых антигенов и митогенов; обладает выраженными антипролиферативными, а также иммуномодулирующими эффектами (стимулируют активность макрофагов, естественных киллеров, Т-киллеров и В-лимфоцитов).
Интерфероны образуются в местах и во время репродукции вируса, поэтому вступают в борьбу с инфекцией на самых ранних стадиях заболевания. Интерфероны не взаимодействуют с вирусом и не мешают его адсорбции на клетке, но активно подавляют репродукцию вируса, проникшего в клетку. Для этого интерфероны инициируют ферментативные реакции, одна из которых приводит к блокаде синтеза вирусных белков на стадиях их транскрипции и трансляции, а другая — к активации внутриклеточного разрушения вирусных нуклеиновых кислот, в том числе и РНК. Таким образом, интерфероны подавляют сборку белков, входящих в состав генома, капсида и оболочки вирусов.
Естественным интерферонам сопутствуют другие многочисленные цитокины (интерлейкины, колониестимулирующиефакторы, факторы некроза опухолей и т. д.), расширяющие спектр их действия за пределы, доступные рекомбинантным, синтетическим интерферонам — продуктам генной инженерии. Интерфероны являются важнейшим фактором неспецифической резистентности, противовирусная эффективность которого сравнима с совокупной эффективностью всех других факторов иммунитета.
Лизоцим — фермент, который вырабатывается нейтрофилами и запасается в их специфических гранулах. Защитные эффекты лизоцима особенно значительны на слизистых оболочках, так как он обладает прямым бактерицидным и (в меньшей степени) вируцидным действием. Кроме того, лизоцим стимулирует лизис клеток макрофагами и нейтрофилами, активизирует синтез антител. Лизоцим высвобождается из нейтрофилов почти мгновенно — уже через 60 с после активации иммунной системы.
Естественные антитела — иммуноглобулины М, обладающие поливалентной специфичностью; слущиваются с поверхности зрелых покоящихся В-лимфоцитов.
Белки системы комплемента способны нейтрализовать некоторые вирусы, но их главной функцией является посредничество: а) в неспецифическом фагоцитозе; б) в специфических цитотоксических процедурах, обусловленных функцией противовирусных антител; в) в развитии экссудативной фазы воспаления.
· Неспецифический клеточный иммунитет.
Естественные киллеры (ЕК) — тип лимфоцитов, не имеющих специфических рецепторов к конкретным вирусам, но способных опознавать «неправильные» клетки (инфицированные, ксеногенные, опухолевые) без предварительной сенсибилизации и убивать их.
Активные ЕК-клетки появляются через 2-е суток после заражения вирусом, т. е. прежде, чем появляются специфические Т-киллеры. Помимо того, что ЕК-клетки проявляют прямую (неспецифичную) цитотокисчность, они участвуют в реакциях цитотолиза, опосредованного антителами. Активность ЕК регулируется интерферонами-γ и интерлейкинами.
Цитотоксичность ЕК реализуется следующим образом:
1) медиаторы, произведенные ЕК, повышают проницаемость мембраны клетки-мишени через изменение активности клеточных ферментов и путем прожигания пор в мембране метаболитами кислорода;
2) цитотоксичные вещества, синтезированные ЕК, вводятся в цитоплазму клетки-мишени и дезорганизуют ее.
Макрофаги выполняютдве основные функции: эффекторную (фагоцитоз свободных вирусов и зараженных ими клеток) и регуляторную (презентация вирусных антигенов Т-лимфоцитам, активация Т- и В-лимфоцитов).
Процесс презентации антигенов клеткам, обеспечивающим специфический иммунитет, проходит в несколько стадий:
· макрофаги осуществляют эндоцитоз (фаго- или пиноцитоз) вирусов;
· производят ферментативную переработку вирусных антигенов до уровня пептидов;
· выводят вирусные пептиды на свою поверхность;
· представляют их распознавания Т-лимфоцитам (весь процесс занимает около получаса).
Таким образом, с началом репродукции вируса происходит быстрая инфильтрация зоны зараженного эпителия факторами естественного иммунитета для ограничения инфекции путем подавления репликации вируса в клетках и/или разрушения инфицированных клеток.
Адаптивный (специфический) противовирусный иммунитет
Репродукция вируса в эпителии вызывает развитие антиген-специфи-ческого иммунного ответа, связанного с деятельностью лимфоцитов. Различают клеточный и гуморальный приобретенный противовирусный иммунитет.
· Т-клеточный иммунитет.
Лимфоциты CD 4+ (син. регуляторы, хелперы)выполняют организационные функции: распознают антигены вирусов, представленныемакрофагами, и передают информацию клеткам-эффекторам. Кроме того, Т-хелперы первого типа синтезируют интерлейкин-2, необходимый для пролиферации Т-клеток, и интерферон-γ, стимулирующий цитотоксичные Т-лимфоциты. Т-хелперы второго типа (син. супрессоры) регулируют интенсивность инфильтрации пораженных тканей клетками Т-системы.
Цитотоксические Т-лимфоциты
CD
8+
(син.
эффекторы или Т-киллеры) созревают в
8-09-2015, 19:55
