Боль формируется как ответная реакция организма на разрушающие его раздражители. Данная реакция, по-видимому, выработалась в процессе эволюции живых существ как приспособительное свойство, направленное на улучшение выживаемости во внешней среде, так как при помощи болевого ощущения определялись те раздражители, которые непосредственно угрожают его жизнедеятельности или даже жизнеспособности. Если бы организм не обладал чувством боли, как это наблюдается в отдельных случаях у людей ("врожденная анальгия"), то своевременно определить вредоносность воздействия было бы невозможно, и смерть организма в таких условиях была бы более вероятной.
Можно предполагать, что боль является отрицательной биологической потребностью, формирующей перцептуально-мотивационный компонент той функциональной системы, которая контролирует два важнейших полезных приспособительных результата, две жизненно важные константы организма:
1. целостность его покровных оболочек, обеспечивающих изолированность от внешнего мира и тем самым постоянство внутренней среды организма,
2. уровень кислородного дыхания тканей, поддерживающий их нормальную жизнедеятельность.
Различают два основных вида боли – физическую и психогенную. В зависимости от причин физическую боль делят на три категории:
![]() Боль, обусловленная внешними воздействиями (за исключением боли от чрезмерных адекватных влияний на органы чувств, например, зрение, слух). Такая боль имеет следующие особенности: она всегда возникает на коже, непродолжительна, за исключением тех случаев, когда нарушается целостность кожи. Определить локализацию такой боли и установить причину ее возникновения легко. Возможно устранение внешнего воздействия. Нервная система остается неповрежденной , сохраняются целостность ее периферического аппарата и функций центральных механизмов, модулирующих болевое ощущение. В эту категорию входит большинство видов экспериментально вызванной боли. Боль, возникающая в результате внешних воздействий, может быть условным элементом в механизме обучения организма предупреждению повреждений. Эта категория включает боль, наблюдающуюся при клиническом сенсорном исследовании, которое определяет сохранность функций органов и тканей.
Боль, обусловленная внешними воздействиями (за исключением боли от чрезмерных адекватных влияний на органы чувств, например, зрение, слух). Такая боль имеет следующие особенности: она всегда возникает на коже, непродолжительна, за исключением тех случаев, когда нарушается целостность кожи. Определить локализацию такой боли и установить причину ее возникновения легко. Возможно устранение внешнего воздействия. Нервная система остается неповрежденной , сохраняются целостность ее периферического аппарата и функций центральных механизмов, модулирующих болевое ощущение. В эту категорию входит большинство видов экспериментально вызванной боли. Боль, возникающая в результате внешних воздействий, может быть условным элементом в механизме обучения организма предупреждению повреждений. Эта категория включает боль, наблюдающуюся при клиническом сенсорном исследовании, которое определяет сохранность функций органов и тканей.
![]() Боль, обусловленная внутренними процессами. При боли этой категории возбуждаются любые типы рецепторов и механизмы их активации могут быть различными. Возникающий при этом афферентный поток воспринимается как боль. В появлении такой боли кожа обычно не участвует, за исключением случаев ее прямого повреждения или отраженной боли. Локализация боли, идентификация ее причины пациентом, частичное или полное устранение источника боли нередко невозможны. Она имеет значительно большую длительность. При этой категории боли нервная система остается неповрежденной, так как фокус патологического процесса расположен дистальнее рецепторов. Кроме того, сохраняются нормальное поведение по афферентным волокнам и функции механизмов, модулирующих боль. По типу вовлекаемой ткани боль этой категории делят на эктодермальную, мезодермальную и эндодермальную, а также боль от чрезмерной нагрузки мышц.
Боль, обусловленная внутренними процессами. При боли этой категории возбуждаются любые типы рецепторов и механизмы их активации могут быть различными. Возникающий при этом афферентный поток воспринимается как боль. В появлении такой боли кожа обычно не участвует, за исключением случаев ее прямого повреждения или отраженной боли. Локализация боли, идентификация ее причины пациентом, частичное или полное устранение источника боли нередко невозможны. Она имеет значительно большую длительность. При этой категории боли нервная система остается неповрежденной, так как фокус патологического процесса расположен дистальнее рецепторов. Кроме того, сохраняются нормальное поведение по афферентным волокнам и функции механизмов, модулирующих боль. По типу вовлекаемой ткани боль этой категории делят на эктодермальную, мезодермальную и эндодермальную, а также боль от чрезмерной нагрузки мышц.
![]() Боль, связанная с повреждением нервной системы, в особенности ее афферентного аппарата. Хотя такая боль часто сопровождается ощущениями на коже, правильно идентифицировать внешние причины бывает затруднительно или невозможно. Также трудно определить локализацию источника боли. Боль этой категории продолжительная, может длиться годами и устранение ее источника невозможно. Нервная система повреждена: отмечаются дефекты проводящих периферических или центральных путей, а также нарушения функций механизмов, модулирующих боль. При боли этой категории повреждения лежат проксимальнее рецепторов в периферических нервах, спинном мозге или высших центрах мозга. Они могут быть локальными или системными (невралгии, каузалгии, фантомная боль, таламический синдром).
Боль, связанная с повреждением нервной системы, в особенности ее афферентного аппарата. Хотя такая боль часто сопровождается ощущениями на коже, правильно идентифицировать внешние причины бывает затруднительно или невозможно. Также трудно определить локализацию источника боли. Боль этой категории продолжительная, может длиться годами и устранение ее источника невозможно. Нервная система повреждена: отмечаются дефекты проводящих периферических или центральных путей, а также нарушения функций механизмов, модулирующих боль. При боли этой категории повреждения лежат проксимальнее рецепторов в периферических нервах, спинном мозге или высших центрах мозга. Они могут быть локальными или системными (невралгии, каузалгии, фантомная боль, таламический синдром).
В физической боли также различают:
- Первичную боль (быструю, колющую острую),например, вызванную уколом иглы в кожу; она точно локализована, быстро исчезает после удаления стимула, не вызывает эмоциональной реакции;
- Вторичную боль (медленную, невыносимую, жгучую), она появляется через 0,5 – 1 с после ощущения первичной боли, не имеет четкой локализации, остается некоторое время после удаления стимула, сопровождается изменениями функций сердечно-сосудистой и дыхательной систем, может влиять на характер личности, ее образ мышления (к вторичной боли относят также тупую боль в висцеральных органах и глубоких соматических структурах);
- Хроническую боль (физическая боль, продолжающаяся длительное время у некоторых больных хроническими заболеваниями), для нее характерны сложные нервные механизмы эмоционального, аффективного и поведенческого уровня, выражающиеся в реактивной депрессии, которая делает человека недееспособным и в корне меняет его жизнь.
Психогенная боль связана с психологическими или социальными факторами, такими как эмоциональное состояние личности, окружающая ситуация, традиция культуры. Она имеет неопределенное начало, возникает без очевидной причины. Природа психогенной боли может быть неясна во многих отношениях. Часто отмечается расхождение между остротой боли, описываемой пациентом, и его поведением. Боль может не наблюдаться в ночные часы. Характерно плохо определяемое и изменяемое место боли, не всегда совпадающее с дерматомами или местом отраженной боли. Кроме того, психогенная боль несвязанна с внешними стимулами, может изменяться в зависимости от настроения. Она снимается действием антидепрессивных препаратов и других методов, уменьшающих эмоциональное напряжение.
Периферические системы боли
Рецепторы боли. По классификации A. Iggo (1977), рецепторы кожи делятся на механорецепторы, механоноцицепторные и ноцицепторы. Считается, что ноцицепторы представляют собой свободные нервные окончания немиелизированных волокон, образующие плексиморфные сплетения в тканях кожи, мышц и некоторых органов. Обнаружены и тонкие нервные волокна, связывающие их с рецепторами прикосновения, давления и температуры (волокна Тимофеева), что может служить основой возбуждения ноцицепторов при сильных сенсорных возбуждениях.
Если рассматривать ноцицепторы по механизму их возбуждения, то можно выделить два типа. Первый тип ноцицепторов – это механоцицепторов, так как их деполяризация происходит в результате механического смещения мембраны, что позволяет ионам натрия проникать внутрь клетки. Хотя они способны реагировать на введение ацетилхолина, которое блокируется холинолитиками, но при этом чувствительность рецептора к механическим раздражениям не снижается.
К механоцицепторам кожи относятся:
· Ноцицепторы кожи с афферентами А۵ -волокон, возбуждающиеся механическими стимулами, почти не реагирующие на термические и совсем не реагирующие на химические раздражения. Рецептивные поля их узкие, повторные раздражения их инактивируют и у них быстро развивается адаптация (что характерно для первой эпикритической боли).
· Ноцицепторы эпидермиса с афферентами С-волокон, которые возбуждаются механическими стимулами, на нагревание или охлаждение не реагируют, имеют узкие рецептивные поля, легко адаптируются.
· Ноцицепторы мышц с афферентами А۵ -волокон, расположенные на поверхности мышц и в местах перехода мышцы в сухожилие. Активируются особенно сильно при давлении тупыми предметами на укол иглой. Быстро адаптируются.
· Ноцицепторы суставов с афферентами А۵ -волокон, которые возбуждаются только при чрезмерном сгибании или выкручивании суставов.
· Тепловые ноцицепторы кожи с афферентами А۵ -волокон, которые возбуждаются на механические раздражения и нагревание 36-43°С и не реагируют на охлаждение.
Второй тип ноцицепторов – это хемоноцицепторы. Деполяризация их мембраны возникает при воздействии химических веществ (растворы хлористоводородной, серной и уксусной кислот, гистамин, ацетилхолин, окситриптамин, брадикинин и др.), т. е. тех веществ, которые в подавляющем большинстве нарушают окислительные процессы в тканях. Характерно, что после действия повреждающих раздражителей их чувствительность значительно повышается, и они приобретают способность реагировать на ранее не повреждающие механические и термические стимулы. Данный тип ноцицепторов локализуется как на покровных оболочках организма, так и в глубоких тканях, в том числе в висцеральных органах и особенно их много в оболочках кровеносных сосудов.
К хемоноцицепторам Л.Н. Смолин (1975) относит следующие:
· Подкожные ноцицепторы с афферентами С-волокон, активирующиеся механическими стимулами при сильном давлении на кожу и подкожном введении химических веществ.
· Ноцицепторы кожи с афферентами С-волокон, активирующиеся механическими стимулами и сильным нагреванием. Характерно, что при воздействии на кожу обезьян термального раздражителя от 36 до 43°С реагируют рецепторы с афферентами А۵ -волокон, а от 41 до 53°С – ноцицепторы с афферентами С-волокон. Данные ноцицепторы медленно адаптируются.
· Ноцицепторы кожи с афферентами С-волокон, возбуждающиеся механическими стимулами и охлаждением до 15°С.
· Ноцицепторы мышц с афферентами С-волокон, активирующиеся на механические, термические и химические раздражители, в том числе на брадикинин и гистамин.
· Ноцицепторы внутренних паренхиматозных органов, локализующиеся, вероятно, главным образом в стенках артериол.
Таким образом, большинство механоцицепторов имеют афференты А۵ -волокон, и они расположены так, что обеспечивают контроль целостности кожных покровов организма, суставных сумок, поверхности мышц.
Хемоноцицепторы расположены в более глубоких слоях кожи и передают импульсацию преимущественно через афференты С-волокон. Особенности локализации хемоноцицепторов наводят на мысль, что они контролирую дыхательные функции тканей, в том числе и покровных оболочек. По мнению P.W. Nathan (1976), болевые рецепторы делятся на реагирующие на само повреждение и на те, которые реагируют на результат этого разрушения.
Адекватные стимулы для боли. Пока не имеется определенного мнения о том, существуют ли адекватные стимулы для рецепторов боли. Высказан ряд гипотез, из которых наиболее распространена следующая: свободные нервные окончания в коже содержат одно или несколько химических соединений в пузырьках или гранулах. Эти соединения являются специфическими и выделяются в ответ на особую стимуляцию. Агент, высвобождающийся из нервных окончаний, взаимодействует с рецепторами наружной поверхности мембраны окончаний и вызывает ее деполяризацию. Действие соединения на рецепторы прекращается соответствующим ферментом, окружающим нервные терминали (см. рис. 1).

Рис. 1 Предполагаемая модель действия синаптического передатчика на свободное нервное окончание.
1 – рецепторная субстанция, 2 – разрушающий фермент, 3 – свободное нервное окончание.
В качестве активаторов рецепторов предположены ионы калия, гистамин, брадикинин, соматостатин, субстанция Р, простагландины. Однако ни одно из данных веществ еще не обнаружено в свободных нервных окончаниях. В вариантах этой гипотезы в качестве активаторов рецепторов свободных нервных окончаний предлагают рассматривать вещества протоплазмы клеток, разрушающихся при механических или термических воздействиях на ткань, а также продукты, образующиеся при воспалительном процессе. Полагают, что рецепторы терминалей активируются при локальной гипоксии участков тканей в ответ на механическое сдавливание капилляров вокруг свободных нервных окончаний. Высказана гипотеза о том, что изменение концентрации водородных ионов, приводящее к ацидозу в межклеточном пространстве, может обусловливать возбуждение рецепторов протонов, обнаруженных в мембране сенсорных нейронов ганглия тройничного нерва. Согласно другим предположениям, адекватным стимулом для рецепторов боли является сильная механическая деформация свободных нервных окончаний, вызванная сжатием ткани или перемещением жидкости в канальцах дентина зубов.
Предполагаемые рецепторные субстанции и синаптические передатчики. С помощью иммуногистохимического метода показано, что субстанция Р (пептид, обнаруженный во многих областях центральной нервной системы) распределяется вокруг терминалей чувствительных нервов. В непосрне5дственой близости от терминалей наблюдаются деградирующие ферменты – ацетилхолинэстераза (вокруг соматических окончаний) и бутирилхолинэстераза (вокруг висцеральных рецепторов).
Существует гипотеза о том, что каждый функциональный тип чувствительных нейронов спинномозговых узлов вырабатывает свою собственную специфическую рецепторную субстанцию и транспортирует ее аксоплазматическим током из тела клетки к периферическим окончаниям и, вероятно, к центральным окончаниям, где эта субстанция служит синаптическим передатчиком первичного афферентного волокна, т. е. рецепторная субстанция и синаптический передатчик сенсорного нейрона являются одним и тем же химическим веществом.
Одним из предполагаемых синаптических передатчиков ноцицептивных нейронов в заднем роге спинного мозга – субстанция Р, которую содержат 10-20% сенсорных нейронов спинномозговых узлов. Иммуногистохимические методы показали, что этот пептид локализуется в маргинальном и желатинозном слоях заднего рога, там, где оканчиваются волокна болевой чувствительности. Все нейроны в этих областях, которые активировались при стимуляции А-۵ - и С-волокон, эффективно активировались также субстанцией Р.
Другим вероятным передатчиком сенсорных нейронов спинномозговых узлов считают пептид соматостатин, обнаруженный примерно в 10% этих нейронов. Установлено, что нейроны, содержащие субстанцию Р и соматостатин, относятся к популяции малых нейронов спинномозговых узлов, имеющих безмиелиновые аксоны.
По-видимому, периферические или центральные нейроны можно рассматривать как элементы системы боли, если эти нейроны отвечают исключительно на болевые стимулы, имеют анатомические связи с нейронами, образующими системы боли, если стимуляция этих нейронов вызывает ощущении боли и их ответы на болевой стимул уменьшаются одновременно со снижением ощущения боли.
Сенситизация. Общепризнано, что большинство типов сенсорных рецепторов становятся менее чувствительными, если подвергаются длительной стимуляции. В отличие от них у ноцицепторов чувствительность прогрессивно возрастает (до определенных пределов), если действие сохраняется продолжительное время. Такое снижение пороговой чувствительности называется сенситизацией. Это явление обнаружено также в процессе регенерации поврежденного нервного ствола, когда разрастающаяся соединительная ткань вызывает сжатие регенерирующих тонких нервных волокон. При этом в нерве регистрируется необычайно высокая фоновая ритмика и низкий порог для активации волокон в области повреждения. Согласно одной из гипотез о происхождении этого феномена, повреждение тканей вызывает высвобождение рецепторной субстанции, сопровождающееся инактивацией разрушающего ее фермента и стойкой деполяризацией мембраны рецептора, что обусловливает устойчивые разряды в афферентном волокне. Сенситизация проявляется в способности ноцицептора отвечать на адекватные стимулы допороговой величины (например, активироваться при температуре 40 °С, а не 45 °С, как отмечалось ранее), а также в способности возбуждаться ноцицептивными стимулами прежде неэффективных модальностей. Явление сенситизации многие исследователи рассматривают как одну из причин кожной гиперальгезии.
Центральные системы боли
Цитоархитектоника задних рогов спинного мозга. В дорсальных рогах спинного мозга находятся центральные нейроны, воспринимающие и перерабатывающие болевые сигналы перед отправкой их в головной мозг. Задний рог принято делить на 5 – 6 пластин. Первая пластина – краевая зона, содержит маргинальные нейроны, которые являются ноцицептивными интернейронами спиноталамического пути. Вторая – третья пластины образуют тесное сплетение мелких нейронов – желатинозную субстанцию, содержащую в себе малые тормозящие интернейроны, создающие сложные замкнутые цепочки, и крупные нейроны, аксоны которых идут в спиноталамический путь. Важной структурой желатинозной субстанции являются гломерулы – сложные синапсы между терминалями первичных афферентных волокон, дендритами центральных нейронов и окончаниями нисходящих путей. Эти структуры, как полагают, обеспечивают взаимодействие между афферентными и центральными потоками импульсов в процессе переработки информации. Четвертая и пятая пластины, или собственное ядро, - зона скопления самых крупных нейронов заднего рога, дендриты которых проникают в желатинозную субстанцию, а аксоны многих из них формируют спиноталамический путь. Нейроны собственного ядра легко активируются болевыми и неболевыми стимулами. Более глубокие пластины серого вещества (седьмая – восьмая), не относящиеся к заднему рогу, дают начало спиноретикулярным волокнам.
Центральные проекции первичных афферентных волокон. Перед входом в спинной мозг толстые и тонкие волокна дорсальных корешков перераспределяются. При этом тонкие миелиновые и немиелиновые волокна, несущие информацию о боли, группируются в отдельные пучки, которые входят в спинной мозг и образуют зону Лиссауэра. Пройдя в ней вдоль спинного мозга 1 – 2 сегмента, терминали волокон проникают в первую пластину серого вещества задних рогов. Толстые миелиновые волокна, войдя в спинной мозг, образуют петлю, входят в серое вещество с внутренней стороны задних рогов через пятую пластину и лишь затем достигают желатинозной субстанции (вторая – третья пластины).
Тонкие первичные афферентные волокна оканчиваются в первой половине – маргинальной зоне, а большинство толстых афферентных волокон – во второй пластине желатинозной субстанции. Перед окончанием толстые афферентные волокна проходят вдоль внутренней поверхности задних рогов, входят в серое вещество через четвертую – пятую пластины и затем поднимаются во вторую пластину. Здесь они оканчиваются факелоподобными пучками, но не проникают в маргинальный слой. Факелоподобные пучки окончаний толстых афферентных волокон делят желатинозную субстанцию на дольки, в которых нейроны организованы в вертикальные столбы. Крупные нейроны четвертой пластины посылают свои дендриты в эти дольки, где и устанавливаются синаптические контакты с толстыми первичными афферентными волокнами.
Считается доказанным, что нейроны второй – третьей пластин (область желатинозной субстанции) во взаимодействии с маргинальными нейронами образуют специализированную систему модулирующего контроля болевого афферентного входа, а пятая пластина является уровнем полимодального ноцицептивного входа и областью взаимодействия с толстыми неболевыми афферентами (см. рис. 2).
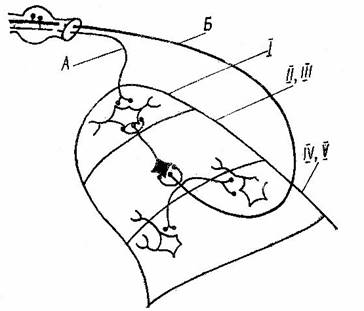
Рис. 2 Схема некоторых связей толстых и тонких первичных афферентов нейронами заднего рога.
А – тонкие, Б – толстые афференты, Й – маргинальный слой, ЙЙ и ЙЙЙ – желатинозная субстанция, ЙV и V – собственное ядро.
Тонкие афферентные волокна от кожи, мышц, сухожилий и внутренних органов (группы А-۵ -, С, ЙЙ, ЙЙЙ, ЙV) через интернейроны заднего рога замыкается на мотонейронах сгибательных мышц и образуют обширную группу сегментарных сгибательных рефлексов, которые играют важную роль в ноцицептивных механизмах, создавая защитные рефлекторные реакции.
Функциональная организация нейронных цепей в заднем роге. В настоящее время предложены две основные схемы взаимодействия афферентных сигналов в заднем роге. Вопрос о входе к маргинальным нейронам пока не решен. Зона Лиссауэра содержит не только первичные афферентные волокна, но и аксоны нейронов желатинозной субстанции. После перерезки этой зоны аксосоматические и аксодендритные синапсы на маргинальных нейронах дегенерируют, что указывает на то, что С-волокна и аксоны нейронов желатинозной субстанции должны оканчиваться на них. Как уже упоминалось, С-волокна оканчиваются в маргинальной зоне и желатинозной субстанции. В свою очередь, нейроны желатинозной субстанции образуют тормозящие синапсы на соме маргинальных нейронов.
Толстые афферентные волокна заканчиваются возбуждающими синапсами на нейронах желатинозной субстанции и больших нейронах собственного ядра. Полагают, что ритмическая активность нейронов желатинозной субстанции импульсами от толстых афферентных волокон может выражаться в интенсивном торможении маргинальных нейронов, на которых образуют свои синапсы тонкие волокна. Такая нейронная цепь может создать механизм, посредством которого толстые неболевые афферентные волокна моделируют порог боли. На рисунке показана принципиальная схема возможной организации такой системы контроля.

Рис.3 Схема контроля интенсивности сенсорного потока в заднем роге серого вещества спинного мозга.
А – тонкие, Б – толстые афференты, ЖС – желатинозная субстанция, Т – нейроны, передающие сенсорную информацию в мозге, (+) – возбуждение, (-) – торможение.
Толстые неболевые
8-09-2015, 21:54
