Введение о диабете
Греческим словом диабет называют болезни, сопровождающиеся выделением больших количеств мочи.
Сахарный диабет характеризуется повышенным содержанием сахара (глюкозы) в крови и часто сопровождается выделениями глюкозы почками с мочой.
Развитие медицины показало, что сахарный диабет может существовать и без появления глюкозы в моче, концентрация глюкозы в крови может быть повышенной, но не достигающего почечного "порога".
Отличительным симптомом сахарного диабета и его самой главной характеристикой является постоянная гипергликоэмия.
Когда количество глюкозы после еды увеличивается, в поджелудочной железе происходит выделение инсулина. Инсулин способен снижать уровень глюкозы в крови путём усиления его использования клетками.
У людей с диабетом уровень сахара в крови остаётся повышенным. Это связано с недостаточной продукцией инсулина поджелудочной железой, а значит неэффективностью этого количества инсулина.
Различают 2 формы диабета: сахарный диабет 1 типа (5%) и сахарного диабета 2 типа (95%).
В основе 1 типа диабета лежит аутоиммунное заболевание, в результате которого иммунная система организма атакует клетки поджелудочной железы, которые становятся неспособными производить инсулин.
При 2 тапе диабета поджелудочная железа совершенно здорова и постоянно выделяет в кровь такое количество инсулина, которое точно соответствует концентрации в крови глюкозы. Уровень глюкозы в данном варианте повышен из-за неспособности клеток поглощать глюкозу, из-за нарушения восприятия сигнала инсулина рецепторами, расположенными на поверхности клеток.
У страдающих диабетом 1 типа вследствие аутоиммунной агрессии разрушаются бетта-клетки, продуцирующие инсулин, из-за чего развивается его дефицит.
Большинство больных 2-м типом сахарного диабета страдают ожирением.
Сравнение 1 и 2 типов диабета.
2 тип диабета встречается у людей с повышенным весом, страдающих ожирением. Причины, которые приводят к повышению уровня глюкозы, индивидуальны. Резистентность организма к инсулину (т. е. Снижение чувствительности клеток к инсулину) – это важный фактор, независящий от секреции инсулина. Второй фактор – это понижение производства инсулина бета-клетками поджелудочной железы, т. е. 2 типа диабета может иметь сочетания комбинаций дефицита секреции и дефицита действия инсулина.
История диабета
Симптомы диабета: экстремальная жажда, частое мочеиспускание были известны врачам в течении тысячелетий. Всё это время они мало что знали о причинах этого смертельного заболевания, пока в 1922 г. первый пациент успешно не вылечился инсулином.
Древние индусы описывали как чёрные муравьи и мухи атакуют мочу диабетиков. Индийские врачи из Сумруты в 400 г. до н.э. описали сладкий вкус мочи, это был ключ к диагнозу. Около 250г. до н.э. появилось название "диабет", это слово с греческого означает "сифон" и характеризует, как эта болезнь быстро лишает человека жидкости. До середины 1800 года предлагалось огромное количество лечений диабета. Предлагались "невероятные диеты", опиум (т.к. вылечивал другие заболевания). Успешным было лечение голодной диетой, которая строго ограничивает накопление калорий.
К решению загадки диабета пришли в 1889 г. в Германии. Врачи Джозеф фон Меринг и Оскар Минковский хирургически удалили поджелудочную железу собаки. У собаки немедленно развился диабет. Так была установлена связь между поджелудочной железой и диабетом, исследование показало, что удаление поджелудочной приводит к диабету.
Молодой парень, Леонард Томпсон, первый пациент, которого лечили инсулином. 11января 1922 г. он был старше 14 лет и весил 64 пуда, первая инъекция инсулина привела к снижению уровня сахара в крови. Удаление все еще не было достаточно злокачественным, а абсцессы развивались на участке инъекции. Несколько недель спустя Леонард лечился опять и пошёл на поправку. Уровень сахара в его крови снизился, он набрал вес и жил ещё 13 лет. Умер от пневмонии в возрасте 27 лет.
В 1923 г. Бантинг и Маклоед получили Нобелевскую премию за открытие инсулина. Бантинг разделил эту премию с Бестом, и Маклоед разделил с Коллипом. Свою Нобелевскую лекцию Бантинг закончил, говоря об открытии:"Инсулин не избавление от диабета, это его лечение. Оно даёт диабетикам достаточное количество углеводов, таким образом, белки и жиры могут быть включены в диету в достаточном количестве, чтобы обеспечить энергией необходимой для жизнедеятельности.
Эпидемиология
Свыше 18 миллионов американцев больны диабетом. Из них около 5 миллионов не знают о своей болезни.
1 группой диабета страдают 5-10% больных, эта группа поражает одного из 400 детей и подростков.
2 группа более распространённая. Поражает 90-95% всех больных диабетом. Эта форма диабета может не распознаваться многие годы. По последним данным о заболевании диабетом число больных с этим диагнозом быстро увеличивается.
2 группа эпидемического диабета.
Когда люди думают об эпидемиях, они думают об инфекционных болезнях, таких, как грипп. Однако преобладающая 2 группа диабета имеет теперь эпидемическое значение. В США на заботу о здоровье диабетиков выделено свыше 130 биллионов (10.9) долларов. Штаты на пятом месте по смертности. Число больных с таким диагнозом продолжает расти. Вычислено, что каждый третий из детей, рождённых в 2000году, в своей взрослой жизни будут страдать диабетом. По прогнозам, диабет станет одним из наиболее общих заболеваний в мире за пору десятилетий, поразит меньше половины биллиона человек.
Если раньше 2 группа среди юных встречалась редко, следовательно, первоначально называлась "взрослый диабет", то теперь случаи болезни 2 группой диабета увеличиваются у молодёжи старше 20 лет и у детей. У этого молодого поколения диабетиков в течении многих десятилетий будет ухудшаться состояние здоровья. В 1990г. у 4,9% американского населения был поставлен диагноз - диабет.
Ожирение
За диабетом широкое распространение получило ожирение. На сегодняшний день людям трудно удерживать здоровый вес. Мы не испытываем недостатка в пище и ведём малоподвижный образ жизни. В результате, у многих из нас вес больше, чем он должен быть.
Но ещё только пару столетий назад люди были более активны, и запасы еды были недостаточны.
Физиология и биохимия регуляции сахара. Обзор метаболизма глюкозы
Глюкоза - существенное топливо для организма.
Количество глюкозы в кровотоке регулируется многими гормонами, наиболее важным из которых является инсулин. Инсулин - это "гормон достатка", который выбрасывается при избытке глюкозы. Инсулин стимулирует:
- поглощение мышцами и жировыми клетками глюкозы из крови.
- потребление клетками глюкозы, которая дает им энергию в форме АТФ.
- запасание глюкозы печенью и мышцами в виде гликогена (краткосрочный запас энергии).
- запасание глюкозы в виде жира адипоцитами (долговременный запас энергии)
- использование клетками глюкозы для синтеза белков для многих целей в организме.
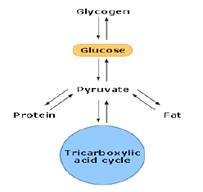
Схема 1: Метаболизм глюкозы.
Она может быть использована как энергия пирувата и лимонной кислоты, а также может быть переработана в жир (долговременное хранение) и гликоген (краткосрочное хранение). Тот час из пирувата может быть синтезирована какая-нибудь аминокислота, таким образом, глюкоза косвенно может способствовать синтезу белка.
Глюкагон - это главный гормон, противоположный действию инсулина и выделяемый при недостатке пищи. Инсулин способствует формированию гликогена (энергозависимый процесс или анаболический эффект). Глюкагон приводит к расщеплению гликогена, при этом выделяется энергия (катаболический эффект). Глюкагон также помогает организму стимулировать использование других ресурсов глюкозы, таких как жиры и белки.
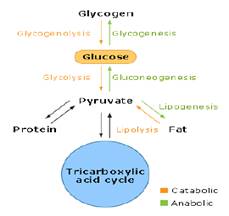
Схема 2: Анаболизм и катаболизм глюкозы
Метаболизм глюкозы включает в себя 2 процесса: энерго-продуцирующий (катаболизм) и энерго-потребляемый (анаболизм) процессы.
Регуляция глюкозы в крови
Уровень глюкозы в крови не постоянный - увеличивается и уменьшается в зависимости от потребностей организма, регулируется гормонами. Нормальный уровень глюкозы в пределах от 70 до 100 мл/дл, 3,3 – 6,1 ммоль/л.
Три причины влияют на повышение уровня глюкозы: режим питания, расщепление гликогена, печёночный синтез глюкозы.
Приём пищи приводит к увеличению глюкозы в крови. Но время, за которое увеличивается уровень глюкозы, зависит от нескольких факторов:
- от количества и типа съеденных углеводов;
- от скорости пищеварения и скорости абсорбции;
Так как глюкоза полярная молекула, то для её абсорбции сквозь гидрофорбную стенку кишки требуется специальный переносчик глюкозы (GLUTS), которых существует 5 видов. В кишечнике преимущественно GLUT2 и GLUT5.
Печень - главный орган, в котором образовывается глюкоза: путем расщепления гликогена, образованием глюкозы из промежуточных углеводов, белков и метаболизма жира. Также печень важный орган по переработке глюкозы и может принимать различное количество глюкозы. Глюкоза попадает из пищеварительного тракта в воротную вену. Печень быстро удаляет излишнее количество глюкозы из кровотока. Так что даже после еды уровень глюкозы в крови не у диабетиков редко превышает 6,1 ммоль/л.
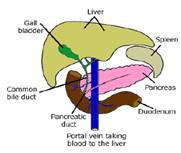
Схема 3: Воротное кровообращение
Воротная вена несёт в себе почти всю кровь от пищеварительного тракта и приносит её к печёнке. Кровообращение "обогащённой" крови между кишкой и печенью называется воротным кровообращением. Оно даёт возможность печени удалить вредные вещества из крови, прежде чем она поступит в систему кровообращения.
После еды - роль инсулина
После еды происходит увеличение глюкозы в крови. Это обнаруживают бета-клетки поджелудочной железы и выбрасывают в кровь инсулин. Инсулин даёт возможность использовать глюкозу тканями, в том числе скелетными мышцами и адипоцитами. При увеличении глюкозы уменьшается секреция глюкагона, выработка глюкозы из других источников и расщепление гликогена.
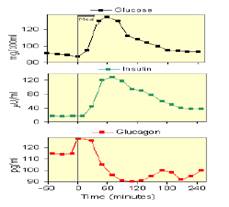
Схема 4. Изменение соотношения гормонов после еды.
Изменение в крови уровней глюкозы, инсулина и глюкагона после богатой углеводами еды.
Использование глюкозы
Внутри клетки некоторое количество глюкозы используется немедленно через гликолиз. Это основной путь метаболизма углеводов происходит во всех клетках организма. И весь сахар, превращённый в глюкозу, проходит этот путь.
В сытом состоянии высокий уровень инсулина и низкий уровень глюкагона стимулируют гликолиз, при котором освобождается энергия, и продуцируются промежуточные углеводы, которые могут использоваться в других метаболических путях.
Действие гликогена.
То количество глюкозы, которое не было немедленно использовано, забирается печенью и мышцами, где превращается в гликоген.
Инсулин:
- стимулирует образование печёночного гликогена (катализатор синтеза гликогена в печени)
- замедляет действие на печень фосфорилазы гликогена (фермент, катализирующий расщепление гликогена в печени).
- замедляет синтеза глюкозы другими источниками.
Инсулин также стимулирует образование гликогена в мышцах, но другим методом. Он заключается в увеличении числа переносчиков глюкозы (GLUT4) на поверхность клетки. ГЛЮТ 4 – главный переносчик глюкозы в клетки мышц и жировой ткани. Это ведёт к быстрому усвоению глюкозы и превращению её в мышечный гликоген.
Действие жиров
Когда запас гликогена полностью восстановится, излишек глюкозы превращается в жир, и этот процесс называется липогенез. Глюкоза превращается в жирные кислоты, которые хранятся в виде триалглицеридов (3 молекулы кислоты, присоединённые к 1 молекуле глицерина). Источником углерода для синтеза жирных кислот служит ацетил-Ко-А, образующийся при распаде глюкозы. Таким образом, избыток углеводов, поступающих в организм, трансформируется в жирные кислоты, а затем в жиры.
Инсулин способствует липогенезу:
- увеличивая число переносчиков глюкозы (GLUT4) на поверхности жировых клеток. Это является причиной быстрой утилизации глюкозы.
- увеличивая активность липопротеиновых липаз, которые освобождают много жирных кислот для синтеза триалглицеридов.
Вдобавок к содействию жировому синтезу инсулин замедляет разрушение жиров, подавляя гормоночувтствительную липазу (снижает запас жиров).
Результат - низкий уровень жирных кислот в крови.
Инсулин также имеет аноболический эффект, воздействующий на белковый метаболизм. Он стимулирует проникновение аминокислот в клетки и стимулирует образование белков из аминокислот.
Голодание - роль глюкагона.
Голоданием принято считать проведение более 8 часов без пищи. В результате наблюдается падение уровня сахара в крови, замедление секреции инсулина и усиление выделения глюкагона. Глюкагон противоположен действию инсулина. Глюкагон увеличивает уровень сахара стимулированием мобилизации запасов гликогена в печени. За 10–18 часов запасы гликогена истощаются, и если голодание продолжается, то глюкагон продолжает стимулировать продукцию глюкозы печенью.
Кроме низкого уровня глюкозы в крови, освобождение глюкагона стимулируют богатая белками пища и стресс:
- аминокислоты увеличивают секрецию глюкагона и незначительно инсулина. Глюкагон предотвращает гипогликэмию, вызванную инсулином и стрессом (организм предупреждает повышение уровня глюкозы, которая требуется во время стресса)
- при стрессе в кровь выбрасывается глюкагон, который увеличивает продукцию глюкозы печенью путем стимуляции распада глюкогена. Количество глюкозы в крови зависит от силы стресса.
Голод
Метаболическое состояние голода (т.е. тканевое голодание) более обыденно проявляется у людей, которые стараются стремительно потерять вес или у тех, которые чувствуют отвращение к пище. После пары дней без еды печень будет истощать запасы гликогена, но продолжать производить глюкозу из аминокислот и жиров.
Окисление жирных кислот как источников энергии увеличивается при голодании и физической работе. В этих состояниях их концентрация в крови увеличивается в результате мобилизации из жировых депо и они активно окисляются печенью, мышцами. При голодании часть жирных кислот используются многими тканями как источник энергии. Они в отличии от жирных кислот могут использоваться нервной тканью. Наиболее важный орган, использующий кетоновые продукты – это мозг, потому что он не способен к метаболизму жирных кислот.
"Голод посреди изобилия"
Диабет часто называют "голодом посреди изобилия", потому что внутриклеточный уровень глюкозы низкий, хотя внеклеточный уровень может быть экстремально высоким.
При диабете 1 типа в периферических тканях используются неглюкозные источники энергии, например, жировые кислоты и кетоновые тела. При тканевом голодании в крови можно обнаружить кетоновые тела. Кетоны - слабые кислоты, они закисляют кровь.
Это метаболическое состояние называется диабетическокетоацидоз (DKA). Гипергликимия и кетоацидоз являются признаком диабета 1 типа (схема 5).
![]() К кетоновым телам относятся бета-гидроксибутират, ацетоацетат и ацетон. Первые 2 молекулы могут окисляться в тканях, обеспечивая синтез АТФ. Ацетон образуется только при высоких концентрациях кетоновых тел в крови и выделяясь с мочой, выдыхаемым воздухом и потом позволяет организму избавляться от избытка кетоновых тел.
К кетоновым телам относятся бета-гидроксибутират, ацетоацетат и ацетон. Первые 2 молекулы могут окисляться в тканях, обеспечивая синтез АТФ. Ацетон образуется только при высоких концентрациях кетоновых тел в крови и выделяясь с мочой, выдыхаемым воздухом и потом позволяет организму избавляться от избытка кетоновых тел.
Влияние печени на уровень глюкозы
Печень получает богатую глюкозой кровь из пищеварительного тракта через воротную вену (схема3).
Печень имеет большое количество переносчиков GLUT2, которые не нуждаются в присутствии инсулина для транспорта глюкозы в клетки печени. GLUT2 имеет низкое родство к глюкозе, что дает возможность стремительному транспорту глюкозы, когда уровень сахара в крови будет выше нормы. Поэтому в печени уровень глюкозы внутри и снаружи клетки может приближаться к одинаковому.
Первый шаг к "запиранию" глюкозы внутри клетки заключается в фосфорилировании глюкозы - 6 - фосфат (G6Р). Печень отличается от остальных органов тем, что использует ферменты глюкокиназ, несколько хексокиназ. Глюкокиназа может производить G6P быстрее и также сковывать этим продуктом (это потому, что в печени G6Р может делать каналы в гликогене).
Глюкоза и инсулин оба моделируют метаболические энзимы в таких способах, как поддержание формирования гликогена. Этот процесс движения вперёд приносит больше глюкозы в печень. Инсулин поддерживает синтез гликогена, стимулируя гликоген синтетазу и сковывая гликоген фосфорилазу.
История инсулина. Синтез инсулина
Инсулин - вырабатывающие клетки тела называются в-клетками и они находятся в поджелудочной железе. Эти скопления клеток вместе образуют островки Лангерганса, названного в честь немецкого медицинского студента, который описал их.
Синтез инсулина начинается с транскрипции гена инсулина, который находится в 11 хромосоме. В результате трансляции мРНК образуется белок из 110 аминокислот. Этот первый трансляционный продукт назван препроинсулином, является неактивным. Он содержит сигнальный пептид, состоящий из 24 аминокислот, остатки которых требуются для перехода растущей полипептидной цепи через мембрану в эндоплазматический ретикулум. В эндоплазматическом ретикулуме от препроинсулина с помощью протеазы отщепляется сигнальный пептид и образуется проинсулин. Проинсулин состоит из 1 цепи, содержащей 3 домена В-цепи, содержащую аминогруппу – N-конец, А-цепи, содержащую карбоксильную группу – С-конец и соединяющий эти цепи С-пептид. Внутри эндоплазматического ретикулума специфические пептидазы удаляют С-пептид проинсулина, возникает созревшая активная форма инсулина.
В аппарате Гольджи инсулин и свободный С-пептид упаковываются в секреторные гранулы, которые накапливаются в цитоплазме В-клеток.
Экзоцитоз гранул осуществляется входом глюкозы в В-клетку.
Структура инсулина
В 1958 году Фредрик Санджер был награждён своей первой Нобелевской премией за установление последовательности АМК, составляющие инсулин. Впервые был определён в протеине порядок построения АМК (первостепенная последовательность).
Инсулин состоит из 2-х цепей АМК, названные цепью А (21АМК) и цепью В (30АМК), которые связаны вместе двумя дисульфидными мостиками. Молекула инсулина соединяет также внутримолекулярный дисульфидный мостик, соединяющий 6 и 11 остатков А-цепи вместе.
У многих видов животных состав А, В цепей молекулы имеют значительное сходство по первичной структуре с инсулином человека. По этой причине свиной инсулин может поддерживать обратный недостаток уровня человеческого инсулина у пациентов-диабетиков. Сегодня свиной инсулин большей частью замещен массовым производством человеческого инсулина бактериями (рекомбинантный инсулин).
Молекулы инсулина склонны образовывать димеры в р-ре и в присутствии ионов цинка инсулиновые димеры соединяются в гексомеры. В то время как мономеры инсулина легко диффундируют в крови и действуют стремительно, гексомеры распространяются медленно и поэтому их эффект наступает медленно.
Секреция инсулина
Увеличение уровня глюкозы внутри ![]() -клеток поджелудочной железы запускает выброс инсулина.
-клеток поджелудочной железы запускает выброс инсулина.
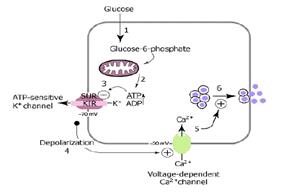
1) Глюкоза транспортируется в В-клетку двумя переносчиками глюкозы (GLUT2). Под действием глюкокиназы она фосфорилируется, образется глюкозо-6-фосфат. Этот этап очень быстрый и эффективно запирает глюкозу внутри клетки
2) Метаболизм глюкозы продолжается, АТФ вырабатывается в митохондриях.
3) Увеличение в АТФ чем АДФ закрывает АИФ-зависимые К-каналы в мембране В-клетки. Положительно заряженные ионы калия не выходят из В-клетки.
4) Повышение положительного заряда внутри В-клетки является причиной деполяризации.
5) Потенциалзависимые кальциевые каналы открываются, поток выделяющихся ионов кальция (Са 2+) поступает в клетку.
6) Увеличение концентрации кальция внутри клетки приводит к секреции инсулина путем экзоцитоза.
Имеются 2 фазы выхода инсулина в ответ на повышение глюкозы. Первая – немедленное освобождение инсулина, который хранится в секреторных гранулах. После небольшой задержки начинается вторая фаза, более длительная, чем первая, когда идет освобождение недавно синтезированного инсулина.
Освободившись, инсулин остается активным только короткое время, после этого распадается с помощью ферментов. Инсулиназа в
8-09-2015, 23:00
