«Длинный протокол»
Протокол называется «длинным», потому что, как правило, он начинается с 21–23-го (редко со 2–3-го) дня менструального цикла, предшествующего стимуляции. Чтобы заблокировать гипофиз, в начале лечения в течение 5 дней принимается только агонист. После достижения блокады гипофиза наступает менструация, и со 2–3 дня от ее начала проводится стимуляция препаратами, содержащими ФСГ, так же, как и в «чистой» схеме, но совместно с продолжающимся введением агониста.
«Оптимальный протокол»
При использовании нового антагониста Оргалутрана протокол стимуляции значительно укорачивается при сохранении выраженной и легко обратимой блокады гипофиза. Стимуляция начинается, как и в «чистой» схеме, со 2–3 дня менструального цикла путем ежедневного введения препарата, содержащего ФСГ. Затем с 5-го или 6-го дня стимуляции делаются ежедневные инъекции Оргалутрана на фоне продолжающейся стимуляции. Таким образом, «Оптимальный протокол» становится коротким, как в «чистой» схеме, и эффективным, как в «длинной» схеме. Комбинация препаратов нового покаления Пурегона и Оргалутрана (антагонист) - это:
- сокращение сроков лечения;
- лучшая переносимость инъекций;
- доказанная эффективность.
Благодаря этому совместное использование Пурегона и Оргалутрана можно назвать – « Два слагаемых надежды в лечении бесплодия».
На рисунке 1 представлена УЗ-картина стимулированного яичника с множеством фолликулов. Красными точками помечен максимальный фолликул диаметром 18 мм:
Сколько же фолликулов необходимо для того, чтобы возможно было провести ЭКО?
Минимальное количество фолликулов, необходимое для проведения ЭКО, зависит от нескольких факторов:
1. размеров фолликулов;
2. возраста женщины;
3.количества и результатов предыдущих попыток стимуляции овуляции;
Некоторые специалисты считают, что в процессе стимуляции необходимо получить как минимум 5 фолликулов размерами 14 мм. и более, однако противники этой теории утверждают, что возможно проведение процедуры уже при наличии хотя бы одного фолликула достаточного размера.
В большинстве клиник США придерживаются мнения о том, что необходимо как минимум 3-4 доминантных фолликула для того, чтобы процедура можно было считать успешной.
Индукцию овуляции проводить нельзя, если:
1. Нет уверенности в том, что маточные трубы проходимы;
2. Отсутствует возможность ультразвукового мониторинга роста фолликулов;
3. Если уровень ФСГ превышает 20 МЕ/л на фоне аменореи;
4. Длительность лечения бесплодия уже превышает 2 года.
Искусственная инсеминация (ИИ) - эта процедура, при которой в полость матки вводится специально обработанная сперма мужа или донора. Сочетание ИИ с индукцией овуляции значительно повышает эффективность лечения.
ИИ проводится в дни предполагаемой овуляции однократно/двукратно через 12 и 36 часов (по некоторым данным оптимально через 38-42 ч) после введения хорионического гонадотропина (этот препарат программирует овуляцию через 36-42 часа).
Недопустимо проведение ИИ в качестве замены ЭКО, если есть прямые показания для проведения программы ЭКО.
На рисунке 2 схематически изображено введение подготовленной спермы в полость матки.
От каких же факторов зависит эффективность внутриматочной инсеминации?
По данным литературы известно, что эффективность процедуры снижается при:
1. У женщин старше 38 лет;
2. У женщин со сниженным овариальным резервом;
3. При низком качестве спермы;
4. При наличии средней и тяжелой форм эндометриоза;
5. У женщин с выраженным спаечным процессом в малом тазу.
Какая же сперма может быть использована для внутриматочной инсеминации?
Для инсеминации должна использоваться сперма супруга или донора, содержащая более 10 млн. подвижных сперматозоидов в 1 мл. Другим критерием является наличие в материале, предназначенном для инсеминации не менее 4 млн. сперматозоидов нормальной морфологии.
Сколько попыток инсеминации можно провести?
Известно, что большинство беременностей, полученных в результате инсеминации, наступают в течение первых 3 циклов. После 3 попыток, шансы, а также эффективность данного метода снижается и является достоверно низкой при проведении 4-6 безуспешных манипуляций.
Таким образом, рекомендуется проведение инсеминации не более, чем в течение 4-6 циклов. В некоторых случаях, когда доказанным фактором бесплодия является отсутствие овуляции, возможно увеличение количества попыток до 9.
Какое количество внутриматочных инсеминаций необходимо проводить в течение одного цикла?
Этот вопрос до настоящего времени остается спорным. Некоторые исследования показали отсутствие достоверного повышения эффективности при проведении двух инсеминаций в соответствующие дни цикла по сравнению с одной. По некоторым данным, использование двукратной инсеминации достоверно увеличивает частоту наступления беременности.
По теории вероятности, использование двукратной инсеминации повышает шансы того, что сперма будет введена именно в нужный промежуток времени, тем более, что длительность жизни сперматозоидов в организме женщины составляет около 2-5 дней.
Забор созревших ооцитов (пункция яичников)
Пункция яичников проводится через задний свод влагалища под контролем УЗИ и кратковременным наркозом современными препаратами с минимальными побочными эффектами.
Женщина спит и ничего не чувствует. На рисунке 1 показана ультразвуковая картина забора фолликулярной жидкости специальной иглой для получения созревших ооцитов.
После того, как произведена пункция всех неоходимых фолликулов, за женщиной проводится наблюдение в течение часа, после чего ее отпускают домой. На рисунке 2 изображена яйцеклетка хорошего качества, полученная в результате пункции фолликулов у 25 летней женщины.
Для сравнения, на рисунке 3 Вы можете увидеть ооцит низкого качества, полученный при пункции фолликулов у 43-летней женщины. Отличия между этими ооцитами видно даже невооруженным взглядом.
Культивирование эмбрионов
В эмбриологической лаборатории производится оплодотворение сперматозоидами яйцеклетки. Этот этап занимает от 3 до 5 суток. На рисунке 4 изображена оплодотворенная яйцеклетка. В центре – 2 пронуклеуса – мужской и женский, а в правом верхнем углу – полярное тельце – признак того, что оплодотворение уже произошло.
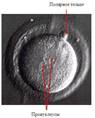
Рисунок 4. Оплодотворенная яйцеклетка.
Далее, начинается эмбриологический этап, во время которого эмбриолог наблюдает за делением клеток. На рисунке 5 изображены последовательные стадии развития эмбриона в пробирке.
Одним из важных этапов эмбриологической части процедуры является оценка «качества» полученных эмбрионов, которая проводится специалистом-эмбриологом на основании ряда признаков:
- количество клеток;
- одинаковость размера;
- степень фрагментации.
Эмбриолог обязательно отмечает наличие многоядерности, появление вакуолизации, гранулярности и т.п. Обычно, определение «качества» эмбриона возможно не ранее, чем через 48 часов после оплодотворения.
Через 2 суток, как правило, должен быть получен хотя бы один эмбрион, состоящий минимум из 3 клеток. По истечении 72 часов эмбрион должен состоять не менее, чем из 6 и более клеток.
Эмбрионы с большим количеством клеток правильной формы и одинакового размера, с отсутствием или небольшой фрагментацией имеют большее количество шансов для имплантации, чем эмбрионы, не отвечающие данным требованиям.
Для сравнения ниже изображены эмбрион «высокого» и «низкого» качества.
Оценка «качества» эмбриона при исследовании с помощью микроскопа дает нам некоторые основания для оценки предполагаемых шансов для имплантации данного эмбриона после его переноса. Однако, статистика показывает, что программа бывает неудачной при переносе 3 великолепно «выглядящих» эмбрионов, в то время, как при переносе эмбрионов «низкого качества» были рождены очень красивые дети.
К сожалению, истинный генетический потенциал, необходимый для дальнейшего развития, а также имплантации в полости матки оценить не представляется возможным. Многие эмбриологические лаборатории используют балльную шкалу оценки состояния эмбрионов, однако, единой схемы до сих пор не существует. Сейчас это направление интенсивно изучается эмбриологами всего мира.
Достаточно часто пациенты задают вопрос эмбриологу, опасаясь, что эмбрионы «низкого качества», которым все-таки удалось прикрепиться в матке и начать свое развитие, могут в итоге «превратиться» в детей «низкого качества». Опыт многих лабораторий мира показывает, что дети, рожденные после переноса таких эмбрионов, столь же сообразительны, умны и красивы, как дети, рожденные в результате переноса эмбрионов «высокого качества». Единственным моментом, заслуживающим внимания при переносе таких эмбрионов, является их более низкие шансы к внутриутробному развитию и рождению.
Перенос эмбрионов в полость матки
Этот этап является одним из важных моментов, поскольку эмбрионы хорошего качества, полученные в лаборатории, должны быть очень бережно и с минимальной травматизацией полости матки быть перенесены приблизительно в середину дна полости матки.
Для женщины эта процедура безболезненна и не требует дополнительного обезболивания. Специальный катетер с эмбрионом вводится через шейку матки в полость матки, что контролируется ультразвуком.
После того, как катетер достигает нужной точки, эмбрион переносится в полость матки, катетер удаляется и производится его проверка с использованием микроскопа (контроль полноценного введения нужных эмбрионов в полость матки). Если эмбрионы все-таки остались в катетере, то процедура немедленно повторяется с последующей повторной проверкой состояния этого катетера.
На рисунке 8 изображена ультразвуковая картина переноса эмбрионов: зеленым – движение катетера в полость матки через шейку матки:
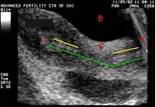
Рисунок 8. Ультразвуковая картина переноса эмбрионов*
В течение следующего часа женщина должна полежать, а дальше несколько ограничить физическую активность. Через 9-11 дней после переноса эмбриона рекомендуется проведение исследования содержания хорионического гонадотропина в крови женщины для установления факта наличия беременности.
ИНЪЕКЦИЯ СПЕРМАТОЗОИДА В ЦИТОПЛАЗМУ ЯЙЦЕКЛЕТКИ (ИКСИ)
ИКСИ – русская транслитерация английского сокращения ICSI – – инъекция с помощью микроманипуляторов единичного сперматозоида в цитоплазму яйцеклетки (intracytoplasmic sperm injection) для её оплодотворения; проводится под микроскопом при увеличении х200 – х400.
На рисунке ниже изображен процесс введения иглы для инъекции сперматозоида в яйцеклетку.
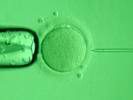
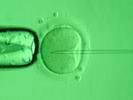

Рисунок 1. Введение иглы для инъекции сперматозоида в яйцеклетку. При проведении данной процедуры оплодотворение в пробирке происходит в 70-85% случаев.
Показания к проведению ИКСИ
• Существенное ухудшение одного или более параметров спермограммы;
• Наличие антиспермальных антител;
• Отсутствие сперматозоидов в эякуляте (азооспермия), когда получение сперматозоидов осуществляется хирургическим путем из яичка (TESA) или придатка яичка (PESA);
• Получение сперматозоидов из мочи при ретроградной эякуляции;
• Отсутствие оплодотворения в предшествующих 2-х попытках стандартной процедуры ЭКО;
• Ситуации, когда можно предполагать низкий процент оплодотворения при стандартном ЭКО, например, у пациенток с эндометриозом тяжелой степени или бесплодием неясного генеза.
Проведение данной процедуры включает в себя несколько этапов:
1. Пункция фолликулов после стимуляции суперовуляции для получения ооцитов;
2. Забор одного сперматозоида очень тонкой и острой иглой;
3. Введение сперматозоида в цитоплазму яйцеклетки под микроскопом;
4. Проверка наличия оплодотворения на следующее утро.
Частота наступления беременности при использовании процедуры ИКСИ по данным многих исследований достоверно выше частоты наступления беременности при проведении стандартной программы ЭКО.
Вероятнее всего, это связано с тем фактором, что, как правило, женщины, включенные в эту программу моложе, и являются фертильными (поскольку показанием для проведения ИКСИ является в основном мужской фактор), что приводит к повышению качества яйцеклеток, полученных в результате пункции.
Необходимо также отметить, что ИКСИ в некоторых случаях проводится и по «женским показаниям», в тех случаях, когда возможно получить лишь небольшое количество яйцеклеток и не очень хорошего качества, что связано со снижением овариального резерва.
ЭКСТРАКЦИЯ СПЕРМАТОЗОИДОВ ИЗ ПРИДАТКА ЯИЧКА (МЕЗА) ИЛИ ИЗ ТКАНИ ЯИЧКА (ТЕЗЕ)
К сожалению, у некоторых мужчин в эякуляте отсутствуют сперматозоиды, поэтому обычные методы, такие, как ЭКО и ИКСИ требуют дополнительных предварительных «шагов», позволяющих получить необходимые сперматозоиды. Именно к таким методам получения сперматозоидов и относится:
-ТЕЗЕ (testicular sperm extraction) - экстракция (извлечение) сперматозоидов из ткани яичника;
-МЕЗА (microsurgical epididymal sperm aspiration) – микрохирургическая аспирация сперматозоидов из придатков яичка;
-ПЕЗА (percutaneous epididymal sperm aspiration) – чрескожная аспирация сперматозоидов из придатков яичка.
Использование процедуры МЕЗА позволяет получить сперму наилучшего качества и в достаточном количестве по сравнению с другими технологиями. Эта процедура является также самой щадящей и имеет минимальное количество осложнений.
При проведении этих методов, как правило, стремятся к получению максимального количества сперматозоидов, которые можно потом заморозить и использовать в следующих циклах при неудачных попытках ЭКО.
Наличие азооспермии у мужчин (отсутствия сперматозодидов в эякуляте) может быть связано с несколькими факторами, именно поэтому выделяют 2 типа азооспермии:
1) Обструктивная азооспермия.
Это означает, что на каком-то уровне заблокированы протоки, через которые сперма выбрасывается наружу, то есть происходит эякуляция. Причинами этого состояния могут быть либо операции (вазэктомия), либо врожденная патология.
То есть у этой категории мужчин сперма сама по себе хорошая, однако, необходимо провести какие-то манипуляции для получения этих «здоровых» сперматозоидов. С этой целью возможно использовать либо методику ПЕЗА, при которой тонкой иглой проводится забор сперматозоидов из придатков яичка, или ТЕЗЕ при которой сперматозодиды получают из самого яичка путем его биопсии. Обе манипуляции проводятся под местной анестезией в амбулаторных условиях.
У пациентов с обстурктивной азооспермией эффективность получения сперматозоидов при проведении ТЕЗЕ стремится к 100% в том случае, если предварительная диагностическая биопсия подтвердила наличие сперматогенеза.
2) Необструктивная азооспермия.
Это патология, при которой сперматозоиды отсутствуют в эякуляте не потому, что что-то мешает их попаданию, а потому, что их количество критически снижено. Как правило, большинство таких мужчин имеют небольшие зоны в яичке, в которых образование спермы все-таки происходит, поэтому у таких мужчин проводит биопсия яичка из нескольких мест для того, чтобы обнаружить зоны активного сперматогенеза (ТЕЗЕ).
В последнее время в таких случаях используется новая методика – микроТЕЗЕ, при которой биопсия яичка проводится с использованием специального операционного микроскопа, что позволяет уже во время проведения этой манипуляции точно определить, из какой зоны необходимо брать кусочек яичка для получения максимального количества сперматозоидов.
Также может использоваться метод, имеющий название «тестикулярное картирование». Перед проведением биопсии проводится исследование зон яичка с использованием тонкой иглы, которой из нескольких мест получают жидкость, которую сразу исследуют на содержании сперматозоидов. Этот метод позволяет также наметить те зоны яичка, которые необходимо «принять во внимание» при проведении процедуры ТЕЗЕ. Как правило, сперматозоды, необходимые для оплодотворения, в таких случаях можно получить в 70%.
При использовании вышеописанных методик в дальнейшем рекомендуется использование процедуры ИКСИ для повышения вероятности оплодотворения.
ПЕРЕНОС ГАМЕТ И ЗИГОТ В МАТОЧНЫЕ ТРУБЫ
Это методы ВРТ, которые включают в себя перенос эмбрионов (англ., TET), зигот (англ., ZIFT) или гамет в маточные трубы (GIFT). По некоторым представлениям «доставка» клеток в маточную трубу, а не в полость матки, как при обычном переносе эмбриона, максимально приближена к процессу естественного оплодотворения, которое происходит в норме именно в маточной трубе.
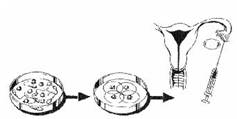
Рисунок 1. Механизм переноса гамет и зигот в маточные трубы.
Что же включают в себя эти процедуры?
ТЕТ включает в себя получение яйцеклеток, оплодотворение их в лаборатории спермой мужа «в пробирке» с последующим переносом эмбриона через 2 дня после оплодотворения в маточную трубу.
ZIFT- это перенос эмбриона через 1 день после оплодотворения, то есть на стадии зиготы. Обе процедуры требуют хирургического вмешательства в виде лапароскопии, во время которой и осуществляется перенос клеток в маточные трубы.
Кому показаны данные методы?
TET и ZIFT могут проводиться любой бесплодной паре в том случае, если маточные трубы проходимы и находятся в нормальном функциональном состоянии, а также в случае отсутствия внутриматочных синехий (спаек), то есть при удовлетворительном состоянии полости матки.
Эти процедуры могут быть показаны также при неэффективность процедуры внутриматочной инсеминации в течение 4-6 циклов.
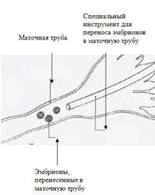
Рисунок 2. Процесс переноса гамет и зигот в маточные трубы.
ТЕТ/ZIFT (перенос гамет, зигот или эмбрионов в маточную трубу) или обычное ЭКО (перенос эмбрионов в сразу в полость матки)?
Всегда возникает вопрос: что же лучше, и в каком случае и что предпринять? Тактика в современной медицине определяется не только медицинскими показаниями, но также и пожеланиями женщины. Например, при прочих равных условиях, при отсутствии противопоказаний для переноса гамет или эмбрионов в маточную трубу, женщина настаивает на выполнении именно этой манипуляции, чтобы максимально приблизить процесс оплодотворения к естественному. Либо категорически от нее отказывается в связи с проведением лапароскопии, то есть оперативного вмешательства. Более того, каждая клиника имеет свои возможности и стоит на определенных позициях относительно того или иного метода.
Однако, ниже будут приведены некоторые факты, которые, возможно, помогут сформировать собственное мнение.
1. Согласно данным некоторых исследований частота имплантации (то есть наступления беременности) при проведении переноса в маточную трубу достоверно выше, чем при переносе в полость матки.
2. Однако, по данным рандомизированных исследований достоверных отличий при использовании переноса в маточную трубу или в полость матки не выявлено.
3. Требуются дальнейшие исследования для определения более точных показаний для включения пациентов в программу TET и проч.
4. Считается, что эффективность того или иного метода также определяется не только квалификацией врача, а также его опытом в отношении использования того или иного метода.
5. Использование методов переноса в маточную трубу достоверно повышает стоимость всей программы за счет включения в нее стоимость лапароскопии.
Таким образом, сторонники данных методов говорят
а) о высокой их эффективности;
б) максимальной приближенности к естественному процессу.
Противники переноса в маточную трубу утверждают, что
а) высокая эффективность программы переноса в маточную трубу связана с тем, что в эту программу включаются практически здоровые пациентки (имеют идеальные маточные трубы и полость матки) и ведущим фактором бесплодия является исключительно мужской — с
8-09-2015, 19:38
