На нейронах заднего рога конвергируют не только разномодальные кожные, но также мышечные и висцеральные афференты. Происходящее на этих нейронах взаимодействие соматовисцеральных афферентных потоков лежит в основе возникновения отраженной боли. Установлено, что нейроны, на которых осуществляется взаимодействие соматических и висцеральных афферентов, активируются через висцеральные входы при естественном раздражении висцеральных рецепторов, но только в том случае, когда интенсивность воздействия, например давление в желчных путях достигает ноцицептивного уровня.

Рис. 3 - Ответ нейрона IV слоя заднего рога спинного мозга на ноцицептивное раздражение кожи, наносимое до и после ритмической стимуляции пизкопороговых афферентов. 1 — фоновая импульсная активность: 2 — импульсная активность при ноцицептивном раздражении до стимуляции низкопороговых афферентов: 3 — то же после ритмического раздражения низкопороговых афферентов
Линия под осциллограммами — период ноцицсптпвного воздействия на кожу. Калибровка: времени — 1 с, амплитуды — 250 мкВ.
Естественно, что не все нейроны заднего рога имеют ноцицептивные афферентные входы. Во всех пластинах, особенно в IV, имеется достаточно большая популяция клеток с узким функциональным диапазоном, которые активируются легкими механическими воздействиями и не отвечают на повреждающие стимулы. В то же время клетки, отвечающие на ноцицепцию, выявлены в VI пластине и даже в вентральном роге. Эти нейроны, вероятно, участвуют в регуляции не только моторной, но и сенсорной деятельности спинного мозга, и в частности в регуляции боли, способствуя локализации ответа на боль. Поэтому цитоархитектонически выделяемые пластины в заднем роге спинного мозга скорее должны рассматриваться как зоны преимущественной концентрации нейронов с определенными свойствами, а не как строго функционально специализированные нейронные ансамбли.
Таким образом, можно считать, что конвергентные нейроны, локализованные в основании заднего рога, большинство из которых имеют восходящие проекции, принимают самое непосредственное участие в возникновении информации такого качества, которая высшими отделами головного мозга расценивается как болевая и которая запускает сложные механизмы ответного реагирования на боль. Однако в настоящее время есть все основания считать, что активность релейных нейронов, связанных с ноцицептивной афферентацией, их ответы на разномодальные стимулы, взаимодействие на них различных афферентных входов и, следовательно, формирование восходящего импульсного потока модулируется нейронами желатинозной субстанции.
Нейроны желатинозной субстанции, локализованные во II пластине, стали предметом активного исследования в последние 15—20 лет. Морфофункциональная организация этой области детально рассматривается в специальных обобщающих статьях и обзорах. Поэтому здесь мы коснемся лишь некоторых свойств нейронов желатинозной субстанции, необходимых для понимания их роли в регуляции ноцицепции.
Эти нейроны имеют рецептивные поля различных размеров, формы и локализации. У половины из них рецептивные поля по размерам и локализации соответствуют таковым у нейронов IV—V пластин и располагаются в пределах какой-либо одной области нижней конечности. Характерной особенностью 1/3 нейронов желатинозной субстанции является наличие у них очень маленьких рецептивных полей. У незначительного количества нейронов рецептивные поля занимали всю поверхность ипсилатеральной и иногда даже контралатеральной конечности. Именно на них конвергируют А-δ-, С-волокна, а на некоторых и А-р-афференты. Примечательно, что аксоны этих клеток не выходят за пределы спинного мозга.
Ориентация аксонов желатинозных нейронов весьма различна и во многом определяется локализацией сомы клетки. У нейронов, расположенных в дорсальной части желатинозной субстанции, аксоны направлены дорсально и проецируются в тракт Лиссауэра. Аксоны нейронов средней трети идут в продольном направлении внутри желатинозного вещества. По мере приближения к нижней границе желатинозной субстанции аксоны принимают вентральное направление и проникают, как правило, в глубжерасположенные слои заднего рога. О протяженности аксональных проекций имеются разноречивые и даже полярные представления. Согласно одним данным, аксоны нейронов желатинозной субстанции оканчиваются в пределах одного сегмента, в то время как по другим — они достигают даже таламуса. Однако аксоны большинства желатинозных нейронов не проецируются дальше одного сегмента и оканчиваются в пластинах I, IV, V или даже в пределах одной II пластины. У меньшей части нейронов аксоны, входящие в тракт Лиссауэра, прослеживаются на расстоянии 15 — 40 мм.
Отдельные клетки имеют контралатеральные аксональные проекции.
Основная масса нейронов имеет спонтанную активность в диапазоне от 1 до 40 имп/с. Она представлена разрядами постоянного ритма без высокочастотных «пачек» импульсов. Ни перерезка дорсолатеральных канатиков, ни полная спинализация существенно не изменяли фоновую активность желатинозных нейронов, что свидетельствует о ее независимости от нисходящей тонической регуляции и о большой роли афферентного сегментарного входа в ее формировании. Нейроны желатинозной субстанции реагируют на естественное раздражение их рецептивного поля. Большинство клеток отвечали как на неповреждающую механическую, так и на ноцицептивную стимуляцию. По данным Р. Cervero и A. Iggo, разномодальная активация рецептивного поля сопровождается исключительно торможением активности нейронов, и в зависимости от характера воздействия они могут быть разделены на 3 группы. В первую группу входят клетки, активность которых тормозилась при низкопороговой механической стимуляции рецептивного поля. Вторую группу составляют нейроны, торможение активности которых возникало при раздражении рецептивного поля как повреждающими, так и неповреждающими стимулами. К третьей группе были отнесены клетки, разряды которых угнетались только при ноцицептивном раздражении рецептивного поля. Эти 3 группы клеток в функциональном отношении, т.е. по характеру ответов на разномодальную стимуляцию рецептивного поля, являются антиподами глубжерасположенных нейронов.
По общепринятому мнению, клетки желатинозной субстанции отличаются от других нейронов заднего рога, в частности V пластины, характером ответов на раздражение С-волокон и взаимодействием А- и С-афферентных входов. Так, нейронам желатинозной субстанции не свойствен феномен «взвинчивания». Они не изменяют, как нейроны V пластины, ответы на раздражение С-волокон при выключении А-афферентов, а предшествующая стимуляция их не уменьшает ответные реакции желатинозных нейронов, возникающие при внутриартериальном введении брадикинина. Наряду с хорошо изученным быстрым реагированием нейронов желатинозной субстанции на разномодальные афферентные воздействия, выявлены более медленно и длительно протекающие изменения их активности. Эти изменения, вероятно, обусловлены действием различных биологически активных соединений, осуществляющих нейромодуляторную функцию, таких как энкефалпны, соматостатин, ангиотензин, холецистокинин, гликокортикоиды, субстанция Р, ГАМ.К, норадреналин, серотонин, локализующихся в дорсальной части заднего спинного мозга. Однако функциональная роль медленных, длительных изменений активности нейронов желатинозной субстанции и их связь с регуляцией ноцицептивного афферентного потока пока не выяснены и требуют новой концептуальной гипотезы.
Функциональная роль желатинозной субстанции до настоящего времени весьма спорна. Практически все исследователи придают ей важное значение как нейрональной системе, регулирующей сенсорный вход и болевую чувствительность на сегментарном уровне. Однако каждый имеет свое, порой весьма противоречащее имеющимся, представление о механизмах этой регуляции. В настоящее время снова получила подтверждение и развитие точка зрения, высказанная более 30 лет назад, о том, что желатинозная субстанция функционирует как релейная инстанция, передающая ноцицептивную информацию от первичных афферентов к нейронам спиноталамического тракта. Именно в области желатинозной субстанции оканчивается основная масса ноцицептивных А-δ- и С-афферентов, которые непосредственно активируют нейроны желатинозной субстанции.
Согласно другой, более общепринятой концепции клетки желатинозной субстанции не просто передают, а модулируют, эффективность синаптического воздействия афферентных входов на нейроны дорсального рога спинного мозга. Традиционно считается, что эта модуляция реализуется тормозными механизмами и что большая часть клеток желатинозной субстанции функционирует как тормозные интернейроны. Примечательно, что налоксон при внутривенном введении, возбуждая нейроны V пластины, одновременно угнетает активность нейронов желатинозной субстанции.
Модуляция афферентного сегментарного входа клетками желатинозной субстанции может осуществляться как пост-, так и пресинаптическими механизмами. В настоящее время известно немало достаточно хорошо проверенных фактов, свидетельствующих о важной роли желатинозной субстанции в генерации деполяризации первичных афферентов. Желатинозной субстанции отводится ключевая роль в одной из самых распространенных и, пожалуй, самых дискуссионных теорий боли — теории «входных ворот» P. Мелзака и Р. Уолла. Эта теория в первом ее постулате объясняет формирование ноцицептивного потока на сегментарном уровне на основе центрального взаимодействия быстропроводящей миелиновой и медленнопроводящей безмиелиновой систем на первых релейных нейронах спинного мозга. Афферентная импульсация, возникающая в миелиновых волокнах при неповреждающих раздражениях, одновременно с активацией релейных нейронов через коллатерали возбуждает нейроны желатинозной субстанции. Они, в свою очередь, деполяризуют первичные миелиновые афференты и тем самым пресинаптически ограничивают активирующее их влияние на Т-клетки. При ноцицептивном воздействии активируются тонкие миелиновые и безмиелиновые волокна, которые оказывают тормозное влияние на нейроны желатинозной субстанции, в результате чего уменьшается деполяризация миелиновых волокон, т.е. «открывается» афферентный вход и возрастает эффективность синаптического воздействия на Т-нейроны. Т-нейроны при достижении критического уровня, определяемого временной и пространственной суммацией «ноцицептивных» и неноцицептивных сигналов, формируют восходящий поток импульсов нового качества, который воспринимается вышерасположенными структурами мозга.
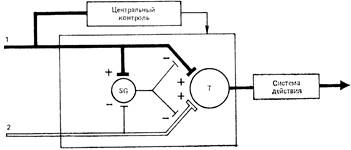
Рис. 4 - Схема системы контроля афферентного входа
Положение теории Р. Мелзака и П. Уолла о том, что процессы пресинаптического торможения и облегчения являются ведущими в реализации модулирующего влияния желатинозной субстанции, длительное время являлись предметом активного обсуждения. Эта теория, как и любая новая теория, постоянно совершенствуется и дополняется. В современных ее модификациях, и в том числе самих авторов, больший акцент сделан на роль постсинаптических и нейрохимических процессов в регуляции передачи разномодальных импульсов на релейные нейроны спинного мозга.
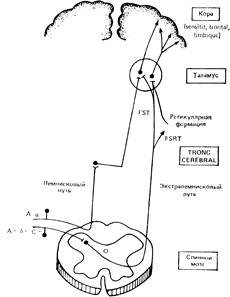
Рис. 5 - Схема лемнисковой и экстралемнисковой восходящих афферентных систем
Таким образом, можно считать, что формирование восходящего «ноцицептивного» потока в спинном мозге происходит двумя способами — на основании взаимодействия разномодальных афферентных входов на релейных нейронах и в результате активации «специфических болевых» нейронов, имеющих восходящие проекции.
Восходящие пути болевой чувствительности. Существуют 2 основные «классические» — лемнисковые и экстралемнисковые — восходящие афферентные системы. В пределах спинного мозга одна из них располагается в дорсальной и дорсолатеральной зоне белого вещества, другая — в его вентролатеральной части. Известно, что в ЦНС не существует специализированных путей болевой чувствительности и что интеграция боли осуществляется на различных уровнях ЦНС на основе сложного взаимодействия лемнисковых и экстралемнисковых проекций. Вместе с тем не вызывает сомнений тот факт, что значительно большую роль в передаче восходящей ноцицептивной информации играют вентролатеральные проекции, морфофункциональная организация которых детально исследована и обобщена в ряде монографий и обзоров. Об этом свидетельствуют и клинические наблюдения, показывающие, что после антеролатеральной хордотомии или деструкции этой системы при некоторых заболеваниях возникает длительная и выраженная аналгезия. С другой стороны, ощущение боли и ее локализация сохраняются при перерезке всех, кроме вентролатеральных, путей, а стимуляция аксонов в антеролатеральном квадранте после хордотомии вызывает интенсивную боль.
Источниками вентролатеральных проекций являются нейроны I—V и даже VI—VIII пластин спинного мозга, аксоны которых имеют диаметр от 1 до 11 мкм и скорость проведения 7—74 м/с. Вентролатеральные восходящие пути в пределах спинного мозга имеют определенную соматотопическую организацию — волокна, исходящие из более каудальных сегментов, располагаются более латерально, а из ростральных — медиально и вентрально. Конечные проекции первоначально выявляются в продолговатом мозге, затем — в среднем и, наконец, в галамусе. В зависимости от места окончания восходящая антеролатеральная система разделяется на 3 основных тракта — спиноталамический, спиноретикулярный и спиномезенцефалический. Первый из них обозначается как неоспиноталамический, а два других объединяются в палеоспиноталамический тракт. Однако данные последних лет со все большей убедительностью свидетельствуют об относительности такого строгого разделения, поскольку коллатерали аксонов одних и тех же нейронов спинного мозга могут проецироваться в различные супрасегментарные структуры. Более того, предполагается, что некоторые свойства нейронов — источников восходящих трактов: размеры рецептивных полей, ответы на разномодальные стимулы, скорость проведения по аксону — различаются в зависимости от проекции их аксонов.
Неоспиноталамический тракт начинается от нейронов I, V и частично VI — VII пластин спинного мозга. Нейроны — источники этого тракта, имеют кожные рецептивные поля различных размеров. В зависимости от модальности афферентных входов они разделяются на несколько групп. Одни из них, локализованные преимущественно в I пластине, активируются только ноцицептивными стимулами, другие, в основном клетки IV — V пластин, отвечают и на неповреждающие воздействия. На большинстве нейронов спиноталамического тракта, располагающихся в V пластине, конвергируют мышечные, кожные, висцеральные афференты, и эти клетки отвечают прогрессивно увеличивающейся частотой разрядов на неноцицептивную и разномодальную ноцицептивную стимуляцию. Аксоны спиноталамических нейронов после перекреста в передней комиссуре восходят контралатерально в вентролатеральном квадранте спинного мозга. В стволе головного мозга Неоспиноталамический тракт располагается дорсолатеральнее пирамид и нижнеоливарного комплекса и, не прерываясь, достигает таламуса. В пределах заднего таламуса он разделяется на латеральную и медиальную части. Первая из них оканчивается преимущественно в n. ventralisposteriorlateralis, а вторая — в медиальных и интраламинарных ядрах. Недавно установлено, что нейроны — источники спиноталамического тракта содержат глутамат и холецистокинин. Выявлено даже различие в их нейрохимической организации в зависимости от проекции аксонов — нейроны, аксоны которых оканчиваются в медиальном таламусе, содержат энкефалин и динорфин, в то время как клетки, проецирующиеся в латеральный таламус, — вазоактивный интестинальный пептид.
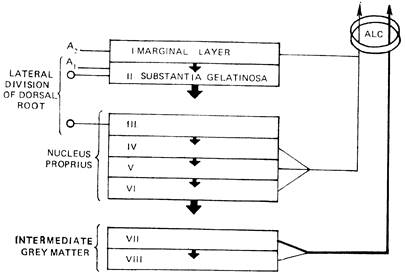
Рис. 6 - Схема источников путей, восходящих в антеролатеральных столбах спинного мозга. I — VIII — слои серого вещества спинного мозга по В. Rexed
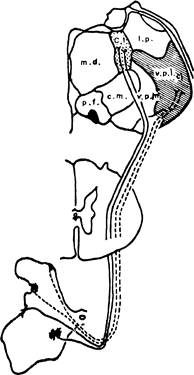
Рис. 7 - Схема спиноталамического тракта. Ядра таламуса, с. 1. — центральное латеральное, с. т. — центральное медиальное; 1. р. — латеральное заднее, m. d. — медиальное заднее, р. f. — парафасцикулярное, v, р. I. каудальная часть вентрального заднелатерадь-ного; v. р. m. — вентральное заднемедиальное
Прецизионными электрофизиологическими и гистологическими методами установлены различные проекции спиноталамических нейронов в таламусе. Аксоны спиноталамических нейронов I пластины и IV—V пластин оканчиваются соответственно в его вентролатеральных и задних ядрах, а глубжерасположенные клетки — в интраламинарных ядрах. Однако тонкая структура терминалей спиноталамических проекций из I и V слоев заднего рога спинного мозга в вентробазальный комплекс таламуса не отличается от таковой у терминалей спиноталамических аксонов клеток VII слоя заднего рога, оканчивающихся в центральном латеральном ядре таламуса. Спиноретикулярные нейроны имеют небольшие кожные рецептивные поля и активируются как неноцицептивными, так и ноцицептивными стимулами, причем частота их разрядов увеличивается с усилением интенсивности раздражения.
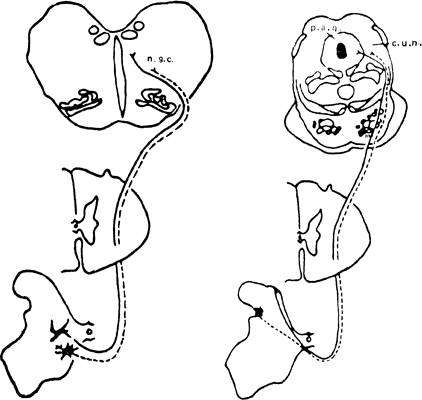
Рис. 8 - Схема спиноретикулярного тракта. n. g. с. — гигантоклеточное ядро.
Спиноретикулярный тракт оканчивается в каудальной части ствола мозга. Именно в этой области, особенно в ретикулярном гигантоклеточном ядре, парагигантоклеточном ядре и в большом ядре шва, обнаружена массивная конечная дегенерация при перерезке вентролятеральных столбов. У человека больше половины волокон, восходящих в вентролатеральных столбах, оканчивается ипси- и контралатерально в зоне медиальных и латеральных ядер ретикулярной формации продолговатого мозга. Восходящие проекции от этих ядер достигают интраламинарных ядер таламуса и диффузно распространяются в гипоталамусе и лимбических структурах.
Спиномезенцефалический тракт иногда рассматривается как компонент спинорстикулоталамической системы, поскольку он формируется аксонами нейронов тех же пластин, где локализованы спиноретикулярные клетки. Однако есть отличие в его морфологической организации и проекциях. Волокна спиномезенцефалического тракта в вентро-латеральных столбах располагаются более поверхностно. Часть из них перекрещивается в спинном мозге, другие восходят преимущественно ипсилатерально и перекрещиваются в области покрышки головного мозга. У кошек часть спиномезенцефалических проекций от нейронов I слоя располагается в дорсолатеральном канатике. Оканчивается спиномезенцефалический тракт в ретикулярной формации среднего мозга в центральном сером веществе и в таламусе. Клетки — источники спиномезенцефалического тракта различаются по локализации в спинном мозге, по размерам рецептивных полей, по ответам на разномодальные стимулы в зависимости от окончания их аксонов. К этим восходящим волокнам добавляются многочисленные проекции из бульбарных структур, и вся эта сложная система часто объединяется в «диффузный покрышковый» или спинотектальный путь. В среднем мозге он отдает коллатерали в центральное серое вещество и в глубокие отделы верхних бугров. Волокна из центрального серого вещества, в свою очередь, проецируются в медиальные таламические ядра, в вентральную тегментальную область и в гипоталамус.
Антеролатеральные тракты являются основной, но не единственной ноцицептивной системой. Известно, что после антеро-латеральной хордотомии примерно у 50% лиц через несколько месяцев снова возникала боль. Имеются также многочисленные экспериментальные и клинические данные о невозможности получения стойкой аналгезии при разрушении таламических сенсорных ядер. Определенное значение в передаче болевой информации в ростральном направлении имеют тракты, восходящие в дорсальных и дорсолатеральных столбах белого вещества спинного мозга, традиционно относящиеся к лемнисковой афферентной системе.
Спиноцервикальный тракт —
отчетливо выражен у низших млекопитающих, особенно кошек, и в меньшей степени у обезьян и человека. Он формируется аксонами клеток IV—VII пластин, которые восходят в дорсолатеральных столбах и оканчиваются в латеральном цервикальном ядре на уровне Ci-ii шейных сегментов. Нейроны — источники этого тракта активируются тактильными и различными ноцицептивными раздражениями их рецептивных полей. От латерального шейного ядра афферентные проекции восходят через латеральную часть медиального лемниска, оканчиваются в среднем мозге и в контралатеральном задневентральном ядре
8-09-2015, 20:15
