Таким образом, на начальном этапе развития заболевания под воздействием эндотоксинов происходит в первую очередь расширение стенок мелких сосудов (в основном венул), а также значительно повышается проницаемость сосудистой стенки. В результате всего вышеизложенного, несмотря на отсутствие абсолютного дефицита объема, венозный возврат к сердцу уменьшается (относительная гиповолемия). В ответ на это происходит рефлекторное симпатическое сужение вен. Но активное сужение вен эффективно уменьшает венозное кровенаполнение только в том случае, если вены хорошо наполнены и растянуты. Если же трансмуральное давление достаточно низко, чтобы привести вены в полуспавшееся состояние, даже сильные сокращения гладкой мышцы вен оказывают только незначительное влияние на количество крови в них. При такой ситуации сужение вен может даже несколько увеличить местную емкость вен, так как оно делает стенку более жесткой, в результате чего просвет становится большим и приобретает более круглую форму, несмотря на то, что просвет окружности уменьшается. В результате снижения венозного возврата повышается активность симпатической нервной системы, что наряду с непосредственным влиянием эндотоксинов ведет к сокращению пре- и посткапиллярных сфинктеров (стимуляция a-рецепторов). В результате кровоснабжение тканей становится недостаточным, минутный объем сердца в эту фазу большей частью нормальный или даже повышенный (т. е. МОС нормальный или увеличенный, ЧСС увеличивается, общее периферическое сопротивление уменьшается и снижается АД). Артерио-венозная разница по кислороду и обеспечение периферии кислородом понижены.
В дальнейшем по мере дальнейшего развития шока происходит формирование рокового порочного круга. Прекапиллярные артериальные сфинктеры более чувствительны к токсическим влияниям (в том числе ацидозу), поэтому их спазм быстро сменяется парезом. Посткапиллярные (венулярные) сфинктеры более устойчивы к метаболическим нарушениям и длительное время остаются в состоянии тонического напряжения. Таким образом, кровь, притекающая в капиллярное русло депонируется, в связи с чем нарастает тканевая гипоксия, усугубляется метаболический ацидоз, пропотевает плазма с нарастающей компрессией капилляров, что наряду с застоем крови в венозном русле, способствует дальнейшему уменьшению венозного возврата и увеличению относительной гиповолемии.
В результате возникает следующая причинно-следственная связь: стаз в капиллярах - висцеральный застой - уход воды - повышение вязкости крови - агрегация красных и белых кровяных телец, образование красного и белого тромба - истощение факторов свертывания и тромбоцитов вследствие диссеминированного внутрисосудистого свертывания - возникновение изнуряющей коагулопатии с повышенной предрасположенностью к кровотечению.
В пораженных областях аэробные энергетические пути переключаются на анаэробный гликолиз. Переключение окислительного обмена на гликолитический путь значительно увеличивает потребление глюкозы при одновременном уменьшении выхода АТФ. Это снова ведет к снижению уровня глюкозы. Биосинтез белка при шоке ограничен. Это особенно быстро влияет на синтез тех белков, которые имеют короткое время полужизни, например, факторы свертывания. Таким образом, нарушение свертывания крови еще более усиливается. При шоке начинается выход калия из клеток. Метаболический ацидоз возникает в результате увеличенной продукции лактата, а также пирувата, a-кетоглутарата и кетоновых тел. Ацидоз частично компенсируется усиленным дыханием. В результате повышения концентрации Н+ в плазме наблюдается следующее: отрицательное инотропное действие на сердце; снижение чувствительности прекапиллярных сфинктеров в смысле вазомоторных реакций с образованием отеков; повышение выброса катехоламинов; активирование свертывающей системы в качестве одной из причин диссеминированного внутрисосудистого свертывания. Некоторые вещества, образующиеся при шоке (в частности и сами цитокины), обладают отрицательным инотропным действием. Длительное действие этих факторов ведет к расширению сердца и сердечной недостаточности, тем самым, к уменьшению МОК.
Почки. По причине эфферентного сокращения сосудов при шоке уменьшается давление гломерулярной фильтрации, в результате чего развивается олигурия (4-20 мл/ч) или анурия (4 мл/ч). Сужение почечных сосудов сохраняется еще долгое время после нормализации давления крови. Ишемия вызывает прогрессирующий некроз канальцев вследствие гломерулярной, а затем тубулярной недостаточности с образованием цилиндров в дистальных канальцах. Признаком почечной недостаточности является увеличение содержания в крови таких, обычно выделяющихся с мочой соединений, как мочевина и креатинин.
Таким образом, одним из основных патофизиологических механизмов в развитии инфекционно-токсического шока при пневмониях следует считать развитие гиповолемии вследствие секвестрации крови в микроциркуляторном русле и выхода ее в ткани из-за повышения проницаемости капилляров. По образному выражению И. Теодореску-Ексари при ИТШ происходит «кровотечение в собственные сосуды».
Патогенетические стадии
Стадия компенсации
Компенсаторные прессорные реакции, направленные на поддержание АД и восполнение ОЦК. Происходит выброс катехоламинов, вызывающих спазм прекапиллярных сфинктеров. Открываются прямые артериовенозные шунты.
Стадия субкомпенсации
Инициальный спазм прекапилляров сменяется парезом и застоем крови в вено-венулярном отделе микроциркуляторного русла. В эту стадию развивается циркуляторная недостаточность (шок). Снижается венозный возврат к сердцу - снижается сердечный выброс. Включаются компенсаторные реакции – тахикардия, резорбция провизорного фильтрата в почечных канальцах. При уменьшении венозного возврата на 25-30% начинается декомпенсация со снижением АД и нарушением перфузии жизненно важных органов. В этих условиях реализуются механизмы централизации кровообращения.
Нарастает метаболический ацидоз - тахипное. возникают биоплярные изменения КОС – респираторный алкалоз в малом круге и метаболический ацидоз в большом.
Стадия декомпенсации
Характеризуется присоединением ДВС-синдрома - тканевая гипоксия - изменения в шоковых органах.
«Предтечей» ДВС синдрома является изменение реологии крови – сладж феномен.
В нормальных условиях кровь имеет характер стабильной суспензии.
Сохранность суспензионной стабильности крови обеспечивается величиной отрицательного заряда эритроцитов и тромбоцитов (дзета-потенциал – потенциал поверхности скольжения частицы в коллоидном растворе), определяемом соотношением белковых фракций (альбумины/глобулины) и достаточностью кровотока.
Уменьшение отрицательного заряда эритроцитов (увеличение глобулинов или фибриногена, их абсорбция на поверхности эритроцитов) приводит к развитию сладжирования крови.
Сладж (от англ. sludge – густая грязь, тина) – изменение реологии крови, характеризующееся прилипанием друг к другу эритроцитов, лейкоцитов и тромбоцитов и повышением вязкости крови, что затрудняет её перфузию через микрососуды.
Сладж может быть обратимым (только при агрегации эритроцитов) и необратимым (агглютинация эритроцитов).
Типы сладжа:
1. Классический – крупные размеры агрегатов, неровные очертания контуров и плотная упаковка эритроцитов;
2. Декстрановый – различная форма и величина, округлые очертания, плотная упаковка;
3. Аморфный грануловидный – мелкие агрегаты в виде гранул, состоящих из нескольких эритроцитов.
Сладж - резкое замедление кровотока, сепарация плазмы от эритроцитов, маятникообразные движения плазмы - стаз.
В связи с закупоркой терминальных артериол большим количеством агрегатов, капиллярные сосуды пропускают только плазму. При этом повреждается стенка сосудов (набухание, десквамация эндотелия).
Параллельно с процессами сладжирования и предшествуя им происходит нарушение проницаемости сосудов обмена (капилляры, венулы) в сторону её повышения. Это приводит к выходу жидкой части крови в интерстиций и сгущению крови, что усиливает процессы агрегации эритроцитов.
Морфологической основой проницаемости сосудов является эндотелий и базальная мембрана + периваскулярная ткань = неспецифический гистогематический барьер.
В морфологическом отношении повышение сосудистой проницаемости характеризуется увеличением промежутков между эндотелиоцитами вследствие сокращения и усиления везикулярного транспорта.
Раннее повышение проницаемости связано с воздействием биологически активных аминов и брадикинина, позднее (более 60 минут) – протеаз, каллидина, глобулярных веществ нейтрофилов. Действие этих веществ направлено на стенку капиллярных сосудов – межклеточный цемент эндотелия и базальную мембрану и заключается в физико-химических изменениях (деполимеризация сложных белково-полисахаридных комплексов).
Схема патогенеза шока
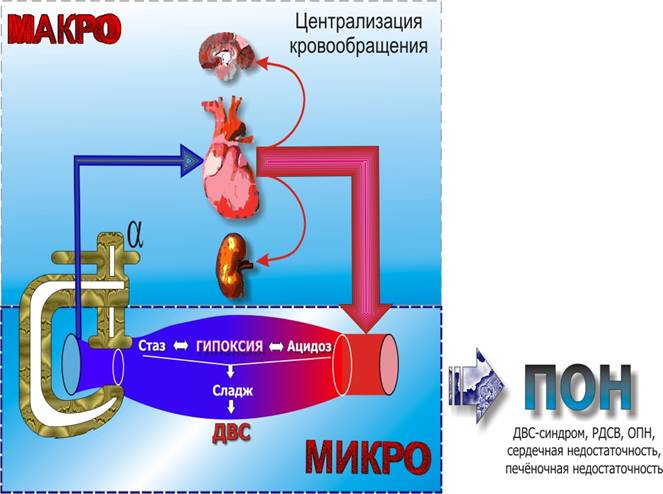
Клиническая картина
Шок развивается на фоне нарастания интоксикации: у больного появляется озноб, за которым следует резкий подъем температуры, часто наблюдается тошнота, рвота, диарея, состояние прострации.
В клиническом плане выделяют следующие группы симптомов, определяющих степень тяжести и прогноз.
| № | Критерии септического синдрома |
| 1. | Клинические признаки инфекции |
| 2. | Температура тела выше 38о С или ниже 36о С |
| 3. | Частота дыхания > 20 в минуту |
| 4. | Число сердечных сокращений > 90 в минуту |
| 5. | Количество лейкоцитов больше 12,0х109 /л или меньше 4,0х109 /л или при 10% незрелых форм |
| 6. | 1 или более изменений со стороны следующих органов: - нарушение сознания; - Ро2 < 70 мм рт. ст.; - олигоурия < 30 мл/час; - увеличение уровня лактата. |
К числу ранних признаков начинающегося ИТШ относятся гипервентиляция, вызывающая респираторный алкалоз, и церебральные нарушения в виде беспокойства или заторможенности. Эти первые симптомы шока часто не привлекают внимание, что приводит к запоздалой диагностике и ухудшает прогноз. По мере развития болезни усиливается тахикардия, одышка, артериальная гипотензия, а иногда тенденция к гипертензии, наблюдается бледность конечностей с акроцианозом. Кожные покровы теплые и сухие («теплый шок»).
При исследовании в этот период определяется: снижение ОПСС и могут появляться ранние признаки снижения фракции выброса (нормализуется на 7-10 сутки), увеличение сердечного выброса, ЧСС, частоты дыханий и Ро2 смешанной венозной крови (из-за артериовенозного сброса)
При прогрессировании шока развивается артериальная гипотензия, нарастает олигурия. При исследовании у этих больных отмечаются низкие значения центрального венозного давления (ЦВД), низкий объем циркулирующей крови (ОЦК) и сердечный выброс, отмечается повышение ОПСС, ЛСС, альвеолярно-артериального градиента Ро2 , уменьшение рН и Ро2 в артериальной крови т. е. гиподинамическая реакция системного кровообращения, нарастает олигурия и молочнокислая ацидемия. Возникает полиорганная недостаточность (СН, острая почечная недостаточность, РДСВ, печеночная недостаточность, ДВС-синдром).
Основные признаки инфекционно-токсического шока
| Система | Патология |
| ЦНС | Энцефалопатия |
| ЖКТ | Холестатическая желтуха Эрозии желудка |
| Кровь | Ранняя нейтропения, затем нейтрофилия ДВС, особенно при грам «-» бактеримии Тромбоцитопения в 50% |
| Почки | Протеинурия Фокальный пролиферативный гломерулонефрит Острый тубулонекроз |
| Метаболизм | Гипер-, гипогликемия Костно-мышечный протеолизис Гипертриглицеридемия Молочный ацидоз |
| Органы дыхания | Респираторный алкалоз Повышение альвеолярно-артериального градиента Ро2 Респираторная мышечная недостаточность |
Прогноз относительно благоприятный, если быстро начата надлежащая терапия. Во II стадии летальность 40%, в III – 60%.
По мере развития шока отмечается дальнейшее снижение артериального давления, цвет кожных покровов серый, конечности холодные. При исследовании определяется увеличение показателей ЦВД, выраженный метаболический ацидоз и очень высокая концентрация молочной кислоты. Прогноз очень неблагоприятный.
В дальнейшем артериальное давление падает до 50-20 мм рт. ст. и ниже, а часто не определяется. У некоторых больных отсутствует температурная реакция и даже наблюдается гипотермия. У больных низкие показатели ЦВД, низкий ОЦК, сердечный выброс и выраженная молочнокислая ацидемия, которую не компенсирует респираторный алкалоз. Изменяются электролиты крови, отмечается тенденция к гипонатриемии и гипокалиемии. На ЭКГ могут регистрироваться изменения, иногда трудноотличимые от таковых при остром инфаркте миокарда. У таковых больных наступает кома. Летальность при таких проявлениях достигает 100%.
Причины смерти: полиорганная недостаточность(50%), стойкая артериальная гипотензия (40%), тяжелая сердечная недостаточность (10%).
стадии ИТШ
| Критерий | СТАДИЯ | ||
| Компенсации | Субкомпенсации | Декомпенсации | |
| 1. Сознание | Ясное, иногда беспокойство, тревога. | Больные вялые, адинамичные | Сознание угнетено (ступор, сопор) |
| 2. Кожные покровы | Обычной окраски, тёплые на ощупь | Серовато-синего цвета, нередко с мраморным рисунком, холодные на ощупь. Акроцианоз. | Холодные, цианотичные, иногда землистого оттенка. |
| 3. Дыхание | До 30 в минуту | > 30 в минуту, поверхностное | Патологические типы дыхания |
| 4. АД | > 90 и 60 mm.Hg. | 85/60-60/20 mm.Hg. | 50/00-20/0 mm.Hg. |
| 5. ЧСС | Тахикардия до 100 в мин. | > 100 в мин. | > 140 в мин. Пульс нитевидный. |
| 6. Пульсовое давление | В норме | 15-20 mm.Hg. | > 20 mm.Hg. |
| 7. Индекс Алговера | 0,9-1,0 | 1,5 | 2 и более |
| 8. Диурез | Сохранён | Олигурия | Анурия |
Лечение
В основе рационального лечения при ИТШ лежит тщательное наблюдение за больным. Весьма полезна непрерывная регистрация клинических данных. У постели больного особенно важно следить за некоторыми основными показателями:
1. Состояние легочного кровотока (и желательно функцию левого желудочка) контролируют с помощью катетера Свана-Ганца. При его отсутствии необходимо измерять центральное венозное давление (ЦВД). Введение катетера в крупные вены или в правое предсердие позволяет получить точные данные о связи между состоянием правого желудочка и объемом циркулирующей крови, что дает возможность регулировать объем вводимой жидкости. ЦВД выше 12-14 см вод. ст. указывает на некоторую опасность продолжения введения жидкостей и угрозу развития внезапного отека легких.
2. Пульсовое давление позволяет оценить величину ударного объема сердца.
3. Сужение кожных сосудов свидетельствует о сопротивлении периферических сосудов, хотя и не отражает полностью нарушения кровотока в почках, мозге или кишечнике.
4. Почасовое измерение объема выделенной мочи позволяет контролировать уровень кровотока во внутренних органах и степень их перфузии. Обычно для этого необходимо введение постоянного мочевого катетера.
обязательным терапевтическим мероприятием для данной категории больных является соблюдение ПОСТЕЛЬНОГО РЕЖИМА! (учитывая наличие недостаточного венозного возврата, что может усугубляться в вертикальном положении).
Большое значение в проведении лечебных мероприятий у больных с ИТШ имеет, наряду с активной АНТИБИОТИКОТЕРАПИЕЙ, инфузионная терапия . При проведении инфузионной терапии необходимо учитывать, что при пневмониях, чаще вирусно-бактериальных на фоне имеющихся изменений в легких внутривенное введение растворов, в особенности физиологического и 5% глюкозы, может привести к отеку легких, а в некоторых случаях и к отеку мозга. Поэтому проводить инфузионную терапию необходимо строго дифференцированно с учетом конкретных показаний и под постоянным контролем за общим состоянием, уровнем гемодинамики, диурезом, показателями ЦВД, а также за объективными данными со стороны легких. Обычно у больных с острой сердечно-сосудистой недостаточностью инфузию начинают с полиглюкина, после проведения пробы на реактогенность: в течении 1-й минуты вводят объемвосстанавливающий (замещающий) раствор со скоростью 10-15 кап/м, затем делается 3 минутный перерыв - оценка самочувствия больного; 2-я минута - 20-30 кап/м, затем 3 мин перерыв - оценка самочувствия больного. Если состояние не ухудшилось, производится в/в капельное введение препарата с необходимой скоростью, но не более 60-80 капель в мин. Полиглюкин вводится если уровень АД менее 100 мм рт. ст. Если давление составляет 100-110 мм рт. ст. можно вводить реополиглюкин, который дает не только гемодинамический и дезинтоксикационный эффект, но и улучшает микроциркуляцию, устраняет стаз в капиллярах, снижает адгезию и агрегацию тромбоцитов, что лежит в основе его антитромботического действия. Обычно вводится 400 мл полиглюкина и 400-600 мл реополиглюкина. Если эффект недостаточен, используется плазма, альбумин. При отсутствии вышеперечисленных препаратов в/в в течение 5 минут вводят 200 мл 0,9% NaCl или раствор Рингера с лактатом. В отсутствие эффекта дополнительно вводят 1-1,5 л растворов за 20 минут. Если симптомы шока сохраняются, показан инвазивный мониторинг гемодинамики и введение 2-4 литров инфузионных растворов за 1 час. При тяжелом шоке, а также при отеке легких показаны вазопрессорные средства.
Так же могут быть использованы препараты гидроксиэтилкрахмала, которые более эффективно, чем декстрановые производные предупреждают синдром избыточных капиллярных потерь.
Инфукол ГЭК (рефортан, стабизол) выпускается в виде 6% и 10% раствора во флаконах по 100, 250 и 500 мл. Средняя/максимальная доза составляет 2 г/кг, что соответствует 33 мл 6% раствора или 20 мл 10% раствора. Вводят внутривенно, капельно. Первые 10-20 мл вводят медленно (контроль общего состояния для исключения анафилактических и анафилактоидных реакций).
Препарат противопоказан при гипергидратации, декомпенсированной сердечной недостаточности, почечной недостаточности с олигурией и анурией, при выраженном нарушении свёртывания.
Вазопрессорные средства. Дофамин, 5-20 мкг/кг/мин в/в; в отсутствии эффекта добавляют норадреналин, 0,5-30 мкг/ мин в/в, по возможности уменьшая дозу дофамина до «почечной» (2-4 мкг/кг/мин).
Режимы дозирования допамина:
1. Доза 1,0-5,0 мкг/кг/мин – «почечная», вызывает расширение коронарных, церебральных и почечных артерий. Прочие симпатомиметики повышают почечный кровоток исключительно за счёт увеличения сердечного выброса. Вазодилятирующий эффект связан со стимуляцией дофаминэргических DA1 -рецепторов, расположенных на мембране гладкомышечных клеток сосудов, а также DA2 -рецепторов пресинаптической мембраны. Стимуляция последних ингибирует пресинаптическое высвобождение норадреналина нейронами симпатической нервной системы, что способствует вазодилятации.
2. Доза 5,0-15,0 мкг/кг/мин – «инотропная» доза, при которой эффект препарата обусловлен стимуляцией b - адренорецепторов. b1 -стимуляция приводит к повышению сократимости миокарда и увеличению ЧСС, причём ЧСС увеличивается в большей степени, чем при использовании добутамина. b1 -стимуляция дополнительно способствует вазодилятации.
3. Доза > 15,0 мкг/кг/мин. Доминирует мощное сосудосуживающее действие, обусловленное стимуляцией a-адренорецепторов. Препарат также вызывает высвобождение норадреналина. Применение этой дозы нецелесообразно.
Расчет дозы. 800 мг препарата (содержимое 4 ампул допамина по 200 мг в каждой) растворяется в 500 мл 5% раствора глюкозы. 1 мл смеси содержит 1,6 мг препарата. Для более точного дозирования лучше всего использовать педиатрические микрокапельные дозирующие системы (1 мл=60 микрокапель). При этом 1 микрокапля содержит 26,7 мкг допамина. По таблице производят перечёт мкг/кг/мин в микрокапли/мин. При использовании обычной системой (1 мл=20 капель) скорость введения (микрокапли/мин) следует разделить на 3.
Инотропные средства. При низком сердечном выбросе к инфузии дофамина или норадреналина добавляют добутамин, 5-20 мкг/кг/мин.
К побочным реакциям вышеперечисленных препаратов относят эктопические нарушения ритма, тошноту и рвоту и иногда тахикардию. Они обычно нивелируются при уменьшении дозы препарата.
Эффективность кортикостероидов для выведения больных из самого инфекционно -токсического шока в настоящее время не доказана , хотя, возможно, какое-то положительное действие на биологические мембраны они могут оказать. В частности, в литературе имеются указания на то, что выработка NO может замедляться или исчезать под влиянием глюкокортикостероидов. Тем не менее при всех видах шока применяют ГКС, обычно преднизолон в дозе 5-10-20 мг/кг/сут.
Экспериментальные методы: применение больших доз налоксона, НПВП, моноклональных антител к эндотоксинам и фактору некроза опухолей, антагонистов рецепторов
8-09-2015, 20:45
