На основании проведенных популяционных исследований были выявлены этнические особенности в патогенезе и клиническом течении туберкулеза [Хаудамова Г.Т., 1991; Хоменко А.Г., 1996; SteadW.W., 1992; BellamyR., 1998]. Анализ заболеваемости туберкулезом органов дыхания основных этнических групп Казахстана (казахов и русских) выявил повышенный риск (в 3 раза) заболевания коренного населения [Хауадамова Г.Т., 1991].
Вероятно, большая часть такой этнически зависимой предрасположенности обусловлена факторами внешней среды, то есть определенными традициями данной популяции, экономическими причинами и т. д. Однако имеются данные о том, что более подвержены туберкулезу популяции, происходящие с территорий свободных от этого заболевания [BellamyR., 1998; SteadW.W., 1992]. Данное положение легко объяснимо с точки зрения естественного отбора. Резистентность к туберкулезной инфекции создавалась и поддерживалась в процессе симбионтных отношений макро- и микроорганизмов [Земскова З.С., Дорожкова И.Р., 1984].
С целью разделения генетических и средовых эффектов и оценки их соотносительного вклада в этиологию и патогенез туберкулеза были предприняты близнецовые исследования [Kallman F., Reisner D., 1943; Comstock G.W., 1978; FineP.E.M., 1981]. Эти работы показали, что заболеваемость туберкулезом монозиготных близнецов в среднем в 3,5 раза выше, чем дизиготных.
Полученные в ходе близнецовых исследований факты свидетельствовали о генетической подоплеке туберкулеза, однако, не предоставили данных о типе наследования заболевания. Генетический анализ восприимчивости и резистентности к туберкулезу, проведенный на лабораторных животных, показал, что наследование этих признаков носит сложный, полигенный характер [LurieM.B. etal., 1952; LynchC.J. etal., 1965].
На основании экспериментальных исследований была выдвинута гипотеза мультифакториального типа наследования предрасположенности к туберкулезу легких [Мороз А. М., Торонджадзе В. Г., 1977]. Позднее Б. А. Березовский и соавт. (1986) сравнили имеющиеся сведения по генетике туберкулеза с критериями мультифакториального наследования, предложенными J.H. Edwards (1969). Полученные в ходе сравнения результаты подтвердили высказанную ранее гипотезу.
С генетической точки зрения, мультифакториальные заболевания представляют результат сложного взаимодействия большого числа генов с разнообразными факторами окружающей среды. В отличие от менделирующей патологии, в основе которой лежат редко встречаемые "главные гены", но со значительными эффектами, при мультифакториальных болезнях генетическая система полигенов представлена огромным числом аллельных вариантов генов, эффекты которых в отдельности незначительны. Однако их совокупное действие формирует неблагоприятный "генетический фон", который под влиянием дополнительных факторов реализуется в патологический фенотип [Пузырев В. П., 2003].
Современные представления о генетической составляющей мультифакториальных заболеваний во многом связаны с концепцией подверженности и порогового проявления мультифакториального фенотипа [Falconer D., 1965; Edwards J.H., 1969]. Согласно этой концепции, подверженность к заболеванию наследственно обусловлена, но реализация ее возможна только при взаимодействии с факторами среды. Патологический фенотип проявляется при пересечении некоего "порога" подверженности, описываемого количественными признаками. Порог подразумевает наличие резкого качественного различия: за этим порогом на шкале подверженности располагаются пораженные индивиды [Фогель Ф., Мотульски А., 1989].
Развитие молекулярно-генетических технологий позволило решить проблему идентификации конкретных генетических систем, ответственных за предрасположенность к мультифакториальным заболеваниям. Картирование генов осуществляется в рамках двух стратегий: генов-кандидатов и позиционного клонирования [Пузырев В.П., Степанов В.А., 1997].
Ген определяется как кандидатный, если продукт его экспресии вовлечен в развитие болезни. Анализ ассоциации полиморфизма генов-кандидатов с изучаемой болезнью или патологическими признаками позволяет установить их патогенетическую роль и, таким образом, "картировать" ген заболевания. При позиционном клонировании определение генов подверженности проводится путем анализа сцепления заболевания и маркерами с установленным положением на хромосоме. Это дает возможность картировать болезни, для которых не известны не только гены-кандидаты, но даже детали развития болезни.
Идентификация генов и их аллелей, от экспресии которых зависит чувствительность или резистентность к туберкулезу позволила бы глубоко проникнуть в фундаментальные механизмы иммунитета и патологии этой инфекции. В результате появилась бы возможность использовать методы генетического типирования для выявления среди здоровых людей групп с генетически повышенным риском заболевания, требующих первоочередных мер профилактики и, вероятно, особого подхода к вакцинации [Кобринский Б.А., 1987].
Сложность патогенеза, а так же различия в клиническом проявлении туберкулеза предполагают, что число генов-кандидатов заболевания достаточно велико (табл. 1). При этом вклад каждого из них в суммарную подверженность различен [HillA.V.S., 1998]. Дело еще более осложняется действием факторов внешней среды, значительно модифицирующих положение порога подверженности туберкулезу. Кроме того, большое значение для определения генов сложнонаследуемых заболеваний имеет также выбор популяции для исследования. Индивидуальные сочетания аллелей генов предрасположенности, формирующие риск заболевания, являются уникальными для каждой популяции, что может быть одной из причин невоспроизводимости в разных выборках результатов анализа сцепления болезни с маркером [TerwilligerJ.D. etal., 1997].
Таким образом, само по себе картирование генов туберкулеза еще не исчерпывает все проблемы генетики данной патологии. Следующим за картированием шагом, по-видимому, является изучение совместного действия комплекса генов предрасположенности, выявление его основных функциональных звеньев, установление особенностей взаимодействия с факторами негенетической природы – вот задачи, которые необходимо решить для понимания механизмов нормальной и патологической реализации генетической информации.
Таблица 1 Гены-кандидаты подверженности туберкулезу
| Ген | Хромосомная локализация (MIM) |
Название белкового продукта | Функция белка |
| NRAMP1 | 2q35 (600266) | Макрофагальный протеин 1, ассоциированный с естественной резистентностью | Транспорт двухвалентных ионов металлов, киллинг внутриклеточно расположенных МБТ |
| VDR | 12q12-q14 (601769) |
Рецептор к витамину D | Связывание с витамином D, активация клеточного иммунитета |
| IL1А, IL1В | 2q14(147760) 2q14(147720) |
Интерлейкин 1a Интерлейкин 1b |
Активация клеточного иммунного ответа |
| IL12В | 5q31.1-q33.1 (161561) |
Интерлейкин 12 b | Индукция синтеза IFN-g |
| IFNG | 12q14 (147570) |
Интерферон g | Активация Т-лимфоцитов, макрофагов |
| TNFА | 12р13.2 (191190) |
Фактор некроза опухолей a | Индукция формирования гранулемы |
| NOS2 | 17р13.1-q25 (600719) |
Индуцибельная синтаза оксида азота | Цитотоксическое действие |
| MBP | 10q11.2-q21 (154545) |
Маннозо-связывающий белок | Активация системы комплемента |
| HLA | 6p21.3 (142860) |
Главный комплекс гистосовместимости | Регуляция силы иммунного ответа |
| IL1RN | 2q14.2 (147679) |
Антагонист рецептора к интерлейкину-1 | Угнетение провоспалительного эффекта |
| IL12R | 19p113.1 (601604) |
Рецептор к интерлейкину 12 | Связывание интерлейкина 12 на поверхности клеток-мишеней |
1.2 Молекулярные механизмы патогенеза туберкулеза у человека
Туберкулез – хроническое инфекционное заболевание, протекающее с внутриклеточным (в макрофагах) паразитированием микобактерий [MyrvikQ. N. etal., 1984]. Несмотря на самую современную химиотерапию, лечение туберкулеза, как правило, бывает длительным и не всегда эффективным. Одной из причин безуспешного лечения данной инфекции по общепринятому мнению является недостаточная эффективность защитных механизмов макроорганизма, в значительной мере генетически обусловленных. Сведения об участии иммунной системы, складывающихся межклеточных взаимодействиях, накопленные за последние десятилетия, изменили (уточнили) представления о патогенезе туберкулеза.
Туберкулез чаще всего развивается в результате заражения МБТ, которые выделяет в окружающую среду больной человек. Респираторный тракт, а так же кишечник являются входными воротами инфекции. Таким образом, основной путь проникновения патогена – аэрогенный, но возможен и алиментарный. Определенную роль при аэрогенном заражении играет система мукоцилиарного клиренса, позволяющая вывести попавшие в бронхи частицы пыли, капельки слизи, слюны, мокроты, содержащие микроорганизмы. Аналогичным образом, при алиментарном пути проникновения микобактерий защитную роль играет переваривающая функция желудочно-кишечного тракта.
После проникновения патогена в легкие важную роль в защите от инфекции играют альвеолярные макрофаги. Эти клетки непосредственно подавляют рост бактерий, фагоцитируя их, а также они участвуют в реакциях клеточного противотуберкулезного иммунитетах [Авербах М.М. и др., 1982; Литвинов В.И. и др., 1983; MyrvikQ. N. etal., 1984].
Процесс фагоцитоза можно разделить на несколько следующих друг за другом этапов. В первую очередь бактерия прикрепляется к фагоциту, затем следует фаза поглощения микроорганизма, и как следствие ингибиция роста или уничтожение инфекта.
Процесс прикрепления микобактерий к фагоцитам осуществляется посредством рецепторов комплемента, маннозных рецепторов и других рецепторов клеточной поверхности макрофага. Взаимодействие между маннозными рецепторами и инфектом происходит при помощи гликопротеина клеточной стенки микобактерий, имеющего маннозный остаток на обращенной во внешнюю среду части молекулы [SchlesingerL. S., 1996].
Мутации генов, белковые продукты которых вовлечены в механизмы иммунологической защиты, определяют степень резистентности к инфекциям. Маннозо-связывающий белок (МВР) является Са-зависимым белком плазмы крови. Выявлено, что у человека этот белок осуществляет функцию активатора системы комплемента, кроме того, он действует непосредственно как опсонин, взаимодействуя с рецепторами макрофагов [HillA.V.S., 1998].
Исследовали взаимосвязь полиморфизма гена МВР с чувствительностью к легочному туберкулезу в Индии. Анализ показал, что с туберкулезом ассоциированы три точечных замены в исследуемом гене [SelvarajP. etal., 1999]. Аналогичное исследование, проведенное в Гамбии, выявило связь полиморфных вариантов данного гена с развитием легочной формы туберкулеза [BellamyR. etal., 2000].
Фагоцитирующая клетка выбрасывает окружающие микроорганизм псевдоподии, которые затем сливаются на периферии, образуя окруженную мембраной вакуоль [Ерохин В.В., 1974; LeakeE.S., MyrvikQ.N., 1971]. Микобактерии, находящиеся в фагосоме попадают под воздействие целого ряда неблагоприятных факторов, направленных на их уничтожение. К таким факторам можно отнести слияние фагосомы с лизосомами, содержащими литические ферменты [JeckettP. S. etal., 1978]. Так же макрофаг способен производить реактивные радикалы кислорода и азота, играющие, вероятно, основную роль в уничтожении инфекта внутри макрофага [NelsonN., 1999]. Установлено, что "нокаутированные" по гену индуцибельной синтазы оксида азота (NOS2) мыши не способны противостоять туберкулезной инфекции, у них наблюдался усиленный рост M. tuberculosis в легких, селезенке и печени. Макрофаги этих мышей не производили NO и инфекция распространялась [JackettP. S. etal., 1978; WalkerL., LowrieD. B., 1981].
Если макроорганизм не в состоянии устранить внутриклеточно размножающихся микобактерий, то в результате хронического воспаления в месте освобождения антигенов происходит скопление большого числа макрофагов, которые выделяют фиброгенные факторы и стимулируют образование грануляционной ткани и фиброза. Возникшая гранулома представляет собой попытку организма ограничить распространение персистирующей инфекции. Однако при интенсивном размножении микобактерий в организме человека и малоэффективном фагоцитозе выделяется большое количество токсичных веществ и индуцируется гиперчувствительность замедленного типа (ГЗТ), которая способствует выраженному экссудативному компоненту воспаления с развитием казеозного некроза. В процессе разжижения казеозных масс микобактерии получают возможность бурного внеклеточного размножения, что обусловливает прогрессирование туберкулеза [Ройт А., 1991, 2000].
Важную роль в противотуберкулезной защите играет, секретируемый макрофагами и моноцитами цитокин – фактор некроза опухолей (TNFa). Он принимает участие в индукции формирования гранулемы, а так же способствует активации Т-клеток, тем самым повышая антибактериальную активность макроорганизма [KindlerV. etal., 1989; MohanV. P. etal., 2001]. На модели мышей с "нокаутированным" геном, кодирующим рецептор для TNFa, продемонстрировано существенное значение фактора некроза опухолей для выживания в условиях туберкулезной инфекции [FlynnJ. L. etal., 1995]. В настоящее время известно несколько мутаций гена TNFА, находящегося в локусе главного комплекса гистосовместимости, однако их связь с туберкулезом не выявлена. Так, в небольшом исследовании, проводившемся в Гамбии, не обнаружили ассоциации полиморфизма 308G/A гена TNFА с клинически подтвержденным туберкулезом. Такой же результат был получен при поиске взаимосвязи полиморфизма гена TNFА c туберкулезом в Бразилии [KnightJ. C., KwiatkowskiD., 1999].
При поиске конкретных генетических систем, отвечающих за развитие восприимчивости или резистентности к туберкулезу, в первую очередь обращалось внимание на главный комплекс гистосовместимости человека – HLA-систему, в которой расположены гены иммунного ответа. При этом продукты данного комплекса – антигены HLA – выступали в качестве биологических маркеров. Результаты анализа ассоциаций аллелей HLA-комплекса с туберкулезом показали связь DR-локуса с заболеванием, к тому же выявили высокую рассовую и этническую специфичность. В русской популяции заболевание ассоциировалось с В5, В14 и В17 антигенами HLA-комплекса [Хоменко А.Г., 1996]. Вероятно, гены комплекса HLA оказывают влияние на восприимчивость к туберкулезу, регулируя силу иммунного ответа и обуславливая этнические различия в подверженности ТБ.
Также была выявлена ассоциативная взаимосвязь ряда генетических маркеров – фенотипов крови с возникновением туберкулеза и с характером уже возникшего заболевания. Анализировали распределение фенотипических и генных частот 9 генетических локусов белков крови: ингибитора протеаз, трансферрина, фосфоглюкомутазы 1, кислой эритроцитарной фосфотазы 1, гаптоглобина, витамин-Д-транспортирующего белка, глиоксалазы 1, комплемента и эстеразы Д. При этом выявили существование различий между больными туберкулезом легких и практически здоровыми людьми. Эти различия выражаются в накоплении у больных туберкулезом одних фенотипов и в уменьшении частот других фенотипов. Следует отметить, что полученный эффект касался в основном одних и тех же 6 белковых локусов, что подтверждает их реальное значение в дифференциации между больными ТБ и здоровыми людьми [Богадельникова И.В., 1999].
С целью картирования генов предрасположенности к туберкулезу группа исследователей провели широкомасштабное сканирование генома с использованием 299 высокоинформативных ДНК – маркеров у 173 пар сибсов, полностью конкордантных по развитию туберкулеза [BellamyR. etal., 2000]. При этом выявили 2 локуса предрасположенности – на длинных плечах хромосомы 15 и Х [CervinoA.C.L. etal., 2002].
На основании экспериментальных исследований, проведенных А.М. Морозом и В.Г. Торонджадзе (1977), были выявлены две линии мышей, оппозитные по своей чувствительности к туберкулезной инфекции. У резистентных линий после внутривенного заражения микобактериями туберкулеза наблюдаются длительный латентный период и медленное развитие инфекционного процесса, выражающееся в персистенции микобактерий на фоне незначительных гранулематозно измененных тканей, не приводящих к гибели животных. В то же время заражение мышей чувствительной линии приводит к быстрому размножению микобактерий в тканях, образованию гранулем в легких, селезенке, печени и быстрой гибели животных [Авербах М.М. и др., 1980; Мороз А. М., 1984]. На этих линиях исследователи изучили некоторые механизмы естественной резистентности и приобретенного иммунитета и высказали предположение, что устойчивость к инфекциям во многом зависит от способности макрофагов подавлять рост микобактерий в своей цитоплазме. Проведенные позднее эксперименты на 60 мышах двух линий, одна из которых чувствительна, другая устойчива к туберкулезной инфекции, полностью подтвердили данное предположение [Ельшанская М. П. и др., 1985].
Важнейший этап патогенеза туберкулеза - персистенция возбудителя в фагосомах макрофагов. Макрофаги поглощают патоген в очагах воспаления, но часто теряют способность элиминировать его в лизосомах, что в итоге приводит к их массированному внутриклеточному размножению и последующему выходу из погибших клеток. Получены данные, свидетельствующие о том, что имеются существенные различия в судьбе фагосом, содержащих вирулентные и авирулентные микобактерии, поскольку только первые препятствуют их слиянию с лизосомами [MyrvikQ. etal., 1984; FrenkelG. etal., 1986].
С точки зрения развития новых подходов к лечению туберкулеза очевидна необходимость контроля прохождения микобактерий по эндосомально-лизосомальному пути: от ранней эндосомы - к поздней, от поздней эндосомы – к лизосоме.
1.3 Физиологические функции белковых продуктов генов-кандидатов подверженности туберкулезу, их роль в патогенезе заболевания
Одним из генов предрасполагающих к развитию туберкулеза является NRAMP1 (от англ. Natural-Resistance-Associated Macrophage Protein 1 gene – ген макрофагального протеина 1, ассоциированного с естественной резистентностью). Более того, R. Bellamy и соавт. (1998) отнесли NRAMP1 к основным кандидатным генам туберкулеза у человека. Белковый продукт этого гена имеет вес около 60 кД, он локализован в лизосомальном компартменте покоящегося макрофага, но во время фагоцитоза он работает на мембране фагосомы [GruenheidS. etal., 1997]. Nramp1 участвует в процессах активации макрофагов, являясь ключевым звеном в механизме транспорта нитритов из внутриклеточных компартментов в более кислую среду фаголизосомы, где он способен вступать в химическую реакцию с образованием NO [BlackwellJ. M., SearleS., 1999].
Белок входит в семейство функционально связанных мембранных белков (к этому семейству относят также Nramp2), ответственных за транспорт двухвалентных катионов, таких как Fe2+ , Mn2+ , Zn2+ , Cu2+ [JabadoN. etal., 2000; CellierM. etal., 2001].
Известно, что ионы металлов являются жизненно важными элементами, участвующими во многих метаболических реакциях, происходящих в каждой живой клетке. Следовательно, недостаток, избыток или отсутствие данных элементов может привести к развитию какого-либо патологического состояния или даже к гибели клетки. Постоянство ионов металлов в организме обеспечивается регуляцией их потребления, хранения и выведения. Для того чтобы поддерживалась необходимая концентрация ионов, каждая клетка обладает определенной системой, обеспечивающей транспорт веществ через мембрану. Сбой этой системы или ее части может повлечь за собой потерю равновесия между выведением и поступлением веществ, что приведет к изменению внутриклеточной концентрации ионов. Недостаточный транспорт ионов может оказаться причиной нехватки жизненно важных метаболических элементов, а чрезмерное их накопление может вызвать токсическое воздействие этих же веществ, ведущее к гибели клетки. Возможно, что антибактериальная функция Nramp1 заключается в создании неблагоприятной для бактерии окружающей среды внутри фагосомы [GruenheidS. etal., 2000; BartonC.H. etal, 1999].
Во время фагоцитоза микроба макрофаг продуцирует активные кислородные метаболиты, которые являются токсичными для бактерии. Выживание патогена во время кислородозависимой перестройки метаболизма фагоцита обеспечивается микробными ферментами, большинство из которых содержат ионы металлов в своих активных центрах [CellierM. etal., 1994].
В свою очередь истощение запаса ионов металлов в фагосоме, вызванное транспортной деятельностью макрофагального белка ассоциированного с естественной резистентностью, приводит к снижению продукции металлосодержещих ферментов поглощенной бактерией.
Следовательно, дефекты продукции или функции Nramp1 могут приводить к нарушению его транспортной функции и, как следствие, к повышению чувствительности к внутриклеточным патогенам, таким как микобактерии (рис. 1) [BartonC.H. etal., 1999].
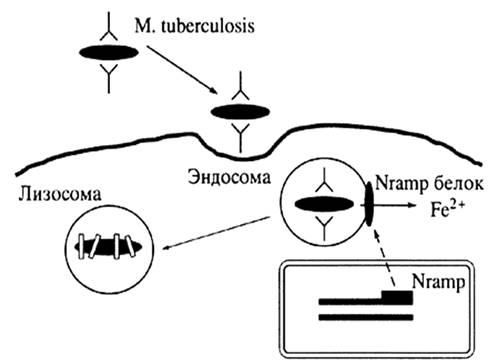
Рис. 1. Схема антибактериального действия NRAMP1 [по Пальцеву М.А., 2002]
Опыты, проведенные на инбредных мышах, показали, что уровень естественной резистентности к внутривенному заражению низкими дозами M. bovis (BCG) контролируется одним геном, локализованным в проксимальном регионе мышиной хромосомы 1. Этот локус обозначили как Bcg (также он известен как Lsh или Ity). Два различных фенотипа Bcg были ассоциированны с чувствительностью (Bcg-s) и с резистентностью (Bcg-r) на ранней стадии инфекции, вызванной M. bovis, M. avium, M. lepraemurium, Leishmaniadonovani, Salmonellatyphimurium [BredleyD.J., 1977; ForgetA. etal., 1981].
Экспериментальные исследования показали, что через 3 недели после заражения 10 КОЕ M. bovis (BCG) из селезенки мышей Bcg-s высевается на 3-4 порядка больше микобактерий, чем из селезенки мышей Bcg-r [GrosP. etal., 1981].Результаты исследований на моделях мышей позволили утверждать, что высокая чувствительность линий мышей
8-09-2015, 21:48
