


 1.
ЛИТЕРАТУРНЫЙ
ОБЗОР
1.
ЛИТЕРАТУРНЫЙ
ОБЗОР
1.1. Теоретические основы разрабатываемого процесса
 1.1.1.
Общие сведения
о процессе
ректификация
1.1.1.
Общие сведения
о процессе
ректификация
Ректификация представляет собой процесс многократного частичного испарения жидкости и конденсации паров. Процесс осуществляется путем контакта потоков пара и жидкости, имеющих различную температуру, и проводится обычно в колонных аппаратах. При каждом контакте из жидкости испаряется преимущественно легколетучий, или низкокипящий, компонент (НК), которым обогащаются пары, а из паров конденсируется преимущественно труднолетучий, или высококипящий, компонент (ВК), переходящий в жидкость. Такой двухсторонний обмен компонентами, повторяемый многократно, позволяет получить в конечном счете пары, представляющие собой почти чистый НК. Эти пары после конденсации в отдельном аппарате образуют дистиллят (ректификат) и флегму – жидкость, возвращаемую для орошения колонны и взаимодействия с поднимающимися парами. Пары получают путем частичного испарения снизу колонны остатка, являющегося почти чистым ВК.
Как отмечалось, достаточно высокая степень разделения однородных жидких смесей на компоненты может быть достигнута путем ректификации. Сущность процессов, из которых складывается ректификация, и получаемые при этом результаты можно проследить с помощью t — х — у -диаграммы (рис. 1.1).
Нагрев исходную смесь состава х1 до температуры кипения получим находящийся в равновесии с жидкостью пар (точка b). Отбор и конденсация этого пара дают жидкость состава x2 обогащенную НК (х2 > х1).Нагрев эту жидкость до температуры кипения t2, получим пар (точка d), конденсация которого дает жидкость с еще большим содержанием НК, имеющую состав ха, и т. д. Проводя таким образом последовательно ряд процессов испарения жидкости и конденсации паров, можно получить в итоге жидкость (дистиллят), представляющую собой практически чистый НК.
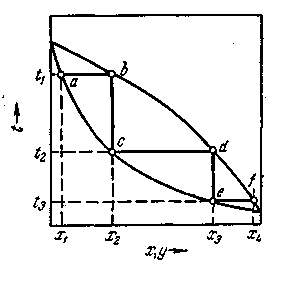
Рис. 1.1. Изображение процесса разделения бинарной смеси путем ректификации на диаграмме t—Х—у.
Аналогично, исходя из паровой фазы, соответствующей составу жидкости x4, путем проведения ряда последовательных процессов конденсации и испарения можно получить жидкость (остаток), состоящую почти целиком из ВК.
В простейшем виде процесс многократного испарения можно осуществить в многоступенчатой установке, в первой ступени которой испаряется исходная смесь. На вторую ступень поступает на испарение жидкость, оставшаяся после отделения паров в первой ступени, в третьей ступени испаряется жидкость, поступившая из второй ступени (после отбора из последней паров) и т. д. Аналогично может быть организован процесс многократной конденсации, при котором на каждую следующую ступень поступают для конденсации пары, оставшиеся после отделения от них жидкости (конденсата) в предыдущей ступени.
При достаточно большом числе ступеней таким путем можно получить жидкую или паровую фазу с достаточно высокой концентрацией компонента, которым она обогащается. Однако выход этой фазы будет мал по отношению к ее количеству в исходной смеси. Кроме того, описанные установки отличаются громоздкостью и большими потерями тепла в окружающую среду.
Значительно более экономичное, полное и четкое разделение смесей на компоненты достигается в процессах ректификации, проводимых обычно в более компактных аппаратах — ректификационных колоннах.
Процесс ректификации осуществляется путем многократного контакта между неравновесными жидкой и паровой фазами, движущимися относительно друг друга.
При взаимодействии фаз между ними происходит массо- и теплообмен, обусловленные стремлением системы к состоянию равновесия. В результате каждого контакта компоненты перераспределяются между фазами: пар несколько обогащается НК, а жидкость — ВК. Многократное контактирование приводит к практически полному разделению исходной смеси.
Таким образом, отсутствие равновесия (и соответственно наличие разности температур фаз) при движении фаз с определенной относительной скоростью и многократном их контактировании являются необходимыми условиями проведения ректификации.
1.1.2. Равновесие в системах жидкость-пар
В общем случае жидкая смесь может состоять из нескольких компонентов. В простейшем случае из двух, например из компонентов А и В. Характер поведения жидкой смеси зависит главным образом от природы составляющих ее веществ и давления.
Для идеальных растворов характерно то, что сила взаимодействия между всеми молекулами (одноименными и разноименными) равна. При этом общая сила, с которой молекула удерживается в смеси, не зависит от состава смеси. Очевидно, что парциальное давление в этом случае должно зависеть лишь от числа молекул, достигающих в единицу времени поверхности жидкости со скоростью, необходимой для преодоления сил внутреннего притяжения молекул, т. е. при данной температуре давление соответствующего компонента возрастает пропорционально его содержанию в жидкой смеси (закон Рауля):
рА = РАхА (1.1) и рВ = РВ(1-хА) (1.2.)
Закон Рауля справедлив и для газов с температурой ниже критической (т. е. такой температуры, выше которой газ при увеличении давления не сжижается).
По степени растворимости компонентов смеси жидкости подразделяют на взаиморастворимые в любых соотношениях, частично растворимые и практически взаимонерастворимые. В свою очередь смеси со взаиморастворимыми компонентами в любых соотношениях делятся на: идеальные растворы, которые подчиняются закону Рауля; так называемые нормальные растворы - жидкие смеси, частично отклоняющиеся от закона Рауля, но не образующие смесей: с постоянной температурой кипения (азеотропов); неидеальные растворы - жидкости со значительными отклонениями от закона Рауля, в том числе смеси с постоянной температурой кипения (азеотропы). (Отметим, что полностью взаимонерастворимых жидкостей нет, обычно все жидкости хотя бы в незначительных количествах, но растворяются друг в друге. Однако в этих случаях на практике для удобства принимают такие жидкости взаимонерастворимыми.)
Смесь двух жидкостей, взаиморастворимых в любых соотношениях, представляет собой систему, состоящую из двух фаз и двух компонентов, и по правилу фаз:
С=К-Ф+2=2-2+2=2 (1.3.)
имеет две степени свободы (из трех - давления Р, температуры t, концентрации х). Однако при анализе и расчете процессов перегонки жидкостей одну из переменных обычно закрепляют и строят диаграмму фаз в плоской системе координат. При этом возможны следующие варианты фазовых диаграмм: Р — t (х = const), Р — — x(t = const), t — х(Р = const).
Для технических расчетов наиболее важной является диаграмма t — х, у, так как обычно процессы перегонки в промышленных аппаратах протекают при Р = const, т. е. в изобарных условиях. На этой диаграмме (рис. 5.2.) по оси абсцисс отложены концентрации жидкой х и паровой у фаз, отвечающие различным температурам.
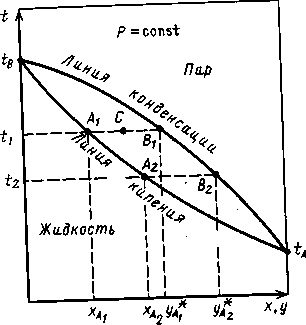
Рис. 1.2. Фазовая диаграмма t — х, у
По закону Дальтона рА = Рy*A, и тогда
y*A= pA/P=(PA/P) xA, (1.4.)
но
Р = pA+pB=PAxA+PB(1-xB)=PB+(PA-PB)xA (1.5.)
тогда
xA=(P-PB)/(PA-PB) (1.6.)
По уравнению (1.6.)) по известным РА и РB при заданной температуре t1 , t2 и т.д. находят хA , хB и т.д., а затем по уравнению (1.4.) -соответствующие значения у*A1 , у*А2 и т.д. и по найденным точкам строят линии кипения жидкости (кривая tAA2A1tB) и конденсации паров (кривая tAB2BltB). Отметим, что уравнение (1.6.) устанавливает связь между концентрациями (по жидкости) и заданными давлениями (общим Р и насыщенных паров РА и РB). Отрезки А1В1 , А2 В2 и т. д., соединяющие точки равновесных составов жидкой и паровой фаз, являются изотермами.
Отметим, что точки, лежащие на кривой tAA2A1tB,, отвечают жидкой фазе, находящейся при температуре кипения. Очевидно, что любая точка, лежащая ниже этой кривой, характеризует систему, состоящую только из жидкой фазы. Аналогично, любая точка лежащая выше кривой tA B2 В1 tB , характеризует систему, темпера тура которой выше температуры начала конденсации пара, т. е пары в этой точке являются перегретыми, и система состоит только из паровой фазы. Точки, находящиеся между кривыми кипения и конденсации (например, точка С на рис. 1.2.), характеризуют системы, температуры которых выше температуры кипения жидкости данного состава и ниже температуры конденсации паров этого же состава. Таким образом, эти точки отвечают равновесным парожидкостным системам.
Основные положения фазового равновесия были рассмотрены в гл. 2 (правило фаз Гиббса, законы Генри и Рауля и др.). Там же для идеальных бинарных систем получено уравнение (1.7.), которое описывает линию равновесия:
у*А = ахА/[1+хА(а-1)], (1.7.)
где а = РА/РВ - относительная летучесть компонента А (иногда а называют коэффициентом разделения).
Очевидно, что для смеси, состоящей из n компонентов, например, А, В, С, D, на основе законов Рауля и Дальтона имеем
yA = (РA/Р)хA; yB = (РB/Р)хB; yC = (РC/Р)хC; yD = (РD/Р)хD. (1.8.)
Поскольку
P=PAxA+
PBxB+
PCxC+
PDxD+
…=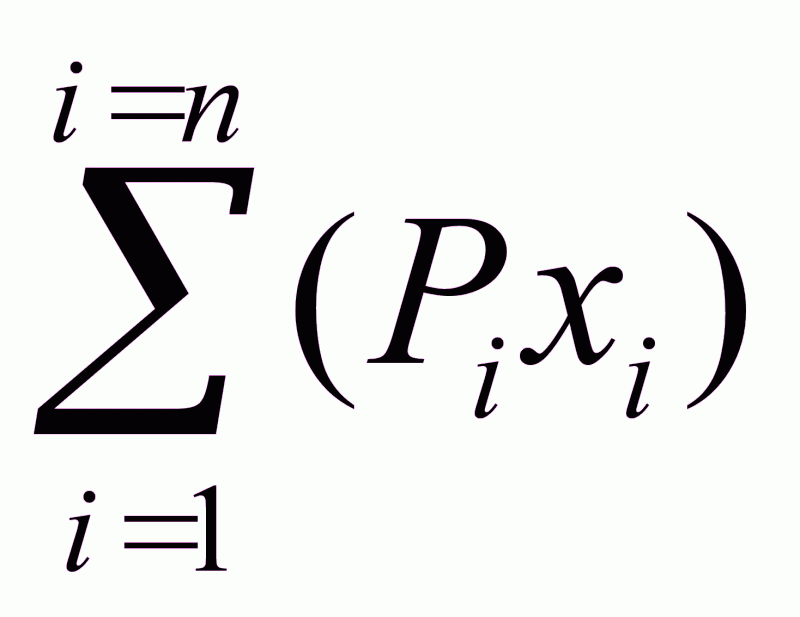 (1.9.)
(1.9.)
то для любого j-го компонента
yj
= PjXj/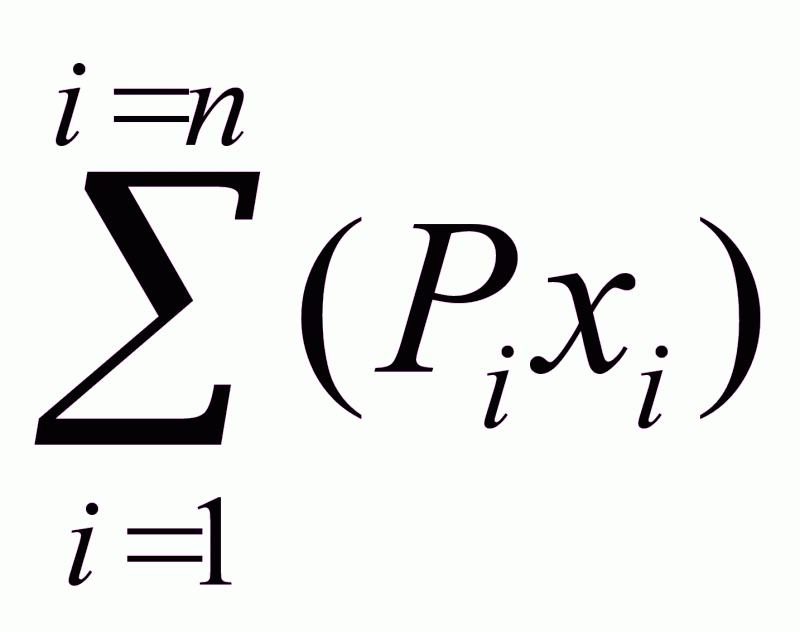 .
(1.10.)
.
(1.10.)
Разделив числитель и знаменатель правой части уравнения (1.10) на величину РА, получим
yj
= а
jXj/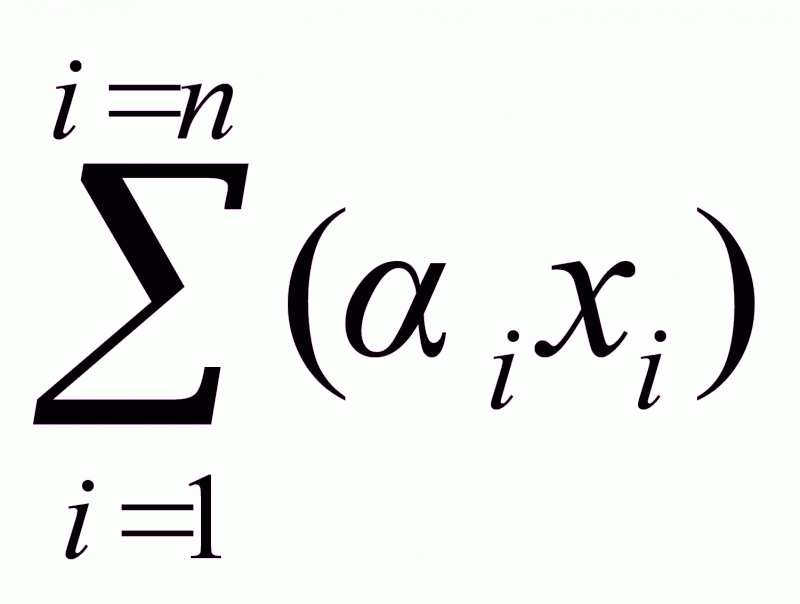 ,
(1.11.)
,
(1.11.)
где а A = РА/РВ ; а в = РВ/РА ; а C = РС/РА и т. д.
Например, зависимость давления насыщенного пара от температуры хорошо описывается эмпирическим уравнением Антуана
lnРА = А - В/(Т+ C), (1.12.)
где А - постоянная, не зависящая от температуры; В и С -константы, определяемые по справочникам; T- абсолютная температура.
Уравнение (5.12) описывает температурную зависимость давлений паров в интервале температур до нескольких десятков градусов и при давлениях, не слишком близких к критическим.
Взаимное положение кривых на фазовых диаграммах t — х — у и у — х как для идеальных, так и для реальных систем могут быть определены с помощью законов Коновалова. Законы Коновалова устанавливают связи между изменениями состава, давления или температуры в двухфазных системах, они лежат в основе теории перегонки и ректификации бинарных смесей.
Первый - закон Коновалова формулируется так: пар обогащается тем компонентом, при добавлении которого к жидкости повышается давление пара над ней или снижается ее температура кипения, или пар всегда более обогащен НК, чем соответствующая ему равновесная жидкая фаза.
Первый закон Коновалова дополняется первым правилом Вревского, отражающим влияние температуры на равновесные составы фаз: при повышении температуры бинарной смеси в парах возрастает относительное содержание того компонента, парциальная молярная теплота испарения которого больше.
Это можно проиллюстрировать с помощью фазовой диаграммы (рис. 1.2.). Для идеальной смеси очевидно, что при одной и той же температуре t содержание НК в парах у*A1 (точка B1 больше его содержания ха в равновесной с парами жидкости (точка А1). При добавлении к смеси НК ее температура кипения снижается, но содержание НК в паре остается выше, чем в жидкости.
Реальные
жидкие смеси
могут значительно
отклоняться
от закона Рауля.
Если зависимость
полного давления
(или сумма
парциальных
давлений) паров
от состава
жидкой смеси
проходит выше
линий, характеризующих
те же зависимости
для идеальных
смесей (рис.
1.3.), то такое отклонение
называют
положительным,
если
ниже - отрицательным
отклонением
от
закона Рауля.
Эти отклонения
определяются
изменением
активности
молекул в растворе,
диссоциацией,
гидратацией
и др. Степень
отклонения
реальной системы
от закона Рауля
выражают величиной
коэффициента
активности
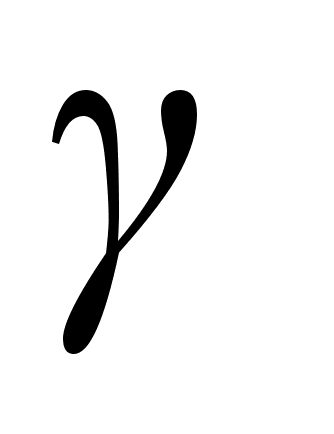 :
:
pA
= PAxA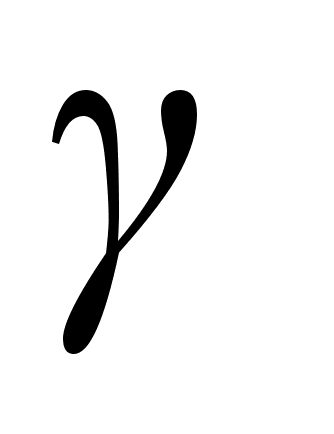 . (1.13.)
. (1.13.)
Для смесей
с положительным
отклонением
от закона Рауля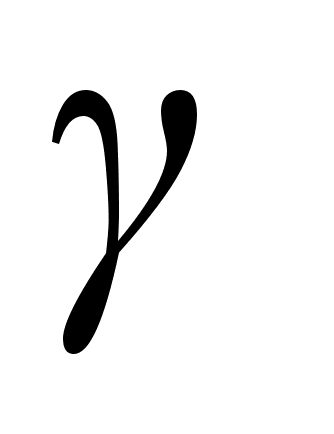 > 1, для смесей
с отрицательным
отклонением
—
> 1, для смесей
с отрицательным
отклонением
—
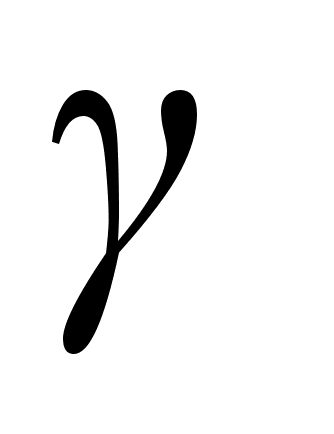 < 1. Отметим, что
определение
значений у
часто затруднительно,
поэтому диаграммы
P
— х
обычно
строят по
экспериментальным
(справочным)
данным.
< 1. Отметим, что
определение
значений у
часто затруднительно,
поэтому диаграммы
P
— х
обычно
строят по
экспериментальным
(справочным)
данным.
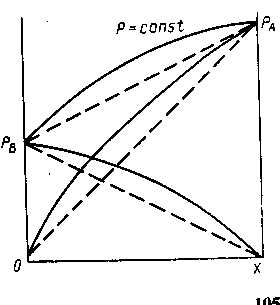
![]()
Рис. 1.3. Диаграмма р — х для смеси с положительным отклонением от закона Рауля (пунктиром показаны соответствующие линии для идеального раствора)
Для многих реальных смесей отклонение от закона Рауля настолько существенно, что приводит к качественно новому состоянию системы, а на фазовых диаграммах Р — х и t — х появляются (рис. 1.4.,б, в) относительный максимум или минимум. При этом кривые жидкости и пара соприкасаются друг с другом в экстремальных точках, в которых составы равновесных фаз одинаковы. Такие смеси, как известно, называют азеотропными, или азеотропами. Их основная особенность состоит в том, что при испарении такая смесь (азеотроп) не изменяет своего состава, поэтому для ее разделения требуются специальные методы (азеотропная и экстрактивная ректификация, изменение давления и др.).
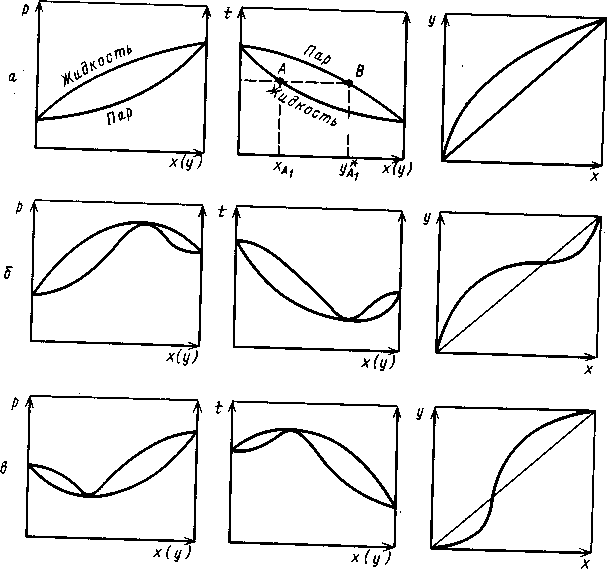
Рис. 1.4. Фазовые диаграммы равновесия жидкость-пар для идеальной (а) и реаль- ных (б, в) систем
Эта особенность азеотропных смесей постулируется вторым законом Коновалова, который можно сформулировать следующим образом: если давление и температура сосуществования двух бинарных фаз имеют экстремум (максимум или минимум), то составы фаз одинаковы. Это справедливо для фаз любой природы. Для систем жидкость - пар второй закон Коновалова определяет основное свойство азеотропов.
При изменении внешних условий - температуры (или давления) значение а изменяется различно по разные стороны от точки азеотропа; одна часть «рыбки» (рис.1.4., б, в) должна становиться шире, другая - уже. Очевидно, что в части диаграммы, где в паре содержится больше, чем в растворе, компонента с меньшей теплотой испарения, при понижении температуры (давления), а увеличивается.
5.1.3. Материальный и тепловой балансы ректификационной колонны
Пусть, согласно схеме на рис. (1.5.), в колонну поступает F кмоль исходной смеси, состав которой хF мол. долей НК. Сверху из колонны удаляется G кмоль паров, образующих после конденсации флегму и дистиллят. Количество получаемого дистиллята Р кмоль, его состав хP мол. долей НК. На орошение колонны возвращается флегма в количестве Ф кмоль, причем ее состав равен составу дистиллята (хф= xP мол. долей). Снизу из колонны удаляется W кмоль остатка состава xw мол. долей НК.
Тогда уравнение материального баланса колоны будет:
Ф+F = G+W. (1.14)
Поскольку G=P+Ф, то
F = P+W. (1.15.)
Соответственно по НК материальный баланс:
FxF = PxP+WxW (1.16.)
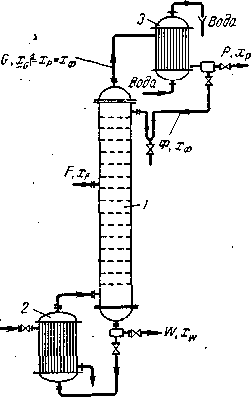
Рис. 1.5. К составлению материального баланса ректификационной колонны:
/ — колонна; 2 — куб; 3 — дефлегматор.
Для колонны непрерывного действия с учетом потерь тепла в окружающую среду имеем:
Приход тепла Расход тепла
С теплоносителем в кипя- С парами, поступающими из
тальнике .……… QКИП.. колонны в дефлегматор QG = GI
С исходной смесью……….QF=FiF С остатком………………… QW =Wiw
С флегмой ................. . QФ = ФiФ Потери в окружающую среду QП
Кроме известных величин, в выражения для количеств тепла входят: I, iF, iф и iw — энтальпии соответственно паров, выходящих из колонны, исходной смеси, флегмы и остатка.
Таким образом, уравнение теплового баланса:
Qкип + QF + QФ = QG + QW + QП . (1.17.)
Подставляя вместо Q их значения и учитывая, что F=Р + W, G = P(R+ 1) и Ф = PR, получим
Qкип + (Р + W)iF + РRiФ = P(R+)I + WiW + QП (1.18.)
Решая уравнение (5.18.) относительно Qкип, находим расход тепла в кипятильнике
Qкип = Р(I – iF) + PR( I -iФ) + W(iW - iF) + QП ( 1.18а. )
Из уравнения теплового баланса (5.18а.) видно, что тепло, подводимое в кипятильник, затрачивается на испарение дистиллята [Р(I—iF)], испарение флегмы [PR(I — iф)], нагревание остатка до температуры кипения [W(iw — iF)], а также на компенсацию потерь тепла в окружающую среду.
Флегма из дефлегматора поступает в колонну при температуре ее кипения. Поэтому энтальпия выходящих из колонны паров I == iФ + rф, где rф — теплота испарения флегмы.
Потери тепла в окружающую среду обычно выражают в долях тепла, подводимого в кипятильник, т. е. принимают QП = aПQкип, где при наличии хорошей тепловой изоляции коэффициент аП = 0,03—0,05.
Делая соответствующие подстановки в уравнение (1.18а.), окончательно получим
QКИП =[P(I – iF) + PRrФ + W(iW - iF)] / (1-aП) (1.19.)
Энтальпии жидкостей, входящих в уравнение (1.18.) и (1.19.), равны произведениям их мольных теплоемкостей с на температуры t (в °С). Теплоемкости с и теплоты испарения для бинарных смесей вычисляют по правилу аддитивности исходя из свойств чистых компонентов А и В:
с = сАх+сВ(1—х)
r = rАх+rВ(1—х)
где х — мольная доля компонента А в смеси.
Количество тепла QДЕФ, отнимаемого охлаждающей водой в дефлегматоре, зависит от количества конденсирующихся в нем паров. При полной конденсации паров, выходящих из колонны, находим
QДЕФ = P(R+1)rФ = P(R+1)(I-iФ) (1.20.)
Уравнения рабочих линий. Для получения уравнений рабочих линий воспользуемся общим для всех массообменных процессов уравнением ():
y=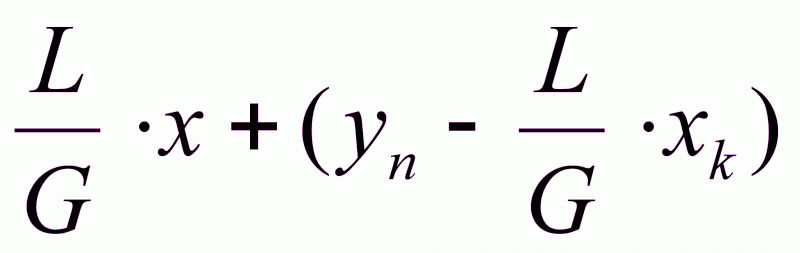 ,
(1.21)
,
(1.21)
где L и G — расходы жидкой и паровой фаз; у, х, уа и хк —соответственно текущие концентрации паровой и жидкой фаз и их концентрации на верхнем конце колонны .
Применяя это уравнение к процессу ректификации, выразим все входящие в него величины в мольных единицах.
Укрепляющая часть колонны. Количество жидкости (флегмы), стекающей по этой части колонны
L = Ф = PR, (1.22)
где R=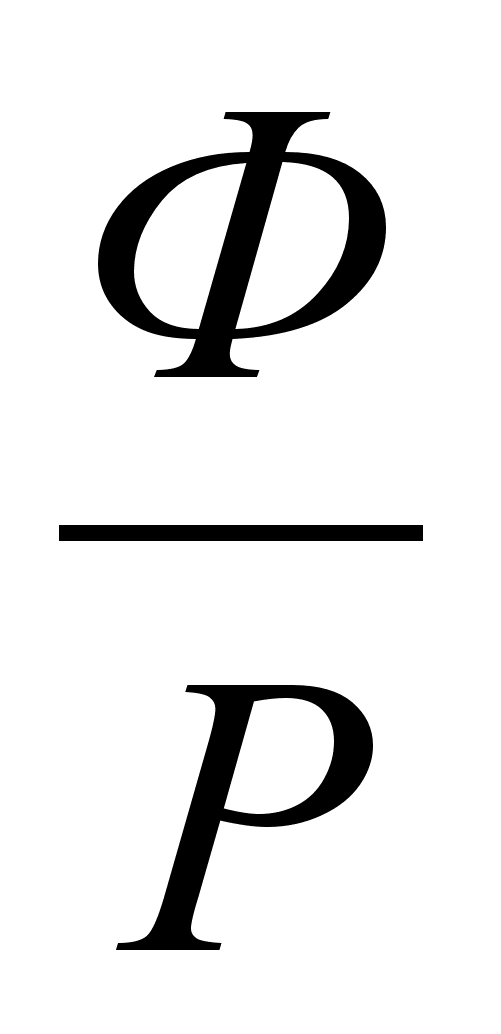 -флегмовое
число, представляющее
собой отношение
количества
флегмы к
количеству
дистиллята.
-флегмовое
число, представляющее
собой отношение
количества
флегмы к
количеству
дистиллята.
Количество паров, поднимающихся по колонне
G=P+Ф=P+PR=P(R+1), (1.23)
Для верхнего конца укрепляющей части колонны состав паров yG=yP и, согласно принятому выше допущению, ур = хр. Следовательно, в данном случае ун = хр.
В том же сечении колонны состав жидкости (флегмы), поступающей из дефлегматора, xф = хр, т. е. хк = хр. Учитывая значения L, G, yk и хk получаем уравнение (1.24), получим
y=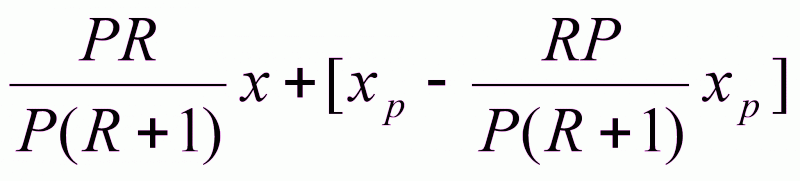 (1.24)
(1.24)
29-04-2015, 04:06
