В последние годы в некоторых работах было предложено определять соотношение билирубин/альбумин вместо определения концентрации билирубина и альбумина отдельно. Тем самым предполагалось достигнуть лучших результатов в прогнозировании и предотвращении билирубиновой энцефалопатии путем оптимизации показаний для заменного переливания крови. Однако существенных результатов эти исследования не дали. Общеизвестно, что существуют факторы, способствующие нарушению связывающей билирубин способности альбумина, а также вещества-лиганды, конкурирующие за места прочного связывания на альбумине (асфиксия, ацидоз, неэстерифицированные жирные кислоты, лекарственные вещества и т.д.).
Гипоксия предрасполагает к развитию билирубиновой энцефалопатии в первую очередь из-за угнетения активности системы глюкоронил-трасферазы. Известно, что митохондрии мозга, равно как и других органов и тканей, содержат билирубиноксидантную систему, окисляющую в присутствии кислорода билирубин. В связи с тем, что процесс гипоксии вызывает повреждение митохондрий и инактивацию оксидаз, может нарушиться механизм окисления билирубина, попадающего в капиллярные субстанции. Этот механизм в норме "срабатывает" у новорожденных в случае достаточной ферментативной активности, тогда как гипоксия нарушает этот процесс. Сочетание желтухи с гипоксией особенно опасно из-за повышенной чувствительности нервных клеток к гипоксии, когда недостаток кислорода вызывает локальный тканевый ацидоз, который может существовать еще некоторое время после коррекции рН крови. Наибольшее значение в патогенезе билирубиновой энцефалопатии имеет проницаемость ГЭБ, который является сложной регуляторной поверхностью, четко контролирующей прохождение веществ через стенку сосудов мозга в клетки мозга. Патоморфологи диагностируют ядерную желтуху не ранее 36 часов после рождения. Таким образом, изменения ЦНС, возникшие в первые 36 часов жизни, могут быть обратимыми. При ядерной желтухе в первую очередь прокрашиваются базальные ганглии: хвостатое ядро, скорлупа, бледный шар. Могут повреждаться также кора мозга, мозжечок, подбугровая область, аммонов рог, ядра продолговатого мозга и мозжечка. Интенсивное поражение ядер дна 4-го желудочка может быть причиной смерти новорожденного. На дне 4-го желудочка чаще прокрашиваются боковые отделы в области кохлеарных и вестибулярных ядер. Значительно реже желтушность находят в зрительном бугре и других отделах мозга. Особенно редуцированы пирамидные клетки 3-го слоя коры, двигательной области спинного мозга и стволовой части головного мозга. После 6-7-го дня жизни ребенка интенсивность острых изменений нейронов снижается, выявляются поля опустошения во многих отделах мозга с последующим развитием глиоза. Нарушается формирование мозга и всего организма ребенка. В клинической картине билирубиновой энцефалопатии наблюдается следующая триада симптомов: гиперкинетическая форма ДЦП, дефект слуха и умственная недостаточность. К сопутствующим проявлениям заболевания относятся ограничение взора вверх, желтушное окрашивание и дефект зубной эмали, дизартрия.
Уробилиноген в моче
Внорме уробилиноген присутствует в моче лишь в следовых количествах (в среднем суточная порция содержит 0,64 мг уробилиногена; повышение до 4 мг все еще рассматривается как не выходящее за пределы нормы). При полной закупорке желчного протока уробилиноген в моче отсутствует, поскольку билирубин не может попасть в кишечник, где он превратился бы в уробилиноген. В этом случае присутствие в моче билирубина и отсутствие уробилиногена свидетельствуют о наличии обтурационной (механической) желтухи либо внутрипеченочной, либо внепеченочной. При гемолитической желтухе увеличение образования билирубина приводит к повышенному синтезу уробилиногена, который появляется в моче в больших количествах. Билирубин в моче больных гемолитической желтухой обычно не обнаруживается; таким образом, повышенное содержание в моче уробилиногена и отсутствие билирубина свидетельствуют о гемолитической желтухе. Обусловленное различными причинами усиление деградации кровяных клеток (например, при пернициозной анемии) также приводит к повышенному содержанию в моче уробилиногена. Кроме того, при попадании инфекции в желчные канальцы содержание уробилиногена в моче может повышаться и в отсутствие нарушений функции печени за счет восстановительной активности инфицирующих бактерий.
Схема, приведенная на рис. 4, суммирует данные о транспорте били-рубина и уробилиногена из печени в кишечник и почки в нормальных условиях, а также при гемолитической желтухе, гепатите или желтухе, обусловленной закупоркой желчных протоков.
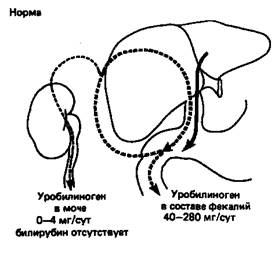
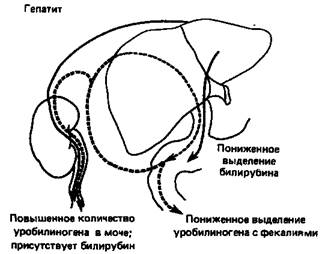
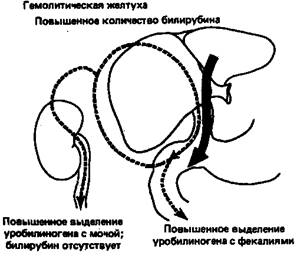
Рисунок 4 - Билирубин-уробилиногеновый цикл
Сплошные стрелки показывают движение билирубиндиклюкуронида, штриховые стрелки — движение уробилиногена.
СПИСОК ЛИТЕРАТУРЫ
1. Марри Р., Греннер Д., Мейерс П., Родуэл В. Биохимия человека. – M., Мир, 1993. –Т 1, 384 с.
2. Berk P. D. et al.Disorders of bilirubin metabolism. In: Metabolic Control and Disease, 8th ed., Bondy P. K., Rosenberg L.E. (eds), Saunders, 1980.
3. Ляхович В.В., Цырлов И.Б. Индукция ферментов метаболизма ксенобиотиков. Новосибирск: Наука, 1981. 240 с.
4. Арчаков А.И. Микросомальное окисление. М.: Наука, 1975. 327 с.
5. Саприн А.Н. // Успехи биол. химии. 1991. Т. 32. С. 146-175.
6. Колесниченко Л.С., Кулинский В.И. // Успехи соврем. биологии. 1989. Т. 107, вып. 2. С. 179-194.
8-09-2015, 22:13
