(Обзор литературы)
Л.С. Страчунский, В.А. Кречиков, НИИ антимикробной химиотерапии, Смоленск, Россия
Моксифлоксацин – новый 8-метоксихинолон широкого спектра действия с высокой активностью в отношении грам(+) и грам(-) аэробной микрофлоры, анаэробов и внутриклеточных возбудителей. Он обладает также активностью против микроорганизмов, резистентных к другим классам антибактериальных препаратов, включая макролидо- и пенициллинорезистентные пневмококки и b-лактамазопродуцирующие штаммы Haemophilus influenzae. В контролируемых клинических исследованиях были продемонстрированы высокая эффективность и безопасность моксифлоксацина при внебольничной пневмонии, обострениях хронического бронхита, синусите, инфекциях кожи, мягких тканей, органов малого таза.
Введение
Когда появились первые хинолоны, никто не ожидал, что их ждет такое блестящее будущее: из небольшой группы препаратов, использовавшихся для лечения инфекций мочевыводящих путей (МВП), они превратились в один из доминирующих классов антибиотиков.
На протяжении более 20 лет налидиксовая кислота и ее производные использовались только для лечения инфекций МВП. Вторая волна развития хинолонов связана с появлением фторированных соединений с гораздо более высокой активностью в отношении широкого спектра грамотрицательных микроорганизмов, некоторых грамположительных возбудителей (Staphylococcus aureus), улучшенной фармакокинетикой, появлением форм для парентерального введения и вследствие этого расширением показаний для применения.
«Золотым стандартом» хинолонов II поколения стал ципрофлоксацин, который с большим успехом используется для лечения многих инфекций. К недостаткам препаратов этого поколения следует отнести низкую активность в отношении пневмококков, хламидий, микоплазм и анаэробов. Эти недостатки преодолены при разработке новых фторхинолонов III–IV поколений (табл.1). Одним из первых препаратов этой группы был левофлоксацин, активность которого против пневмококков и атипичных возбудителей превосходила предыдущие фторхинолоны.
Таблица 1. Классификация хинолонов/фторхинолонов [1, c дополнениями]
|
* Отозван с рынка. ** На стадии клинических испытаний.
Дальнейшие модификации химической структуры привели к появлению соединений, активных и в отношении анаэробов. Однако многие из вновь разработанных препаратов не достигли пациентов или были быстро отозваны с рынка вследствие развития тяжелых нежелательных реакций. Одним из новых препаратов, который стал успешно применяться, явился моксифлоксацин – представитель IV поколения фторхинолонов.
Наиболее важными в молекуле фторхинолонов, отвечающими за их антимикробные свойства, являются группы, занимающие позиции 1, 7 и 8. Циклопропиловая группа в положении 1 обеспечивает активность против грамотрицательных микроорганизмов (рис.1). Присоединение дополнительного кольца в позиции 7 придает высокую активность по отношению к грамположительной микрофлоре, включая пневмококки. Добавление в структуру молекулы метоксигруппы в положении 8 привело к повышению активности в отношении анаэробов без увеличения риска потенциальной фототоксичности [3].
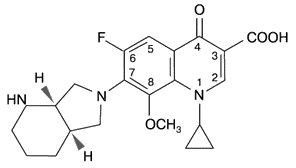 1-Циклопропил-7[(S,S)-2,8-диаза-бицикло(4.3.0)-8-ил]-фтор- 1,4-дигидро-4-оксо-3-хинолонкарбоновой кислоты гидрохлорид
1-Циклопропил-7[(S,S)-2,8-диаза-бицикло(4.3.0)-8-ил]-фтор- 1,4-дигидро-4-оксо-3-хинолонкарбоновой кислоты гидрохлорид
Рис. 1. Химическая структура моксифлоксацина [2]
Механизм действия
Моксифлоксацин, как и все фторхинолоны, действует бактерицидно благодаря ингибированию ферментов класса топоизомераз – ДНК-гиразы (топоизомеразы II) и топоизомеразы IV (рис.2). Эти ферменты выполняют строго определенные функции в процессе формирования пространственной структуры молекулы ДНК при ее репликации: ДНК-гираза катализирует расплетение (отрицательную суперспирализацию) нитей ДНК, а топоизомераза IV участвует в разъединении (декатенации) ковалентно-замкнутых кольцевых молекул ДНК. Ингибирование этих ферментов нарушает процессы роста и деления бактериальной клетки, что приводит к ее гибели.
Основной мишенью моксифлоксацина в грамположительных микроорганизмах преимущественно является топоизомераза IV, а в грамотрицательных – ДНК-гираза [4].
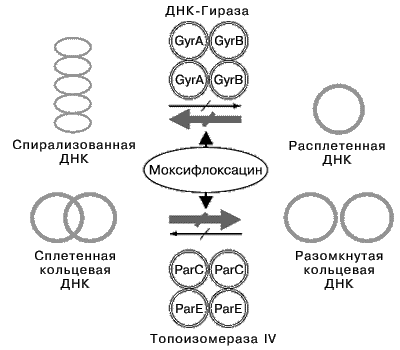
Рис. 2. Механизм действия моксифлоксацина
Механизмы резистентности
Развитие резистентности связано с мутациями в генах gyrA и gyrB (кодируют ДНК-гиразу), parC (grlA) и parE (grlB) – кодируют топоизомеразу IV, а также в гене norA (кодирует мембранные белки, которые участвуют в активном выбросе – эффлюксе – фторхинолонов из клетки) [5]. Высокий уровень резистентности возникает вследствие сочетания этих механизмов [6].
Мутации, возникающие в генах gyrA, gyrB, parC и parE, значительно меньше влияют на активность моксифлоксацина, чем других фторхинолонов. Например, мутации у S.aureus в генах, кодирующих топоизомеразы, меньше снижают активность моксифлоксацина, чем ципрофлоксацина, офлоксацина, левофлоксацина, спарфлоксацина.
У Escherichia coli двойная мутация гена gyrA приводит к снижению IC50 1 норфлоксацина, ципрофлоксацина и спарфлоксацина по сравнению с таковой у немутировавшего типа более чем в 500 раз, в то время как для моксифлоксацина этот показатель не превышает 12 раз [7,8].
Эффлюкс (мутация в гене norA) значительно меньше влияет на активность гидрофобных препаратов, таких, как моксифлоксацин, по сравнению с таковой у гидрофильных препаратов, например у ципрофлоксацина [7].
При применении моксифлоксацина вероятность развития резистентности у грамположительных микроорганизмов, возможно, ниже, чем при применении других фторхинолонов, что связано с его высоким сродством как к топоизомеразе IV, так и к ДНК-гиразе [5, 8].
1 В данной работе степень влияния мутаций gyrA и parC на чувствительность E.coli к фторхинолонам оценивалось как IC50 –концентрация фторхинолона, подавляющая активность фермента на 50%.
Спектр активности
Моксифлоксацин обладает высокой активностью против грамположительных и грамотрицательных микроорганизмов (включая микроорганизмы, устойчивые к другим классам антибиотиков), анаэробов и атипичных возбудителей.
Грамположительные микроорганизмы
Streptococcus pneumoniae
Моксифлоксацин высокоактивен в отношении S.pneumoniae. По данным одного из самых больших исследований [9], включавшем 5640 штаммов, 99,8% из них были чувствительны к препарату, 0,1% – умеренно резистентны, 0,1% – резистентны; МПК90 составила 0,25мг/л (табл.2). Моксифлоксацин обладает также высокой активностью в отношении полирезистентных пневмококков: МПК90 моксифлоксацина для 138 штаммов, устойчивых к пенициллину, эритромицину и тетрациклину, составила 0,5мг/л [14].
Таблица 2. Активность моксифлоксацина invitro против S.pneumoniae, мг/л
|
| Пневмококки: | Пен-Ч – пенициллиночувствительные; Пен-УР – умеренно-резистентные к пенициллину; Пен-Р – пенициллинорезистентные. * НД – нет данных. |
По активности в отношении пневмококка моксифлоксацин превосходит другие фторхинолоны (за исключением ситафлоксацина и гемифлоксацина): он в 2 раза активнее спарфлоксацина [9] и гатифлоксацина [15], в 4–8 раз – левофлоксацина [ 9, 12], в 8 раз – ципрофлоксацина и офлоксацина [12].
По сравнению с b-лактамами и макролидами активность моксифлоксацина в отношении полирезистентных S.pneumoniae значительно выше (табл.3) [9].
Таблица 3. Сравнительная активность моксифлоксацина in vitro против S.pneumoniae, мг/л (n=5640) [9]
|
|||||||||||||||||||||||||||||||||||||||||||||||||
| Пневмококки: | Пен-Ч – пенициллиночувствительные; Пен-Р – пенициллинорезистентные. |
Streptococcus pyogenes
Значение МПК90 моксифлоксацина для S.pyogenes (b-гемолитический стрептококк группыА) составляет 0,06–0,25 мг/л. Моксифлоксацин в 2–4 раза активнее офлоксацина, ципрофлоксацина и левофлоксацина, обладает одинаковой активностью с гатифлоксацином [16,17]. Наличие резистентности к макролидам не влияет на активность моксифлоксацина [17].
Staphylococcus aureus
Для метициллиночувствительных S.aureus (MSSA) МПК90 моксифлоксацина находится в диапазоне 0,06–0,125 мг/л, в то время как для метициллинорезистентных штаммов (MRSA) МПК90 , по данным разных авторов, значительно различается – от 0,06 до 8мг/л [18]. По российским данным, МПК90 моксифлоксацина для MRSA составила 0,125 мг/л, а диапазон МПК – 0,015–2 мг/л [19].
Моксифлоксацин в 8 раз активнее ципрофлоксацина и в 2–4 раза – левофлоксацина против MSSA [ 16, 18]. По данным M.Jones и соавт., моксифлоксацин является одним из самых активных в отношении стафилококков фторхинолоном: МПК90 моксифлоксацина для MRSA, резистентных к ципрофлоксацину, составила 2мг/л, что было равно МПК90 ванкомицина [18].
Грамотрицательные микроорганизмы (табл.4)
Haemophilus influenzae, Moraxella catarrhalis
Моксифлоксацин имеет очень высокую активность в отношении H.influenzae и M.catarrhalis, включая штаммы, резистентные к аминопенициллинам, вследствие продукции b-лактамаз.
Escherichia coli
Как и все другие фторхинолоны, моксифлоксацин обладает высокой активностью по отношению к E.coli, при этом несколько уступая ципрофлоксацину, что, однако, не имеет клинического значения [20,21].
Klebsiella spp.
Моксифлоксацин более активен, чем b-лактамные антибиотики (амоксициллин/клавуланат, цефуроксим), близок по активности к офлоксацину и незначительно уступает ципрофлоксацину [20,21]. На штаммы E.coli и K.pneumoniae, продуцирующие ESBL и резистентные к ципрофлоксацину, моксифлоксацин не действует [22].
Neisseria gonorrhoeae
Для моксифлоксацина характерна очень высокая активность против N.gonorrhoeae, которая несколько ниже, чем у ципрофлоксацина [21].
Pseudomonas aeruginosa
Моксифлоксацин уступает ципрофлоксацину по активности против синегнойной палочки. МПК90 моксифлоксацина, по данным разных авторов, находится в диапазоне от 8 до 32 мг/л и более, а МПК90 ципрофлоксацина – от 0,5 до 16мг/л [ 15, 20, 21].
Таблица 4. Активность моксифлоксацина в отношении аэробных грамположительных и грамотрицательных микроорганизмов, мг/л
|
|||||||||||||||||||||||||||||||||||||||
Внутриклеточные возбудители (табл.5)
Chlamydia spp.
В отношении C.trachomatis моксифлоксацин превосходит не только эритромицин, азитромицин, доксициклин и ципрофлоксацин, но и офлоксацин, что открывает перспективы для его применения в лечении урогенитальных инфекций.
По активности против C.pneumoniae моксифлоксацин находится на одном уровне с левофлоксацином и более активен по сравнению с ципрофлоксацином.
Mycoplasma pneumoniae
Моксифлоксацин обладает большей активностью, чем тетрациклин (МПК90 = 0,25мг/л), доксициклин, ципрофлоксацин и левофлоксацин, однако уступает кларитромицину и азитромицину [27,28].
Mycoplasma hominis
По активности против M.hominis моксифлоксацин значительно превосходит доксициклин, кларитромицин, левофлоксацин и ципрофлоксацин [ 28, 30].
Ureaplasma urealyticum
Моксифлоксацин незначительно уступает кларитромицину и проявляет высокую активность как в отношении чувствительных (МПК90 – 0,25 мг/л), так и резистентных к доксициклину штаммов (МПК90 – 0,5 мг/л). Моксифлоксацин активнее доксициклина, эритромицина, ципрофлоксацина и левофлоксацина [ 28, 30].
Legionella spp.
Моксифлоксацин превосходит по активности ципрофлоксацин и такой классический антибиотик для лечения легионеллезной инфекции, как эритромицин, но несколько уступает кларитромицину и рифампицину [31,32].
Таблица 5. Активность моксифлоксацина в отношении внутриклеточных возбудителей, МПК90 , мг/л
|
Mycobacterium spp. (табл.6)
Моксифлоксацин активен в отношении как чувствительных, так и полирезистентных штаммов M.tuberculosis и превосходит ципрофлоксацин, офлоксацин и левофлоксацин. МПК90 моксифлоксацина для полирезистентных штаммов составляет 0,5мг/л [33,34].
По отношению к атипичным микобактериям (M.kansasii, M.avium-intracellulare) моксифлоксацин превосходит ципрофлоксацин и левофлоксацин [33].
Таблица 6. Активность моксифлоксацина в отношении микобактерий, МПК90 , мг/л
|
Анаэробы (табл.7)
В отличие от фторхинолонов II–III поколений (ципрофлоксацина, офлоксацина, левофлоксацина) моксифлоксацин обладает высокой активностью против анаэробов (как неспорообразующих, так и спорообразующих). По антианаэробной активности моксифлоксацин сравним с имипенемом, метронидазолом и клиндамицином [35,36].
Таблица 7. Активность моксифлоксацина в отношении анаэробов, мг/л [35,36]
|
Постантибиотический эффект
Фторхинолоны обладают выраженным постантибиотическим эффектом (ПАЭ) против грамположительных и грамотрицательных микроорганизмов, который в среднем равен 2ч.
ПАЭ моксифлоксацина для разных микроорганизмов составляет 1,2–3,1ч при концентрации, равной 4ґМПК, и увеличивается с возрастанием концентрации препарата. Например, ПАЭ для S.pneumoniae равно 2,2ч при концентрации препарата 4ґМПК и возрастает до 2,7ч при его концентрации 10ґМПК [37].
Фармакокинетика
Всасывание
Моксифлоксацин практически полностью всасывается из желудочно-кишечного тракта при приеме внутрь. Биодоступность составляет от 86 [38] до 91,8% [39]. При внутривенном введении 400мг в течение 1ч значения максимальной концентрации препарата в плазме (Cmax ) и площади под фармакокинетической кривой (ПФК) незначительно больше, чем при приеме 400мг внутрь [ 38, 40].
Максимальная концентрация препарата в плазме (Cmax ) в исследовании H.Stass и соавт. [38,39] составила 2,5мг/л через 2ч после приема внутрь 400мг. В то же время в исследованиях R.Wise и соавт. [40] и A.Lubasch и соавт. [41] максимальная концентрация была 4,34–4,98мг/л и достигалась через 1ч. Прием пищи, включая молочные продукты, не влияет на всасывание моксифлоксацина [42,43].
Распределение
При приеме внутрь моксифлоксацин имеет большой объем распределения (Vd ): 3,08–3,55л/кг [ 2, 38] и достигает высоких концентраций в тканях и жидкостях организма: в бронхиальном секрете, альвеолярных макрофагах, тканях верхнечелюстной пазухи и жидкости, покрывающей эпителий бронхов (табл.8).
Концентрация моксифлоксацина в жидкостях дыхательных путей значительно превышает МПК90 для основных возбудителей респираторных инфекций (табл. 4, 5).
Моксифлоксацин связывается с белками плазмы на 39,4–48%, что несколько выше, чем у ципрофлоксацина (35%) [ 2, 38].
Таблица 8. Концентрация моксифлоксацина в жидкостях и тканях организма *
|
* После приема 400 мг препарата внутрь.
Метаболизм
Моксифлоксацин метаболизируется в печени путем конъюгации с образованием двух метаболитов: М1 (ацетилглюкуронид) и М2 (сульфопроизводное моксифлоксацина). М1 имеет высокую степень связывания с белками плазмы (89,5%), а М2 практически не связывается – 4,8% (рис.3) [38].
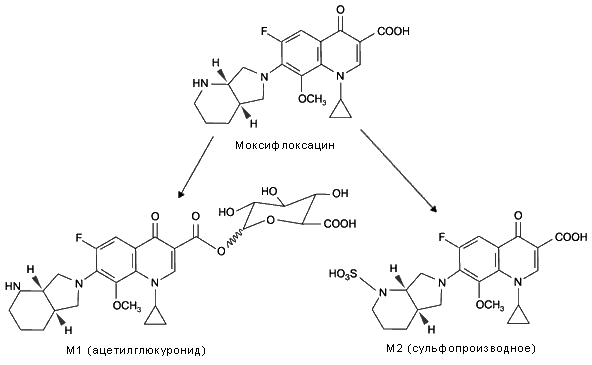
Рис. 3. Метаболизм моксифлоксацина в печени [38]
Выведение
При однократном приеме 400мг моксифлоксацина внутрь более 96% дозы выводится через почки и желудочно-кишечный тракт, при этом с мочой экскретируется 15,1–35,4% препарата [ 2, 38, 40]. В неизмененном виде через почки выводится 19,4% дозы; метаболита М1 – 2,5% и в виде метаболита М2 – 13,6%. С фекалиями в неизмененном виде выводится 25,4% дозы и 35,5% – в виде метаболита М1.
По данным большинства авторов, период полувыведения составляет 12–13ч, что больше, чем у ципрофлоксацина, офлоксацина и левофлоксацина. Длительный период полувыведения позволяет принимать препарат 1 раз в сутки в отличие от большинства фторхинолонов II поколения [ 2, 38, 40, 41]. Другие фармакокинетические параметры приведены в табл.9.
Таблица 9. Фармакокинетические свойства моксифлоксацина
|
* Препарат вводился однократно в дозе 400 мг.
Cmax - максимальная концентрация в плазме, Tmax - время достижения Cmax , ПФК- площадь под фармакокинетической кривой, Vd - объем распределения, CL- клиренс препарата из плазмы; CLR - почечный клиренс, T1/2 - период полувыведения.
Влияние возраста, заболеваний печени и почек
У взрослых возраст практически не влияет на фармакокинетические свойства моксифлоксацина, но значения максимальной концентрации препарата в плазме и ПФК несколько выше у пожилых женщин по сравнению с таковыми у молодых и пожилых мужчин [46].
В отличие от офлоксацина и левофлоксацина при легкой почечной недостаточности – клиренс креатинина >30мл/(мин·1,73 м2 ) – период полувыведения остается неизменным и составляет 14,5ч [47]. Однако пока нет достаточной информации о применении моксифлоксацина при клиренсе креатинина <30мл/(мин·1,73м2 ) или при гемодиализе, поэтому препарат не следует назначать этим категориям пациентов.
У пациентов с легкой и среднетяжелой печеночной недостаточностью (n=8) значения Cmax , ПФК и T1/2 оказались меньше, чем у здоровых добровольцев (n =10): Cmax – 2,55 и 3,02мг/л, ПФК – 25,1 и 32,8мг/(л·ч), T1/2 – 11,7 и 13,4ч соответственно [48]. В целом пока мало данных о применении моксифлоксацина у пациентов с печеночной недостаточностью.
Как видно из данных табл.9, нет существенных различий между фармакокинетическими параметрами при приеме моксифлоксацина внутрь и при внутривенном введении. Это позволит при появлении на рынке формы для парентерального введения использовать моксифлоксацин в ступенчатой терапии с ранним переходом на прием препарата внутрь.
Фармакодинамика
В настоящее время все большее внимание уделяется фармакодинамическим свойствам антибиотиков, которые значительно влияют на их эффективность. Считается, что для фторхинолонов условиями эффективности являются значения отношений [49,50]:
– максимальной концентрации в плазме к МПК (Cmax /МПК) более 10; – ПФК к МПК (ПФК/МПК) более 100–125 (более 40–50 для S.pneumoniae); – ПФК к МПК фракции препарата, несвязанной с белками плазмы (ПФК/МПКнесвяз. ) более 25–30.
По результатам invitro моделирования с использованием респираторных патогенов, значения ПФК/МПК и ПФК/МПКнесвяз. для моксифлоксацина выше, чем для других фторхинолонов (табл.10).
Таблица 10. Фармакодинамические свойства моксифлоксацина * [49]
|
* Данные получены в модели in vitro с использованием полирезистентных штаммов S.pneumoniae.
Клиническое применение
Моксифлоксацин изучался при заболеваниях дыхательных путей (внебольничная пневмония, обострение хронического бронхита, острый синусит), инфекциях кожи и мягких тканей, а также при гинекологических инфекциях.
Внебольничная пневмония
Моксифлоксацин привлекает особое внимание при лечении внебольничной пневмонии в связи с его высокой активностью в отношении фактически всех наиболее вероятных возбудителей, включая полирезистентные пневмококки, гемофилы, продуцирующие b-лактамазы, а также внутриклеточные (атипичные) возбудители M.pneumoniae и C.pneumoniae [ 9, 25, 27].
Ни один из других классов антибактериальных препаратов не обладает таким широким спектром активности и способностью преодолевать приобретенную резистентность респираторных патогенов, как новые фторхинолоны. Например, к макролидам в последнее время часто отмечается ассоциированная резистентность: 45% пенициллинорезистентных пневмококков устойчивы к эритромицину [51], в то время как МПК90 моксифлоксацина для таких штаммов составляет 0,5мг/л [14].
Хорошие микробиологические характеристики сочетаются с благоприятной фармакокинетикой и фармакодинамикой моксифлоксацина: длительный период полувыведения, обеспечивающий однократный прием, высокие концентрации в тканях бронхов и легких, оптимальные значения показателей ПФК/МПК и ПФК/МПКнесвяз. [49].
В обзоре приведены данные 3 рандомизированных двойных слепых исследований клинической и бактериологической эффективности моксифлоксацина при внебольничной пневмонии (табл.11). В 2 исследованиях сравнивали эффективность моксифлоксацина и кларитромицина. По клинической эффективности они были равны – 94–95% [52,53]. По данным G.Hoffken и соавт., бактериологическая эффективность моксифлоксацина выше 2
, чем
8-09-2015, 19:27
