АДЕНИЛАТЦИКЛАЗНЫЙ СИГНАЛЬНЫЙ МЕХАНИЗМ ДЕЙСТВИЯ ПЕПТИДОВ ИНСУЛИНОВОГО СУПЕРСЕМЕЙСТВА У ПОЗВОНОЧНЫХ И БЕСПОЗВОНОЧНЫХ
Автореферат
диссертации на соискание ученой степени
доктора биологических наук
Санкт-Петербург 2007
Актуальность проблемы
Изучение гормональных сигнальных систем, участвующих в регуляции жизненно важных для организма клеточных процессов, является одной из актуальных проблем современной молекулярной эндокринологии и биохимии. К числу систем, осуществляющих реализацию регуляторного действия веществ гормональной и негормональной природы, относится аденилатциклазная сигнальная система (АЦС), которая представлена в клетке сложным трансмембранным комплексом, состоящим, по крайней мере, из трех молекулярных блоков. Необходимыми компонентами АЦС являются: рецепторы, способные воспринимать внеклеточные сигналы, гетеротримерные ГТФ-связывающие белки (G-белки) стимулирующего (Gs) или ингибирующего (Gi) типа, состоящие из трех субъединиц – α, b, γ и обеспечивающие сопряжение между рецептором и третьим компонентом системы - ферментом аденилатциклазой (АЦ), катализирующей образование универсального внутриклеточного посредника – циклического аденозинмонофосфата (цАМФ). При его участии осуществляется реализация целого ряда регуляторных эффектов в клетке (пролиферация, дифференцировка, апоптоз, синтез белка и др.).
К настоящему времени в литературе накоплен значительный объем данных, свидетельствующих об участии АЦС и цАМФ в трансдукции сигналов группы гормонов не пептидной природы (серотонин, адреналин, норадреналин и др.), осуществляющих свой эффект на клетку через рецепторы серпантинного типа, семь раз пронизывающие мембрану. В рамках настоящего исследования мы предприняли попытку выяснить возможность участия АЦС в реализации действия пептидов инсулинового суперсемейства, обладающих рецепторами тирозинкиназного типа, один раз пронизывающими мембрану клетки. До исследований, проведенных нами, участие системы АЦС-цАМФ в реализации действия гормонов инсулиновой природы практически отрицалось. В литературе имелись лишь отдельные сведения о влиянии инсулина, бомбиксина, релаксина на активность АЦ (Pertseva et al., 2003; Patel, 2004). Несмотря на успехи, достигнутые за последние десятилетия в изучении молекулярных механизмов действия инсулина и инсулиноподобных пептидов, многие аспекты плейотропного действия этого гормона и родственных ему пептидов до сих пор остаются невыясненными (Pertseva et al., 2003; Телкова, 2005). В связи с этим изучение ранее неизвестных молекулярных механизмов действия пептидов инсулинового суперсемейства, насчитывающего в настоящее время около 50 представителей, относится к числу актуальных проблем современной эндокринологии. Согласно современным представлениям, инсулин и родственные ему пептиды играют ключевую роль в регуляции ряда клеточных процессов – клеточный рост, апоптоз, метаболизм. Эти пептиды имеют общее эволюционное происхождение, так как возникли в ходе эволюции из общего анцестрального гена в результате дупликации и последующей дивергенции образовавшихся генетических линий, сохранив при этом структурное и функциональное сходство (Murray-Rust et al., 1992; Chan et al., 1992).
К изучению участия АЦС в реализации действия гормонов и ростовых факторов инсулиновой природы лаборатория приступила в начале 90-х годов. Отправной точкой послужили данные, впервые полученные нами, о способности инсулина и родственных пептидов активировать ГТФ-зависимым образом АЦ в мышечных тканях млекопитающих и моллюсков (Plesneva et al., 1994). Мы использовали эволюционный подход, предложенный Л.А. Орбели (1958) применительно к эволюционной биохимии, который включал исследования в филогенезе, онтогенезе и при патологии. Было изучено: 1) влияние на АЦС инсулина, инсулиноподобного фактора роста 1 (ИФР-1) позвоночных и инсулиноподобного пептида (ИПП) беспозвоночных (моллюск Anodonta cygnea ; 2) влияние на АЦС пептидов в тканях-мишенях животных разного филогенетического уровня (позвоночные – крысы, птицы и беспозвоночные – моллюски); 3) действие пептидов инсулинового суперсемейства на АЦС в онтогенезе (в тканях куриных эмбрионов разного возраста и у цыплят); 4) действие пептидов инсулинового суперсемейства на АЦС при экспериментальном диабете у позвоночных и беспозвоночных.
Цель работы. Доказать участие аденилатциклазной сигнальной системы в реализации регуляторных эффектов инсулина, ИФР-1, ИПП моллюска в клетке и расшифровать структурно-функциональную организацию АЦ сигнального механизма их действия в тканях позвоночных и беспозвоночных, а также установить роль АЦ сигнального механизма в регуляции фундаментальных клеточных процессов – клеточный рост, апоптоз.
Задачи исследования
1. Исследовать действие инсулина, ИФР-1 и ИПП, выделенного из висцеральных органов моллюска Anodonta cygnea (Русаков и др., 1991), на АЦС в мышечных тканях позвоночных и беспозвоночных. Охарактеризовать зависимость эффекта от времени и концентрации исследуемых пептидов, а также от присутствия гуаниновых нуклеотидов для подтверждения вовлеченности в АЦ сигнальный механизм гетеротримерных G-белков.
2. Исследовать структурно-функциональную организацию АЦ сигнального механизма, опосредующего эффекты пептидов инсулинового суперсемейства у позвоночных и беспозвоночных и выяснить последовательность этапов передачи регуляторных сигналов этих пептидов на АЦС.С этой целью: а) установить тип рецепторов и G-белков, вовлеченных в АЦ сигнальный механизм действия пептидов, используя ингибиторы рецепторных тирозинкиназ и метод АДФ-рибозилирования бактериальными токсинами; б) выявить участие фосфатидилинозитол-3 киназы (ФИ-3-К), используя специфичный ингибитор вортманнин; в) идентифицировать изоформу протеинкиназы «С» (ПКС); используя ингибиторы ПКС и моноклональные антитела к изоформам ПКС.
3. Исследовать участие АЦ сигнального механизма действия инсулина и ИФР-1 в регуляции процессов клеточного роста и апоптоза, исходя из гипотезы о важной роли цАМФ в регуляции фундаментальных процессов в клетке (Перцева, 2000).
4. Исследовать функциональные нарушения в АЦ сигнальном механизме действия пептидов инсулинового суперсемейства при эндокринной патологии – сахарный диабет 1-го и 2-го типов.
Научная новизна
Впервые обнаружено стимулирующее действие инсулина, ИФР-1 и ИПП моллюска A . cygnea на активность АЦ. Показано участие рецепторной тирозинкиназы и установлена вовлеченность G-белков (Gi) и (Gs) типа в реализацию активирующего действия этих пептидов на АЦ. Впервые показано, что в проявлении АЦ стимулирующих эффектов инсулина и ИФР-1 участвуют ФИ-3-К и изоформы ПКС - ПКСz и возможно ПКСε.
В мышечных тканях позвоночных и беспозвоночных животных обнаружен ранее неизвестный АЦ сигнальный механизм действия инсулина и ИФР-1 и установлена его структурно-функциональная организация, представленная в клетке следующей сигнальной цепью: рецептор тирозинкиназного типа Þ Gi-белок (bγ-димер) Þ ФИ-3-К Þ ПКСz (позвоночные) или ПКСε (беспозвоночные) Þ Gs-белок Þ АЦ Þ цАМФ Þ протеинкиназа «А» (ПКА) Þ эффекторные системы. Этот механизм отличается по числу сигнальных блоков от известного АЦ сигнального механизма действия гормонов, обладающих рецепторами серпантинного типа, представленного в клетке следующей цепью: рецептор серпантинного типа Þ G-белок (Gi или Gs) Þ АЦ Þ цАМФ Þ ПКА Þ эффекторные системы.
Следует отметить, что действие пептидов инсулиновой природы на АЦ в мышечной ткани моллюска осуществляется через АЦ сигнальный механизм, сходный с таковым позвоночных, но имеющий на пострецепторных этапах трансдукции гормонального сигнала отличие на уровне ПКС. Исходя из результатов нашего исследования, в АЦ сигнальном механизме действия пептидов инсулинового суперсемейства у позвоночных принимает участие ПКСζ, а у беспозвоночных (моллюски), как предполагается, – ПКСε.
Экспериментально подтверждена, выдвинутая нами гипотеза, о важной роли АЦ-цАМФ в реализации регуляторного действия инсулина и ИФР-1 на фундаментальные процессы в клетке. Показано участие АЦ-цАМФ системы в способности ИФР-1 и инсулина стимулировать клеточный рост и ингибировать апоптоз в культурах фибробластоподобных клеток.
Обнаружены нарушения в АЦ сигнальном механизме действия инсулина при патологии (сахарный диабет 1-го и 2-го типов).
Теоретическое и практическое значение работы
Теоретическое и практическое значение работы определяется важной ролью инсулина и других пептидов инсулинового суперсемейства в организме высших и низших животных. Обнаружение новых сигнальных механизмов действия пептидов этой группы, в частности инсулина и ИФР-1, расширяет современные представления о спектре сигнальных систем, участвующих в регуляторном действии пептидов инсулинового суперсемейства.
Применение эволюционного подхода (изучение ряда эволюционно-родственных пептидов и использование представителей позвоночных и беспозвоночных) позволило выявить консервативность обнаруженного АЦ сигнального механизма действия пептидов инсулиновой природы.
Данные, полученные на беспозвоночных, могут быть полезны для понимания сигнальных механизмов действия пептидов инсулинового суперсемейства у позвоночных и для разработки моделей эндокринной патологии у человека (сахарный диабет) в рамках нового направления - «эволюционная биомедицина» (Перцева, 2006).
Полученные данные о молекулярных механизмах действия инсулина и ИФР-1 имеют фундаментальное значение и могут применяться при чтении курса лекций в университетах и медицинских ВУЗах как в России, так и за рубежом.
Результаты исследования имеют важное практическое значение в плане выявления молекулярных основ этиологии и патогенеза сахарного диабета, а также в создании новых подходов для диагностики этого заболевания. Обнаруженный нами АЦ сигнальный механизм действия инсулина, может служить основой для разработки биохимического теста, позволяющего проводить диагностику нарушения отдельных звеньев в молекулярном механизме действия инсулина.
Положения, выносимые на защиту
1. Впервые установлено, что пептиды инсулинового суперсемейства (инсулин, ИФР-1 и ИПП моллюска Anodonta cygnea ) ГТФ-зависимым образом активируют АЦ в тканях позвоночных (млекопитающие, птицы) и беспозвоночных (моллюски) животных.
2. Реализация АЦ активирующего действия пептидов инсулиновой природы осуществляется через обнаруженный нами АЦ сигнальный механизм, включающий следующую сигнальную цепь: рецептор-тирозинкиназа Þ Gi-белок (βγ-димер) Þ ФИ-3-К Þ ПКСzÞ Gs-белок Þ АЦ.
3. С участием АЦ сигнального механизма, генерирующего цАМФ, осуществляется регуляторное действие пептидов инсулиновой природы на фундаментальные клеточные процессы - стимулируется клеточный рост и ингибируется апоптоз.
4. При эндокринной патологии (сахарном диабете 1-го и 2-го типов) нарушается функционирование АЦ сигнального механизма действия гормонов инсулиновой природы в основном на уровне Gs-белка и его сопряжения с АЦ.
5. Сходство структурно-функциональной организации АЦ сигнального механизма действия пептидов инсулинового суперсемейства у позвоночных и беспозвоночных животных свидетельствует об его эволюционной консервативности.
Апробация работы
Основные результаты и положения работы были представлены и доложены на следующих конференциях и съездах: 17-я, 19-я, 20-я, 21-я Конференции Европейского Общества Эндокринологов (Кордова, Испания, 1994; Нидерланды, 1998; Фаро, Португалия, 2000; Бонн, Германия, 2002); 4-й Симпозиум по нейробиологии моллюсков (Амстердам, Нидерланды, 1994); Симпозиум по инсулину, ИФР-1 и инсулиноподобным пептидам (Испания, Барселона, 1997); XXXIII Международный конгресс физиологов (Санкт-Петербург, 1997); 2-й съезд Биохимического Общества РАН (Москва, 1997); XVII съезд физиологов России (Ростов-на-Дону, 1998); конференция “Рецепция и внутриклеточная сигнализация” (Пущино, 1998); Съезд Биохимического общества Университета Глазго (Глазго, Великобритания, 1999); 18-ый Международный конгресс биохимиков и молекулярных биологов (Бирмингем, Англия, 2000); 3-я и 4-я Международные конференция по релаксину и родственным пептидам (Брум, Австралия, 2000; Виоминг, США, 2004); XVIII Съезд Физиологического Общества имени И.П. Павлова, Казань, 2001); XI, XII и XIII Международные совещания по эволюционной физиологии (Санкт-Петербург, 1996; 2001; 2006); Международная Европейская конференция (Люксембург, 2002); Вторая конференция “Эндокринная регуляция физиологических функций в норме и патологии”, посвященная 80-летию со дня рождения М.Г. Колпакова. (Новосибирск. Октябрь, 2002); 1-й съезд Общества Клеточных Биологов (Санкт-Петербург, 2003); Физиологический съезд (Екатеринбург, 2004); 1-й Съезд физиологов СНГ (Сочи, Дагомыс, 2005);
Публикации. По теме диссертации опубликовано 75 работ, в том числе 36 статей в рецензируемых отечественных и международных изданиях.
Личный вклад автора – Экспериментальные данные получены лично автором или при его непосредственном участии.
Структура и объем диссертации. Диссертация изложена на 259страницах, состоит из введения, обзора литературы, описания материалов и методов,изложения результатов их обсуждения, заключения, выводов и списка литературы, включающего 285 источников. Работа иллюстрирована 43рисунками и 35 таблицами.
Основное содержание работы
Объекты и методы исследования. Объектами исследования служили: 1) представители позвоночных - крысы Ratus norvegicus линии Wistar; 2) куры породы русская белая «Леггорн »; 3) представители беспозвоночных - пресноводный двустворчатый моллюск Anodonta cygnea ; 4) культура клеток миобластов куриных эмбрионов; 5) фибробластоподобная культура клеток линии Swiss 3T3; 6) культура клеток, трансформированная из нормальных фибробластов линии Е1А+сНа-ras (клетки, впадающие в апоптоз) и E1A+E1B (клетки, не впадающие в апоптоз).
Методы. В работе использован широкий спектр физиологических, биохимических и фармакологических методов:
- выделение фракций плазматических мембран мышечной ткани позвоночных и беспозвоночных животных с использованием метода дифференциального центрифугирования (Kidwai et. al., 1973 с нашими модификациями);
- выделение частично очищенных мембранных фракций культуры клеток миобластов куриных эмбрионов, фибробластоподобных клеток линии Swiss 3T3, E1A+cHa-ras, E1A+E1B (Плеснёва и др., 1999; 2003);
- выделение фракции, содержащей примембранную форму цАМФ-ФДЭ (Houslay, 1985).
- определение активности АЦ с использованием радиоактивного субстрата АЦ реакции - [α32 P]АТФ (Salomon et al., 1974 с некоторыми модификациями);
- определение активности цАМФ-ФДЭ, с использованием радиоактивного субстрата [3 H]цАМФ (Ткачук и др., 1978);
- АДФ-рибозилирование гетеротримерных G-белков холерным и коклюшным токсинами (Pertseva et al., 1992);
- электрофорез в ПААГ
- иммуноблотинг с использованием моноклональных антител для идентификации изоформы ПКСζ;
- определение ростстимулирующей активности действия инсулина, ИФР-1, ЭФР и цАМФ по включению [14 C] тимидина в ДНК культуры клеток Swiss3T3 (Баркан и др. 1992; Плеснёва и др., 1997; 1999);
- использование модели апоптоза на трансформированных клетках, полученных из нормальных эмбриональных фибробластов введением пары комплементирующих онкогенов E1A+cHa-ras, обладающих высокой проапототической чувствительностью к удалению ростовых факторов (Bulavinet.al., 1999) и ее характеристика (Плеснёва и др., 2003);
- оценка антиапоптотического действия инсулина, ИФР-1 и цАМФ с использованием метода клоногенной выживаемости культуры клеток E1A+cHa-ras ( Плеснёва и др., 2003);
- определение активности ферментов углеводного метаболизма – гликогенсинтетазы и глюкозо-6-фосфат-дегидрогеназы (Кузнецова, 1998; Кузнецова и др., 2004);
- определения содержания белков методом Лоури;
- создания моделей экспериментального диабета 1-го и 2-го типов у позвоночных (Ping et al., 1999 с нашими модификациями) и диабетоподобного состояния у беспозвоночных (Плеснева и др., 2006; Кузнецова и др., 2007) с использованием стрептозотоцина.
- статистические методы обработки данных по программам (Statgraph и Anova).
Результаты исследования и их обсуждение
В работе представлены экспериментальные доказательства активирующего действия инсулина, ИФР-1 и ИПП на АЦ, установлена структурно-функциональная организация АЦ сигнального механизма в клетке и его роль в регуляции пептидами инсулиновой природы клеточного роста и апоптоза.
Основные этапы работы состояли в исследовании:
- действия пептидов инсулиновой природы на активность АЦ при разном времени и разной концентрации in vitro и in vivo ;
- участия примембранной цАМФ-ФДЭ в функционировании АЦ сигнального механизма действия инсулиноподобных пептидов;
- звеньев АЦ сигнального механизма (от рецептора до эффекторных систем);
- роли АЦ сигнального механизма, как в регуляции клеточных процессов, так и его функционального применения в условиях патологии;
Влияние in vitro инсулина, ИФР-1 и ИПП на активность АЦ в тканях позвоночных и беспозвоночных и в культурах клеток в разные временные сроки
Проведено исследование in vitro динамики во времени АЦ активирующего эффекта инсулина, ИФР-1 и ИПП моллюска при концентрации пептидов 10-8 М и для сравнения эпидермального ростового фактора (ЭФР), пептида не инсулиновой природы, обладающего рецептором тирозинкиназного типа (Никольский и др., 1987). Показано, что в мембранной фракции скелетных мышц крыс наибольшее выраженное активирующее действие исследованных пептидов на АЦ проявляется через 2.5 мин. Активирующий АЦ эффект инсулина составляет +236%. Эффект менее выражен при действии ИФР-1 (+201%), ЭФР (+186%) и ИПП моллюска +124% (Рис. 1; Таблица 1).

Рис. 1. Концентрация пептидов – 10-8 М Активация АЦ пептидами (в%) по сравнению с базальной активностью фермента, принятой за 100%, приведена в тексте. Различия достоверны (р<0.05 )
Таблица 1.Динамика во времени действия ИФР-1 на активность АЦ в мембранной фракции скелетных мышц крыс
| Воздействия | Активность АЦ (пкмоль цАМФ/мин/мг белка) | ||
| 2.5 мин | 5 мин | 10 мин | |
| Без ИФР-1 | 71.2±4.8 (100%) |
85.11±3.3 (100%) |
101.20±9.24 (100%) |
| + ИФР-1 | 214.31±12.1 (301%) |
136.16±5.2 (160%) |
96.14±4.6 (95%) |
Примечание: В скобках - базальная активность АЦ (без воздействий), принятая за 100% и активность АЦ (в%) при действии ИФР-1
В мембранной фракции культуры куриных миобластов показано (рис. 2), что стимулирующий АЦ эффект инсулина через 2.5 мин составляет +256%, по сравнению с базальной активностью, принятой за 100% и имеет сходство с данными, полученными на мембранной фракции скелетных мышц крыс (+236%) (рис. 1).
В тканях моллюска A.cygnea , ИПП, выделенный из висцеральных органов этого моллюска, оказывает наиболее выраженное активирующее действие на АЦ (+422%), по сравнению с ЭФР (+221%), ИФР-1 (+169%) и инсулином (+133%) (Рис. 3; Таблица 2). Следует отметить, что активирующий АЦ эффект исследуемых пептидов в наибольшей степени проявляется через 2,5 мин, через 5 мин снижается, а через 10 минут практически отсутствует (Таблица 2; Рис. 3).
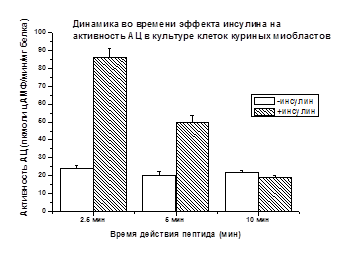
Рис. 2. Концентрация инсулина 10-8 М. Различия достоверны (р<0.05 )
Таблица 2.Динамика во времени действия ИФР-1 на активность АЦ в мембранной фракции гладких мышц моллюска
| Воздействия | Активность АЦ (пкмоль цАМФ/мин/мг белка) | ||
| 2.5 мин | 5 мин | 10 мин | |
| Без ИФР-1 | 110.21±10.8 (100%) |
125.31±9.3 (100%) |
106.04±6.6 (100%) |
| + ИФР-1 | 259.92±11.4 (269%) |
229.31±5.2 (183%) |
103.81±5.8 (98%) |
Примечание – как в таблице 1.
Таким образом, в мембранных фракциях, выделенных из мышечных тканей исследуемых животных и культуры клеток куриных миобластов, наблюдается закономерность проявления эффекта пептидов в зависимости от времени действия. Инсулин, ИФР-1, ИПП и ЭФР оказывают активирующее действие на АЦ в течение 2,5 и 5 мин с максимальным эффектом через 2.5 мин. АЦ активирующий эффект исследуемых пептидов видоспецифичен. В скелетных мышцах крыс ряд эффективности пептидов по их влиянию на АЦ имеет следующий порядок: инсулин > ИФР-1 > ЭФР > ИПП, а в мышечных тканях моллюска - ИПП > ЭФР > ИФР-1 > инсулин.

Рис. 3. Концентрация пептидов – 10-8 М Активация АЦ пептидами (в %) по сравнению с базальной активностью фермента, принятой за 100%, приведена в тексте. Различия достоверны (р<0.05 )
Влияние in vivo разных доз инсулина на активность АЦ в тканях позвоночных и беспозвоночных в разные временные сроки
Обнаружив в опытах in vitro
стимулирующее влияние пептидов инсулинового суперсемейства на активность АЦ, мы исследовали влияние инсулина, основного представителя инсулинового суперсемейства, на активность АЦ в разных дозах и при разном времени действия
8-09-2015, 21:47
