На правах рукописи
Гейн Сергей Владимирович
РОЛЬ b -ЭНДОРФИНА В НЕЙРОЭНДОКРИННОЙ РЕГУЛЯЦИИ ФУНКЦИЙ ИММУННОЙ СИСТЕМЫ
14.00.36 Аллергология и иммунология
Автореферат диссертации на соискание ученой степени доктора медицинских наук
Пермь - 2007
Работа выполнена в аналитической лаборатории Института экологии и генетики микроорганизмов УрО РАН, Пермь.
Научный консультант:
академик РАН и РАМН, д.м.н., профессор
Черешнев Валерий Александрович
Официальные оппоненты:
доктор медицинских наук, профессор Сибиряк Сергей Владимирович,
доктор медицинских наук, профессор Кузнецов Валериан Фёдорович,
доктор медицинских наук, профессор Юшков Владимир Викторович
Ведущая организация: Институт экспериментальной медицины РАМН, Санкт-Петербург.
Защита состоится «__»__________ 2007 г. в ____ часов на заседании диссертационного совета Д 004.019.01 в Институте экологии и генетики микроорганизмов УрО РАН по адресу: 614081, г. Пермь, ул. Голева, 13. Факс (342)2446711.
С диссертацией можно ознакомиться в библиотеке Института экологии и генетики микроорганизмов УрО РАН, Пермь.
Автореферат разослан «___» _______________2007 г.
Ученый секретарь диссертационного совета,
чл.-корр.РАН Ившина Ирина Борисовна
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Поддержание внутреннего гомеостаза определяется взаимодействием нервной, эндокринной и иммунной систем организма. Известно, что иммунная система многокомпонентна, ее функционирование обеспечивается сложной сетью взаимосвязанных сигналов. Одними из важнейших посредников во взаимодействии нервной и иммунной систем выступают эндогенные опиоидные пептиды, представляющие собой группу факторов и играющих ключевую роль в процессах адаптации организма (Корнева, Шхинек, 1988; Зозуля, Пшеничкин, 1990; Корнева, 2007; Maier, 2003; Pruett, 2003; Bodnar, Klein, 2006; Sharp, 2006; Wilbert-Lampenetal., 2007). Несмотря на то, что в последние годы изучению влияния эндогенных опиоидных пептидов на процессы регуляции иммунитета в литературе уделяется достаточно много внимания (Panerai, Sacerdote, 1997; Tomassinietal., 2003, 2004; Sacerdote, 2003), вопрос о механизмах реализации эффектов биорегуляторных пептидов данного класса остается крайне актуальным.
Основной источник опиоидных пептидов в организме - центральная нервная система. Основная группа пептидных гормонов (адренокортикотропный гормон, b-липотропин, меланоцитстимулирующий гормон, b-эндорфин) образуется в результате расщепления большой молекулы – предшественника проопиомеланокортина. При этом наиболее активным и полифункциональным представителем пептидов группы проопиомеланокортина является b-эндорфин. Основной источник b-эндорфина в центральной нервной системе – аркуатное ядро гипоталамуса, на периферии – промежуточная доля гипофиза, из которой пептид секретируется в кровь при стрессе, шоке, травмах и физических нагрузках. b-эндорфин является ключевым фактором, осуществляющим контроль стрессиндуцированных изменений иммунитета со стороны эндогенной опиоидной системы (Зозуля, Пшеничкин, 1990; Pedersen, Hoffman-Goetz, 2000). Роль других соединений из семейства эндогенных опиоидных пептидов, в частности энкефалинов, при стрессе значительно более скромна, а по мнению отдельных авторов (Owens, 1987) вообще отрицается.
Известно (Panerai, Sacerdote, 1997), что изменение концентрации b-эндорфина в головном, спинном мозге и гипофизе часто сочетается с неврологическими и аутоиммунными нарушениями (мигрень, рассеянный склероз, болезнь Крона). Важную роль b-эндорфин играет в патогенезе инфекционных заболеваний, модулируя функции клеток адаптивного и естественного звеньев иммунной системы при их контакте с микроорганизмами и вирусами (Ляшев, 2000; Plotnikoff, 1999; Sitteetal., 2007). В связи с этим изучение роли b-эндорфина в регуляции иммуногенеза представляет большой интерес.
Широкий спектр биологической активности b-эндорфина определяется его способностью взаимодействовать с различными по своей природе сайтами связывания, к которым относятся опиоидные (налоксон-чувствительные) и неопиоидные (налоксон-нечувствительные) рецепторы. Экспрессия опиатных рецепторов трёх основных классов (µ, d, k) и неопиоидного рецептора на клетках различных органов и тканей, в том числе и клетках иммунной системы, доказана методами радиолигандного связывания и детекции соответствующей РНК (Наволоцкая и др., 2004; Madden, 1995;Plotnikoff, 1999;Bidlack, 2000; Krausetal., 2006; Lotschetal., 2006; Sharp, 2006). Подобное распределение участков связывания b-эндорфина объясняет широкий спектр активности данного пептида и указывает на возможность как прямого, так и опосредованного влияния на формирование иммунного ответа (Зозуля, Пшеничкин 1990; Bidlack, 2000; Stanojević etal., 2006).
Нерешенными остаются вопросы, касающиеся изучения роли эндогенной опиоидной системы в стрессиндуцированных изменениях гуморального и клеточноопосредованного иммунитета; различных рецепторов в регуляции выраженности иммунных процессов, индуцируемых эндогенными опиоидами при стрессе, а также на фоне введения двух основных стрессреализующих факторов – глюкокортикоидов и катехоламинов. Малоизученными остаются молекулярные и клеточные механизмы иммунорегуляторного действия b-эндорфина, связанные с эффектами данного гормона на процессы пролиферации, кооперации и дифференцировки клеток иммунной системы, продукцию ряда ключевых цитокинов (g-IFN, IL-4, IL-10, IL-12), являющихся маркерными для регуляторных Т-лимфоцитов 1 и 2 типа (Th1/Th2) и определяющих выбор типа иммунного ответа. В литературе имеются довольно противоречивые данные о влиянии b-эндорфина на функции клеток естественного иммунного ответа (VandenBerghetal., 1994; Petersonetal., 1998; Voccarino, Kastin, 2000; Sacerdote, 2003; Bodnar, Klein, 2006).
Цель настоящей работы – изучение роли опиатергических механизмов в нейроэндокринной регуляции иммуногенеза с оценкой эффектов b-эндорфина на процессы пролиферации, дифференцировки и кооперации клеток иммунной системы.
Основные задачи исследования
1. Изучить роль основных компонентов эндогенной опиоидной системы в регуляции процессов иммуногенеза в условиях острого стресса.
2. Исследовать возможность опосредованности иммунорегуляторных эффектов глюкокортикоидов и катехоламинов через взаимодействие с эндогенной опиоидной системой.
3. Оценить влияние b-эндорфина на функции клеток адаптивного иммунитета и исследовать механизм действия пептида на процессы пролиферации, кооперации и Th1/Th2-дифференцировки лимфоцитов.
4. Изучить роль b-эндорфина в регуляции функций клеток естественного иммунитета.
Научная новизна работы. Экспериментально обоснована интегральная роль эндогенной опиоидной системы в нейроэндокринной регуляции иммуногенеза в норме, в условиях стрессорного воздействии и при введении стрессреализующих гормонов – глюкокортикоидов и катехоламинов. Впервые изучено влияние b-эндорфина на процессы активации, пролиферации, кооперации и Th1/Th2-дифференцировки Т-лимфоцитов с оценкой роли различных клеточных фракций. Выявлен характер участия опиатных рецепторов различных типов в регуляции иммунных реакций под воздействием b-эндорфина и синтетических лигандов опиатных рецепоров пептидной природы. В экспериментах invivo и invitroподтверждено, что основной мишенью b-эндорфина является гуморальное звено иммунного ответа, при этом выявлена зависимость эффектов b-эндорфина от фазы развития иммунной реакции. В модели пролиферативного ответа лимфоцитов обнаружена зависимость эффекта b-эндорфина и селективных агонистов m- и d-рецепторов от концентрации митогена и концентрации исследуемых пептидов. Выявлена ключевая роль d-рецепторов в реализации стимулирующего эффекта b-эндорфина на пролиферацию и продукцию IL-4. Впервые установлена зависимость стимулирующего эффекта опиоидных пептидов на пролиферацию лимфоцитов и продукцию IL-4 от присутствия моноцитов в клеточной культуре. Обнаружено, что b-эндорфин снижает степень выраженности реакции бласттрансформации лимфоцитов при удалении моноцитов из клеточной культуры. Показано, что b-эндорфин стимулирует фагоцитарную активность эффекторов естественного иммунитета и оказывает модулирующее влияние на цитокинпродуцирующую функцию моноцитов и нейтрофилов. Изучен характер участия опиатных рецепторов в регуляции этих процессов.
Теоретическая и практическая значимость. Полученные данные расширяют представление о роли b-эндорфина и опиатных рецепторов разных типов в регуляции иммуногенеза. Обосновано, что формирование иммунного ответа в норме и при стрессе, а также регуляция адаптивного и естественного иммунного ответа реализуется за счёт механизмов, связанных с синтезом опиоидных пептидов. Выявлен механизм влияния опиоидных пептидов на процессы Th1/Th2-дифференцировки Т-лимфоцитов. Полученные экспериментальные данные подтверждают целесообразность использования иммуномодулирующих свойств b-эндорфина в терапии ряда аутоиммунных заболеваний (рассеянный склероз, болезнь Крона и пр.). В связи с широким использованием агонистов опиатных рецепторов в практической медицине, необходим учет последствий их применения. Результаты работы используются в лекционном курсе «Экспериментальная иммунопатология и иммунотерапия» на кафедре микробиологии и иммунологии Пермского государственного университета (614990, Пермь, Букирева 15).
Основные положения, выносимые на защиту
1. В условиях блокады опиатных рецепторов выявляется выраженная модификация иммунорегуляторных эффектов ротационного стресса, глюкокортикоидов и катехоламинов.
2. b-эндорфин в высоких дозах угнетает, в низких - стимулирует гуморальное звено иммунитета, и при этом не влияет на выраженность реакции гиперчувствительности замедленного типа. В клеточных культурах b-эндорфин стимулирует пролиферацию лимфоцитов и продукцию IL-4, не влияет на синтез IL-2 и IFN-g, при этом усиливает степень поляризации Т-хелперов в направлении Th2-клеток. В реализации стимулирующих эффектов b-эндорфина на пролиферацию и продукцию IL-4 доминирующая роль принадлежит d-рецепторам.
3. Клетки моноцитарно-макрофагального ряда играют важную регуляторную роль в направленности эффектов b-эндорфина в отношении функциональной активности CD4+ лимфоцитов.
4. b-эндорфин стимулирует фагоцитарную активность эффекторов естественного иммунитета и оказывает модулирующее влияние на цитокинпродуцирующую функцию моноцитов и нейтрофилов.
Связь работы с крупными программами. Работа проводилась в течение 2000-2007 гг. в соответствии с планом НИР ИЭГМ УрО РАН (номер госрегистрации темы НИР 01.9.009927); в рамках Программы фундаментальных исследований Президиума РАН «Молекулярная и клеточная биология»; гранта РФФИ № 06-04-49001, а также грантов молодых учёных Президиума УрО РАН 2003, 2005 гг.
Апробация работы. Материалы диссертации доложены и обсуждены на Международном симпозиуме «Взаимодействие нервной и иммунной систем в норме и патологии», Санкт-Петербург, 2007; V-VIII конференциях с международным участием «Дни иммунологии в Санкт-Петербурге», Санкт-Петербург, 2001-2007; ХIХ Российском съезде физиологического общества им. И.П. Павлова с международным участием, Екатеринбург, 2004; VI Международной конференции «Проблемы загрязнения окружающей среды», Пермь-Казань, 2005; III съезде Российского научного общества иммунологов, Екатеринбург, 2004; I-V конференциях иммунологов Урала, Екатеринбург, 2001; Пермь, 2002; Челябинск, 2003; Уфа, 2005; Оренбург, 2006; I-II конференциях молодых учёных «Современные проблемы микробиологии, иммунологии и экологии», Пермь, 1999, 2002.
Публикации. Материалы диссертационной работы обобщены в 46 печатных работах, в том числе 15 экспериментальных статьях и 31 материалах конференций.
Объем и структура работы. Диссертация изложена на 251 странице, содержит 35 таблиц, 49 рисунков и состоит из введения, литературного обзора, описания объектов и методов исследования, 5 глав результатов собственных исследований, обсуждения, выводов, списка цитируемой литературы, включающего 448 наименований, в том числе 124 на русском и 324 на английском языках.
Место проведения работы. Работа является частью исследований, выполняемых в аналитической лаборатории ИЭГМ УрО РАН (зав. – к.г.-м.н. М.А. Шишкин) совместно с лабораторией экологической иммунологии (зав. – к.м.н. Б.А. Бахметьев) по изучению механизмов иммуномодулирующих эффектов гормонов, продукция которых изменяется на фоне экологического воздействия. Исследования по проблеме нейроэндокринной регуляции иммуногенеза были инициированы профессором, заслуженным деятелем науки РФ Н.Н. Кеворковым. Научные положения диссертации и выводы, вытекающие из анализа полученного экспериментального материала, базируются на результатах собственных исследований автора.
Автор выражает искреннюю благодарность М.А. Шишкину, к.х.н. С.П. Тендряковой, профессору М.В. Черешневой, за внимание и моральную поддержку. Автор особо признателен сотрудникам группы радиоизотопных исследований к.б.н. Т.А. Баевой, инженеру Е.Г. Чижовой, магистрантам кафедры микробиологии и иммунологии Пермского государственного университета К.Г. Горшковой и И.Л. Шаравьёвой, способствующим завершению настоящей работы и чей вклад в определённые разделы исследований отражён в приведённых в списке литературы публикациях. Автор благодарит главного специалиста Муниципального управления здравоохранением Ростехнадзора, к.м.н. В.Г. Рыжаенкова за помощь в проведении иммуноферментного анализа.
Глубокую благодарность и признательность автор выражает своим учителям и наставникам академику РАН и РАМН В.А. Черешневу и доценту Ю.И. Шилову, оказавшим большое влияние на выбор целей научного поиска и формирование научного мировоззрения автора.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования. В работе использовали белых беспородных мышей массой 20-22 г и лейкоциты периферической венозной крови, полученной от здоровых людей – добровольцев мужского пола в возрасте 19-35 лет.
Для экспериментального моделирования реакции стресс использовали ротационную модель. Ротация мышей производилась в течение 60 мин по 10 мин с перерывами по 5 мин при 78 об/мин. Роль опиатных рецепторов в постстрессорных изменениях иммунных реакций исследовали путем их блокады налоксоном гидрохлоридом и налтриндолом гидрохлоридом. Налоксона гидрохлорид (DuPont, США) в разовой дозе 0,2 мг/кг массы тела и селективный антагонист d-опиатных рецепторов налтриндола гидрохлорид (ICN, США) в дозе 0,1 мг/кг вводили животным подкожно однократно за 20 мин до ротации (Ашмарин, 1988; Михайлова и др., 1992; Croocketal., 1992). В дальнейших экспериментах в системе invivo дозы опиатных антогонистов не изменялись. Иммунизацию животных производили через 1 ч после окончания ротации.
При исследовании иммунорегуляторных эффектов опиоидных пептидов invivo β-эндорфин (Sigma, США) в диапазоне доз от 100 мкг/кг до 0,0005 мкг/кг вводили однократно внутрибрюшинно в объеме 0,2 мл. Контролем для животных, получавших β-эндорфин, служили мыши, которым вводили по той же схеме 0,9% NaCl. μ-агонист DAGO ([d-Ala2 ,N-Me-Phe4 ,Gly5 -ol]-энкефалин и δ-агонист DADLE ([d–Ala2 ,d-Leu5 ] - энкефалин) (Sigma, США) в диапазоне 10 – 0,0001 мкг/кг вводили по схеме аналогичной введению β-эндорфина. Иммунизацию животных производили через 1 ч после введения опиоидных пептидов.
Гидрокортизона ацетат (Гедеон Рихтер, Венгрия) в дозе 50 мг/кг массы тела вводили однократно внутрибрюшинно. Адреналина гидрохлорид (Московский эндокринный завод, Россия) вводили подкожно однократно в дозе 1 мг/кг. Налоксон и селективный антагонист d-опиатных рецепторов налтриндол вводили подкожно за 20 мин до введения гормонов (3 инъекции через 2,5 ч в группе с гидрокортизоном и 1 инъекция в группе с адреналином). Контролем служили интактные мыши, подвергшиеся иммунизации, но не получавшие препаратов. Дополнительным контролем для животных, получавших гидрокортизон и опиоидные пептиды, служили мыши, получавшие по той же схеме изотонический раствор хлорида натрия. Иммунизацию опытных и контрольных мышей проводили одномоментно через 3 ч от начала эксперимента в группах с гидрокортизоном, через 30 мин - в группах с адреналином.
Для моделирования локального иммунного ответа животных иммунизировали эритроцитами барана (108 клеток вводили подкожно в подошвенную поверхность правой стопы). На 4-е сутки вводили разрешающую дозу антигена (108 клеток). На 5-е сутки оценивали выраженность иммунного воспаления при реакции ГЗТ путём регистрации толщины (инженерным микрометром) и массы (на торсионных весах) опытной и контрольной стопы; количество ядросодержащих клеток (ЯСК); интенсивность антителогенеза методом локального гемолиза в геле агарозы (Jerne, Nordin, 1963). Оценку фагоцитарной активности клеток периферической крови, селезенки, регионарного и отдаленного подколенных лимфатических узлов проводили методом В.Н. Каплина с соавт. (Каплин, 1992, 1996) в модификации (Шилов и др., 1997, 1998).
Нефракционированную клеточную взвесь получали путём отстаивания верхнего слоя плазмы крови с лейкоцитами. Выделение фракции мононуклеаров и нейтрофилов проводили на градиенте плотности фиколл-верографин. Разделение моноцитов и лимфоцитов проводили методом адгезии на чашках Петри. CD4+ Т-клетки выделяли при помощи набора магнитных бус DynabeadsM-450 CD4 (Invitrogen, США). Культивирование клеток проводили в течение 24, 48 и 72 ч в пластиковых 24 и 96-луночных планшетах (OrangeScientific, Бельгия) в соответствии с традиционными методиками с использованием полной питательной среды, приготовленной на основе RPMI 1640 или среды 199 (Биолот, Россия) с добавлением 10 mM HEPES, 2 mM L-глутамина (Sigma, США), 100 мкг/мл гентамицина и 10% эмбриональной телячьей сыворотки (Биолот, Россия) или аутоплазмы во влажной атмосфере с 5% СО2 при 370 С.
Пролиферативную активность оценивали по включению 3 H-метилтимидина. Радиоактивность проб определяли на жидкостном сцинтилляционном счетчике Guardian (Wallac, Финляндия). Для определения концентрации IL-1β, TNF-a, IL-6, IL-8, IL-1ra, IL-2, IL-4 и IFN-γ в супернатантах культур клеток использовали спектрофотометр Униплан (Пикон, Россия) и иммуноферментные тест-системы производства ООО Протеиновый контур, ООО Цитокин, Санкт-Петербург, Вектор-Бест, Новосибирск. В экспериментах invitro использовали агонист δ,μ-опиатных рецепторов β-эндорфин в концентрациях 10-7 -10-12 М; меланотропин потенцирующий фактор (MPF) -фрагмент 88-91 β-липотропина (Lys-Lys-Gly-Glu) в концентрациях 10-7 -10-12 М; μ-агонист опиатных рецепторов DAGO ([d-Ala2 ,N-Me-Phe4 ,Gly5 -ol]-энкефалин) в концентрациях 10-7 – 10-12 М; δ-агонист опиатных рецепторов DADLE ([d–Ala2 ,d-Leu5 ]-энкефалин) в концентрациях 10-7 –10-12 М; неселективный антагонист опиатных рецепторов налоксона гидрохлорид и селективный антагонист δ-рецепторов налтриндола гидрохлорид в концентрациях 10-6 , 10-8 , 10-10 М; липополисахарид (ЛПС) Escherichia coli O26:B6 - 0,1 мкг/мл (Sigma, США), фитогемагглютинин (ФГА) – 1,25; 2,5; 5,0; 10,0; 20,0 мкг/мл (Sigma, США), диклофенак натрия (ДН) 25 мкг/мл, моноклональные анти-IL-1b антитела – 2 мкг/мл.
Полученные данные обрабатывали с помощью многофакторного дисперсионного анализа для парных данных и корреляционного анализа. Достоверность различий между группами оценивали с помощью t-критерия Стьюдента и критерия Фишера наименьшей значимой разницы. Сортировку и обработку данных проводили на компьютере IBM PC c использованием программ StatisticaforWindows 6.0 (Statsoft, Inc., США) и DIASTA (Московский государственный университет, Россия).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ И ИХ ОБСУЖДЕНИЕ
Влияние ротационного стресса на показатели иммунитета. Роль опиатных рецепторов. В большинстве опубликованных работ, посвященных изучению влияния стресса на иммунный ответ, исследуются изменения системного иммунного ответа в условиях внутривенной или внутрибрюшинной иммунизации. Принимая во внимание разные компоненты внутрисистемной регуляции общих и локальных форм иммунного ответа, представлялось целесообразным исследование эффектов стресса и блокады опиатных рецепторов в условиях развития локальной формы иммунного ответа.
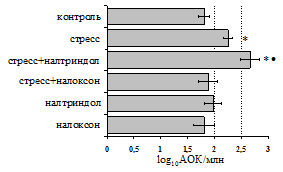
Как видно из рис. 1, в индуктивную фазу иммунного ответа на фоне стресса наблюдается увеличение числа АОК в лимфатическом узле (ЛУ) и усиление степени выраженности реакции ГЗТ. Блокада δ-опиатных рецепторов приводит к ещё более выраженной активации антителогенеза, в то время как
А Б

В Г


Рис. 1. Влияние ротационного стресса в условиях блокады опиатных рецепторов на абсолютное (А) и относительное (Б) число АОК, количество ЯСК в регионарном лимфатическом узле (В) и выраженность реакции ГЗТ (Г) в индуктивную фазу иммунного ответа. Здесь и на рис. 2: * - p<0,05 к контролю; • - p<0,05 к стрессу.
на фоне налоксона стимулирующий эффект ротационного стресса на антителогенез отменяется. Стрессиндуцированное усиление выраженности реакции ГЗТ отменяется как налоксоном, так и налтриндолом. Изолированное введение животным налтриндола или налоксона на количество АОК и степень выраженности ГЗТ влияния не оказывает. В эффекторную фазу иммунного ответа ротационный стресс (рис. 2) стимулирует как клеточный, так и гуморальный ответ, однако, в отличие от индуктивной
8-09-2015, 23:00
