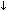Умеренное снижение пневматизации легких, различимы воздушные бронхограммы, границы сердца чёткие (Рис.4).

Рисунок 4 Рентгенограмма грудной клетки в прямой проекции в горизонтальном положении. ( Диагностика и лечение РДС недоношенных // метод. Рекомендация, 2007)
Снижение пневматизации легких, воздушные бронхограммы, границы сердца на рентгенограмме ещё различимы (Рис.5).
Выраженное снижение пневматизации легких, воздушные бронхограммы, границы сердца практически не различимы, стёрты (Рис.6).
Резкое снижение пневматизации легких, воздушные бронхограммы, границы сердца не различимы, "белые лёгкие" (Рис.7).
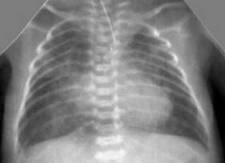
Рисунок 5. РДС. Рентгенограмма в прямой проекции, в горизонтальном положении. Верхние доли легких и средняя доля справа неоднородно слабоинтенсивно затемнены, корни легких расширены, не структурны. Сосудисто-интерстициальный рисунок легких деформирован, усилен, размыт. Тень средостения с нечётким контуром, протекционно смещена влево за счёт подворота. ( Диагностика и лечение РДС недоношенных // метод. рекомендация, 2007)
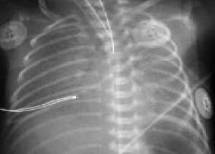
Рисунок 6. РДС. Рентгенограмма грудной клетки в прямой проекции, в горизонтальном положении. Интенсивное мелкоточечное затемнение легочных полей - с-м "матового стекла", на фоне которого не дифференцируется тень средостения. Визуализируются линейные просветления, обусловленные заполненными воздухом бронхами - "воздушная бронхограмма". ( Диагностика и лечение РДС недоношенных // метод. рекомендация, 2007)
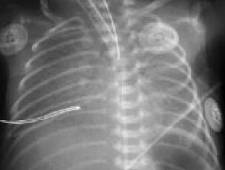
Рисунок 7 . РДС. Рентгенограмма грудной клетки в прямой проекции, в горизонтальном положении. Интенсивное мелкоточечное затемнение легочных полей - симптом "матового стекла", на фоне которого не дифференцируется тень средостения. Визуализируются линейные просветления, обусловленные заполненными воздухом бронхами - "воздушная бронхограмма". ( Диагностика и лечение РДС недоношенных // метод. рекомендация, 2007)
Дифференциальная диагностика.
Транзиторное тахипное новорождённых (синдром влажных легких, респираторный дистресс - синдром II типа). Диагноз ставится на основании данных анамнеза (кесарево сечение, астма у матери, избыточное назначение жидкости) и характерной рентгенологической картины (Рис.8). Заболевание чаще всего протекает доброкачественно и не требует инвазивной респираторной поддержки.
Синдром острого легочного повреждения (респираторный дистресс - синдром взрослого типа (Рис.9)). Всегда осложнение другого заболевания (пневмония, мекониальная аспирация, сепсис, шок, длительное экстракорпоральное кровообращение).
Идиопатическая легочная гипертензия новорождённых (синдром персистирующего фетального кровообращения) (Рис.10). Диагноз ставится на основании рентгенологической картины (обеднение сосудистого рисунка, "синдром чёрных легких") и данных эхокардиографии (право - левый шунт или бидиректоральный ток крови по фетальным коммуникациям).
Дифференциальный диагноз проводят с дыхательными расстройствами как легочного (пневмонии, пороки развития легких и др.), так и нелегочного генеза (вторичные дыхательные расстройства - внутричерепная родовая травма головного или спинного мозга, врожденные пороки сердца, диафрагмальная грыжа, полицитемия, метаболические нарушения и др.). Дифференциальная диагностика с пневмониями изложена ниже.
Агенезия хоан обусловливает невозможность дышать носом и появление цианоза, расстройств дыхания после нормального первого вдоха. Типичны обильные слизистые выделения, заполняющие нос. Порок развития становится очевидным, когда не удается провести катетер или зонд через нос в носоглотку. Лечение хирургическое, но сразу же вводят воздуховод в рот.
Трахеопищеводные свищи клинически проявляются поперхиванием, приступами цианоза, кашлем, появлением хрипов в легких в момент кормления или сразу после него. Контрастное исследование пищевода (с водорастворимым контрастным веществом) и бронхоскопия подтвердят диагноз.
Диафрагмальная грыжа выявляется при рождении или вскоре после него нарастающим тяжелым расстройством дыхания.
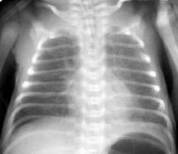
Рисунок 8. Синдром задержки жидкости в легких. Рентгенограмма в прямой проекции, в горизонтальном положении. Сосудисто-интерстициальный рисунок легких размыт на фоне симметричного слабоинтенсивного снижения прозрачности легочных полей. Контуры средостения нечёткие. ( Диагностика и лечение РДС недоношенных // метод. рекомендация, 2007)
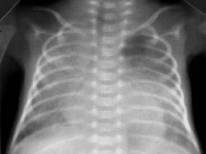
Рисунок 9. РДС взрослого типа. Рентгенограмма в прямой проекции, в горизонтальном положении. Визуализируется слабоинтенсивное затемнение верхней и средней доли правого лёгкого и нижней доли слева. На фоне затемнения дифференцируются более плотные участки, сосудисто-интерстициальный рисунок нечёткий (Диагностика и лечение РДС недоношенных // метод. рекомендация, 2007)
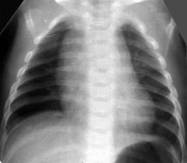
Рисунок 10. Персистирующая легочная гипертензия новорождённого. Рентгенограмма грудной клетки в прямой проекции. Тень средостения расширена в верхнем этаже, имеет чёткие, не ровные контуры. ( Диагностика и лечение РДС недоношенных // метод. рекомендация, 2007)
Типичен малый ладьевидный живот, втянутая передняя брюшная стенка при рождении. При осмотре обращают на себя внимание асинхронные движения правой и левой половины грудной клетки и смещение верхушечного толчка сердца, чаще вправо (ибо левосторонняя диафрагмальная грыжа встречается в 5 - 1 0 раз чаще, чем правосторонняя), резкое укорочение перкуторного тона в нижнем отделе легкого и отсутствие здесь же дыхательных шумов, внезапный цианоз при положении ребенка на здоровом боку. Решающее диагностическое значение имеет рентгенография грудной клетки, которая показывает наличие в грудной клетке структур, ей несвойственных (кишечник, печень и др.). Лечение хирургическое.
У детей с родовой травмой головного и спинного мозга, наряду с расстройствами дыхания, отмечаются и признаки поражения ЦНС. Помогают своевременной диагностике патологии мозга и вспомогательные исследования: нейросонография, рентгенография позвоночника, люмбальная пункция и др.
Врожденные пороки сердца синего типа и синдром персистирующей фетальной циркуляции иногда трудно отличить от РДС. Однако в первые часы жизни у детей с РДС зачастую обычный цвет кожных покровов. При использовании 100% кислорода для дыхания в течение 10-15 мин, особенно при постоянном положительном давлении в воздухоносных путях, у детей с РДС РаО2 повышается, иногда даже выше 100, тогда как при пороках сердца синего типа этого не происходит. Безусловно, имеют значение и данные клинического осмотра, аускультации, оценка по шкале Сильвермана, а также дополнительных исследований (рентгенография грудной клетки, ЭКГ, результаты эхокардиографии).
Пневмонии, вызванные стрептококками В, другими стрептококками (пептострептококки, энтерококки), дают клиническую картину, практически не отличимую от БГМ, ибо вызывают ингибирование сурфактанта и отсюда его дефицит. Диагностическое значение в этом случае имеет выявление других инфекционных очагов (менингит и др.), результаты клинических анализов крови, посевов крови, содержимого трахеи.
Прогнозирование.
Наиболее часто РДС отмечается у глубоко недоношенных детей при гестационном возрасте менее 34 недель. Однако существует группа угрожаемых по развитию РДС новорожденных, родившихся в более поздние сроки беременности. К ним относятся дети, родившиеся у матерей с сахарным диабетом и другими эндокринопатиями при многоплодной беременности, изосерологической несовместимости крови матери и плода, при кровотечениях в связи с отслойкой и предлежанием плаценты. Большую группу составляют новорожденные с морфофункциональной незрелостью, возникшей под влиянием неблагоприятных факторов внешней среды или в результате плацентарной недостаточности, врожденной и наследственной патологии плода, а также дети, родившиеся в асфиксии. Прогностическим критерием является определение в крови беременных женщин уровня альфа-фетопротеина (Таблица №3). Повышение его концентрации выше 75-го перцентиля указывает, помимо нарушения процесса формирования и развития плода во II и в начале III триместра, на отставание зрелости плода по отношению к гестационному возрасту.
Таблица № 3
Перцентили альфа-фетопротеина
| Срок беременности, недель | Перцентили | ||||||
| 3 | 10 | 25 | 50 | 75 | 90 | 97 | |
| 13-14 | 1.76 | 3.89 | 7.38 | 12.9 | 20.1 | 27.8 | 36.4 |
| 14-15 | 2.29 | 4.93 | 9.17 | 15,8 | 24.3 | 33.2 | 43.1 |
| 15-16 | 2.95 | 6.22 | 11.4 | 19.3 | 29.3 | 39.7 | 51.2 |
| 16-17 | 3.79 | 7.83 | 14.1 | 23.6 | 35.4 | 47.6 | 60.9 |
| 17-18 | 4,85 | 9.83 | 17.4 | 28.8 | 42.8 | 57.1 | 72.7 |
| 18-19 | 6.17 | 12.3 | 21.5 | 35.2 | 51.8 | 68.7 | 86.8 |
| 19-20 | 7.84 | 15.4 | 26.6 | 43 | 62.7 | 82.6 | 104 |
| 20-21 | 9.93 | 19.2 | 32.8 | 52.5 | 75.9 | 99.5 | 125 |
| 21-22 | 12.5 | 24 | 40.5 | 64.1 | 92 | 120 | 150 |
| 22-23 | 15.8 | 29.8 | 49.9 | 78.3 | 112 | 145 | 180 |
| 23-24 | 19.2 | 35.8 | 59.2 | 92.2 | 131 | 169 | 208 |
| 24-25 | 21.9 | 40.4 | 66.4 | 102 | 144 | 185 | 228 |
| 25-26 | 24.8 | 45.2 | 73.6 | 113 | 158 | 202 | 248 |
| 26-27 | 27.7 | 50 | 80.7 | 123 | 171 | 218 | 266 |
| 27-28 | 30.4 | 54.4 | 87.2 | 132 | 183 | 232 | 283 |
| 28-29 | 32.9 | 58.3 | 92.8 | 139 | 192 | 243 | 295 |
| 29-30 | 35 | 61.5 | 97.2 | 145 | 199 | 251 | 304 |
| 30-31 | 36.6 | 63.8 | 100 | 149 | 203 | 255 | 308 |
| 31-32 | 37.6 | 65.1 | 102 | 150 | 204 | 255 | 308 |
| 32-33 | 38 | 65.3 | 101 | 149 | 201 | 251 | 302 |
| 33-34 | 37.7 | 64.4 | 99.3 | 145 | 196 | 244 | 292 |
| 34-35 | 36.8 | 62.5 | 95.8 | 139 | 187 | 233 | 278 |
| 35-36 | 35.4 | 59.7 | 91.1 | 132 | 177 | 219 | 261 |
| 36-37 | 33.5 | 56.1 | 85.2 | 123 | 164 | 202 | 241 |
| 37-38 | 31.3 | 52 | 78.6 | 113 | 150 | 185 | 220 |
| 38-39 | 28.8 | 47.6 | 71.7 | 102 | 136 | 167 | 198 |
| 39-40 | 26.3 | 43.2 | 64.2 | 92.2 | 122 | 149 | 177 |
Пренатальная профилактика.
Всем беременным со сроком гестации 24-34 недели при угрозе преждевременных родов назначается один курс кортикостероидов и могут использоваться 2 схемы пренатальной профилактики РДС.
При угрозе преждевременных родов предпочтительнее антенатальное введение бетаметазона. Его использование продемонстрировало более быструю стимуляцию "созревания" в легких плода системы синтеза сурфактанта. Максимальный профилактический эффект при использовании бетаметазона наблюдается на 24 часа раньше, чем при использовании дексаметазона (через 48 часов против 72 часов от начала курсового введения). В отличие от дексаметазона, в многоцентровых исследованиях показана профилактическая эффективность однократного введения бетаметазона (неполный курс) и относительная безопасность при повторных курсах антенатального лечения. Кроме того, антенатальное введение бетаметазона способствует снижению частоты ВЖК и ПВЛ у недоношенных детей с гестационным возрастом более 28 недель, приводя к достоверному уменьшению их перинатальной заболеваемости и смертности.
Бетаметазон - 12мг В/М через 12 часа, всего 2 дозы на курс
Дексаметазон - 6мг В/М через 6 часов, всего 4 дозы на курс
Лечение должно ограничиваться одним курсом.
Показано, что повторные курсы дексаметазона увеличивают риск развития ПВЛ и тяжёлых нервно-психических нарушений к 2-х летнему возрасту.
При возникновении преждевременных родов в сроке 24-34 недели гестации следует предпринять попытку торможения родовой деятельности путём применения токолитиков. При этом преждевременное излитие околоплодных вод не является противопоказанием к торможению родовой деятельности и профилактическому назначению кортикостероидов.
Лечение.
Основные методы респираторной терапии РДС новорождённых.
Диапазон методов поддержания газообмена у детей с дыхательными расстройствами достаточно широк и поэтому требует систематизации.
Все методы респираторной терапии можно подразделить на несколько групп и, по мере увеличения их интенсивности, расположить в следующем порядке:
Метод |
Поток и концентрация | Преимущества | Недостатки |
Носовые канюли |
Маленький = 0.5л/мин. Средний = 0.5-1 л/мин. Большой = >1 л/мин. |
Требуется низкий поток кислорода Если использовать правильно, создается постоянная концентрация кислорода |
Необходимо иметь специальные канюли для новорожденных Необходимо иметь специальный дозатор маленького потока кислорода Подача холодного кислорода в легкие ребенка |
Носовой катетер |
Маленький = 0.5л/мин. Средний = 0.5-1 л/мин. Большой = >1 л/мин. |
Требуется низкий поток кислорода Если использовать правильно, создается постоянная концентрация кислорода |
Необходимо иметь специальный дозатор маленького потока кислорода Подача холодного кислорода в легкие ребенка |
Кислородная палатка (кислородный колпак) |
Маленький = 3 л/мин. Средний = 3-5 л/мин. Большой = >5 л/мин. |
Согревает кислород Можно создать высокую концентрацию |
Требуется высокий поток кислорода, чтобы достичь желаемую концентрацию |
Лицевая маска |
Маленький = 1 л/мин. Средний = 1-2 л/мин. Большой = >2 л/мин. |
Можно быстро осуществить подачу кислорода Удобна для подачи кислорода в течение короткого времени |
Возможно накопление углекислого газа, если поток кислорода или маска слишком маленькие Трудно кормить ребенка, когда наложена маска Трудно фиксировать маску на месте |
Инкубатор |
Если внутри инкубатора используется кислородный колпак, см. выше Если кислород подается непосредственно в инкубатор, следуйте инструкции производителя |
Согревает кислород |
Неудобства подачи кислорода в инкубатор: Требуется высокий поток кислорода, чтобы создать желаемую концентрацию Трудно поддерживать концентрацию кислорода, дверца инкубатора открыты для ухода за ребенком и выполнения процедур |
(Решение проблем новорожденных, ВОЗ, Женева 2005)
Применение CPAP в терапии РДС новорождённых.
Определение и принцип действия. СРАР - continuous positive airway pressure - постоянное (т.е. непрерывно поддерживаемое) положительное давление в дыхательных путях. Препятствует спадению альвеол и развитию ателектазов. Может быть установлено в качестве положительного давления в конце выдоха при проведении ИВЛ или являться самостоятельным методом респираторной поддержки у новорождённых с сохранённым спонтанным дыханием.
Постоянное положительное давление увеличивает функциональную остаточную ёмкость легких (ФОЕ), снижает резистентность дыхательных путей, улучшает растяжимость легочной ткани, способствует стабилизации и синтезу эндогенного сурфактанта.
Существует большое количество специального оборудования для проведения СРАР у новорождённых.
СРАР может проводиться через:
Интубационную трубку, установленную в трахеи (в настоящее время не рекомендуется)
Мононазальную канюлю (назофарингеальную трубку)
Назальную маску
Биназальные канюли
По данным рандомизированных исследований проведение СРАР через биназальные канюли или назальную маску обеспечивает наименьшую работу дыхания у новорождённого.
Специализированные системы разделяют на классические полуоткрытые и открытые. В полуоткрытых системах СРАР выдох производится в дыхательный контур, который запирается клапаном выдоха, создающий положительное давление в дыхательных путях. Таким устройством может быть механический клапан или обычный сосуд с водой. В открытых системах выдох производится во внешнюю среду, и положительное давление создаётся за счёт противопотока, т.е. выдох совершается против основного потока, поступающего к пациенту.
Постоянное положительное давление может генерироваться:
Аппаратом ИВЛ
Водяным замком (Buble CPAP) (Рис.11)
Генератором вариабельного потока
Очень важную роль играет характеристика потока, поступающего к пациенту в такой системе. В классических системах, как правило, поток постоянный. Для создания давления необходимо устанавливать скорость потока от 3 до 7 литров в минуту. В открытых системах поток постоянно изменяет своё направление либо к пациенту, либо в сторону выдоха пациента, поэтому его называют изменчивым или вариабельным. Такая характеристика потока в большей степени облегчает выдох новорождённого и таким образом снижает работу дыхания пациента (рис.12). В открытых системах СРАР для создания адекватного давления требуется больший поток от 6 до 10 литров в минуту.
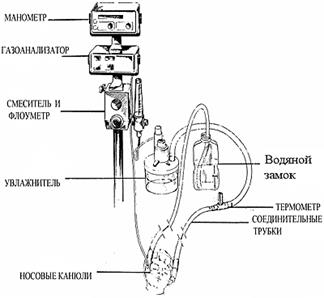
Рисунок 11. Система СРАР с водяным замком (Buble CPAP)
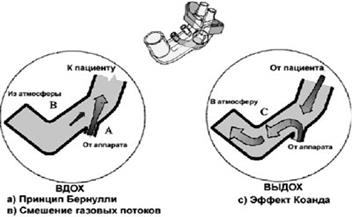
Рисунок 12. Принцип работы генератора вариабельного потока
Преимущества и недостатки различных способов проведения назального CPAP представлены в таблице 4.
Таблица 4
Сопоставление преимущества и недостатков различных способов проведения назального CPAP у новорождённых детей
| Оборудование и канюли | Теоретические преимущества |
| Bubble СРАР - Короткие назальные канюли - Длинные назальные канюли Обычный вентилятор - ЭТТ - Назальные канюли Вариабельный поток (IF) - Назальные канюли - Назальная маска | Bubble СРАР - Дёшево Вызывают осцилляции, которые не влияют на элиминацию СО2 Обычный вентилятор - Дёшево Вариабельный поток (IF) - Наиболее стабильное давление CPAP - Наименьшая работа дыхания |
(Диагностика и лечение РДС недоношенных // метод. Рекомендация, 2007)
Показания и противопоказания.
Профилактическое или раннее (в течение первых 30 минут жизни) применение СРАР - характеризуется началом терапии в родильном зале сразу после рождения и применяется для профилактики и лечения РДС.
Показания: всем новорождённым с гестационным возрастом 32 недели и менее при наличии у них самостоятельного дыхания, необязательно регулярного. При отсутствии у недоношенного самостоятельного дыхания рекомендуется проведение масочной ИВЛ, а после восстановления самостоятельного дыхания начинается СРАР.
Применение СРАР в родильном зале противопоказано детям:
· С атрезией хоан или другими ВПР челюстно-лицевой области, препятствующими правильному наложению назальных канюль
· С диагностированным пневмотораксом
· С врождённой диафрагмальной грыжей
· С врождёнными пороками развития, несовместимыми с жизнью (аненцефалия и т.п.)
· Родившимся в тяжёлой асфиксии (в состоянии шока)
Терапевтическое использование СРАР - показано в случаях, когда у ребёнка начинают развиваться дыхательные нарушения и нарастает зависимость от кислорода.
Перевод на назальный СРАР после экстубации - позволяет сократить длительность искусственной вентиляции легких и снизить риск повторной интубации.
Показания:
· наличие регулярного самостоятельного дыхания
· FiO2 менее 30-35%
· МАР менее 7 см Н2 О
Применение СРАР для предотвращения апноэ - используется у самостоятельно дышащих новорождённых, имеющих эпизоды апноэ любого генеза не более шести раз в час.
Мониторинг. После начала СРАР необходимо организовать непрерывное наблюдение за ребёнком с использованием стандартного и специального (контроль функции дыхания) неонатального мониторинга, а также назначить рентгенологическое исследование легких.
Порядок и варианты проведения CPAP.
При проведении новорождённому метода СРАР обязательна постановка зонда в желудок для декомпрессии. Стандартный алгоритм изменения параметров СРАР может применяться при любом способе проведения данной методики. Основным условием лечения с применением СРАР является наличие самостоятельного дыхания. Терапию начинают с 4 см вод. ст. Далее, в зависимости от реакции больного на применение постоянного расправляющего давления, следует изменять параметры. Если состояние ребёнка не улучшается, возможно, увеличение положительного давления в конце вдоха на 1 см вод. ст. до 5-6 см вод. ст. Следующим шагом может быть увеличение фракции кислорода во вдыхаемой смеси.
При стабилизации состояния, больного оставляют на СРАР в течение нескольких часов или дней и продолжают мониторировать основные витальные функции. По мере стабилизации состояния, первым шагом является уход от высоких концентраций кислорода во вдыхаемой смеси, а затем снижается положительное давление в конце выдоха.
Алгоритмы применения CPAP у недоношенных детей различной массы тела представлены в таблицах 5 и 6.
Таблица 5
Алгоритм изменения режимов СРАР при терапии РДС недоношенным с массой тела менее 1200 граммов
стартовое давление - 4 см вод. ст., FiO2 21-25%
|
* У детей с гестационным возрастом менее 26 недель процедура INSURE не проводится. Если ребёнок требует введения сурфактанта, то после введения рекомендуется продолжить ИВЛ до стабилизации пациента и формирования у него достаточных респираторных усилий. (Диагностика и лечение РДС недоношенных // метод. Рекомендация, 2007)
Таблица 6
Алгоритм изменения режимов СРАР при терапии РДС недоношенным с массой тела более 1200 граммов
стартовое давление 4 смН2 О, FiO2 21-25%
Разделы сайта |