Наличие злокачественной опухоли в матке характеризовалось увеличением активности трипсиноподобных протеиназ в сыворотке крови по сравнению с показателями доноров: у женщин в возрасте от 51 до 60 лет – в 1,24 раза, у женщин в возрасте от 61 до 70 – в 2,0 раза. По сравнению с доброкачественными опухолями активность исследуемых протеиназ при наличии злокачественного процесса была выше в 1,4 раза. Следует отметить, что у больных старше 70 летустановили значительно более высокую (в 3,78 раза) протеиназную активность при наличии злокачественной опухоли. В то же время в этой возрастной группе показатели протеиназной активности как при наличии доброкачественного, так и злокачественного процесса, были в 3,3 и в 2,0 раза ниже, чем в других возрастных группах. Это можно объяснить, вероятнее всего, снижением скорости метаболических процессов, свойственных данному возрасту [31].
Снижение протеиназной активности в сыворотке крови при наличии доброкачественной опухоли и увеличение этого показателя в случае злокачественной опухоли может свидетельствовать, с одной стороны, о неспецифичности ответной реакции организма, а с другой - об отличии протеиназ тканей доброкачественной и злокачественной опухолей.
На основании полученных исследоватили предполагают, что наличие достаточно высокой активности трипсиноподобных протеиназ (выше 36,00 нмоль/мин на 1 мг белка) может свидетельствовать о плохом прогнозе заболевания и, вероятно, показания протеиназной активности свыше 100,00 нмоль/мин на 1 мг белка могут свидетельствовать об активно идущих процессах трансформации клеток, которые наблюдаются при аденоматозе (cancer in situ) [6, 15, 41].
Глава 2. Материалы и методы исследования
2.1 Материал исследования
Активность ферментов определяли в сыворотке крови онкологических больных. Кровь брали в первый день после операции из локтевой вены, далее ее инкубировали 30 минут при комнатной температуре, центрифугировали 20 минут при 4000g и получали сыворотку, в которой определяли активность карбоксипептидазы N и ангиотензинпревращающего фермента.
Изучение активности ферментов было проведено у 45 мужчин в возрасте от 49 до 70 лет. Больные были оперированы по поводу опухолей легких, брюшной полости и мочеполовой системы. Они составили три экспериментальные группы. Первая группа – больные торакального отделения (18 человек); вторая – абдоминального отделения (15 мужчин); третья – урологического отделения (12 человек).
Параллельно с нашим исследованием Корниенко Е. М. проводилась работа по определению параметров гемостаза у онкологических больных данных групп, которые мы использовали в своей работе.
2.2 Методы исследования
2.2.1 Метод определения активности карбоксипептидазы N
Активность КПN определяли в сыворотке крови нингидриновым методом [62].
Опытные пробы содержали 20 мкл 3,5 мМ раствора CoSO4 , приготовленного на 100 мМ Трис-HCl буфере, pH 7,6 и 40 мкл препарата фермента. Контрольные пробы содержали 20 мкл 100 мМ Трис-HCl, pH 7,6 и 40 мкл препарата фермента. Пробы преинкубировали 8 мин при 37o C, реакцию начинали прибавлением в опытные пробы 10 мкл гиппурил-арг, приготовленного на 100 мМ Трис-HCl буфере, pH 7,6 (конечная концентрация в пробе 5 мкМ). Реакцию проводили 120 мин при 37o C и останавливали прибавлением 30 мкл 10 % трихлоруксусной кислоты.
Пробы центрифугировали 20 мин при 4000 об/мин, отбирали 50 мкл надосадочной жидкости, приливали 1 мл нингидринового реактива. Далее пробы встряхивали, выдерживали 12 мин на кипящей водяной бане и измеряли оптическую плотность на КФК-2 при 595 нм против H2 O [58].
Активность КПN определяли как разность оптической плотности опытных и контрольных проб и выражали в нмоль аргинина, образовавшегося за 1 мин инкубации в пересчете на 1 мг белка.
Концентрацию белка в пробах определяли биуретовым методом.
2.2.2 Метод определения активности ангиотензинпревращающего фермента
Активность АПФ определяли в сыворотке крови нингидриновым методом по образованию гли-арг из кбз-гли-гли-арг при рН 8,2 как активность, ингибируемую каптоприлом. Препарат фермента (40 мкл) смешивали с 20 мкл 35 мкМ каптоприла в 100 мМ Трис-НСl буфере, рН 8,2, или 20 мкл буфера и преинкубировали 8 мин при 37˚С. Реакцию начинали прибавлением 10 мкл раствора кбз-гли-гли-арг в вышеуказанном буфере (конечная концентрация в пробе 5 мкМ). Через 120 мин реакцию останавливали прибавлением 30 мкл 10% раствора трихлоруксусной кислоты [59]. Пробы центрифугировали 30 мин при 4000 об/ мин. Отбирали 50 мкл надосадочной жидкости и определяли количество образовавшегося гли-арг нингидриновым методом [62]. Пробы колориметрировали на КФК-2 при l=590 нм. Активность АПФ определяли как разность в оптической плотности проб не содержащих и содержащих каптоприл. Активность фермента выражали в нмоль гли-арг, образовавшегося за 1 мин инкубации в пересчете на 1 мг белка.
Концентрацию белка определяли биуретовым методом.
2.2.3 Метод определения содержания белка
Содержание общего белка определяли биуретовым методом. Принцип метода основан на том, что ионы меди в щелочной среде взаимодействуют с пептидными связями белков сыворотки крови с образованием комплекса красного цвета, интенсивность окраски которого пропорциональна концентрации общего белка.
Опытные пробы содержали 50 мкл сыворотки крови и 2,5 мл рабочего раствора биуретового реагента (концентрат биуретового реагента развести дистиллированной водой в соотношении 1:19). Контрольные пробы содержали 50 мкл дистиллированной воды и 2,5 мл рабочего раствора биуретового реагента. В калибровочную пробу добавляли 50 мкл калибровочного раствора общего белка (раствор бычьего сывороточного альбумина с концентрацией 60 г/л с добавлением хлористого натрия 9 г/л и азида натрия 1 г/л).
Содержимое пробирок тщательно перемешивали, избегая образования пены, инкубировали при комнатной температуре (+ 18 - 25![]() С) в течение 30 минут, после чего измеряли величину оптической плотности калибровочной и опытных проб против контрольной пробы при длине волны 540 нм.
С) в течение 30 минут, после чего измеряли величину оптической плотности калибровочной и опытных проб против контрольной пробы при длине волны 540 нм.
Концентрацию общего белка рассчитывали, как отношение оптической плотности опытной пробы к оптической плотности калибровочной пробы умноженная на концентрацию общего белка в калибровочном растворе (60 г/л).
2.3 Статистическая обработка результатов исследования
Достоверность отличий между средними определяли с использованием t-критерия Стьюдента [16, 29, 40]. Корреляционный анализ проводили с помощью программы «Статистика» (версия 6.0).
Глава 3. Результаты и обсуждение
3.1 Исследование активности карбоксипептидазы N в сыворотке крови онкологических больных в раннем послеоперационном периоде
Результаты исследования показали увеличение активности КПN в сыворотке крови онкологических больных торакального и абдоминального отделения в ранний послеоперационный период по сравнению с пациентами урологического отделения (рис. 1).
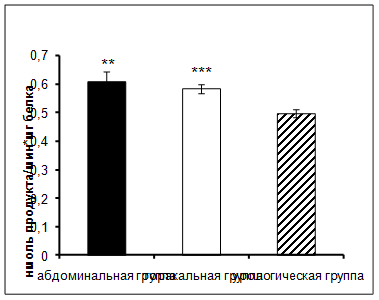
Рис. 1. Активность КПN у онкологических больных в ранний послеоперационный период (нмоль продукта, образовавшегося за 1 мин инкубации на 1 мг белка, M±m, n=12¸18; достоверность отличий: ** – р < 0,01, *** – р < 0,001 относительно урологической группы).
КПNлокализован в плазме крови, обнаружен в стенках кровеносных сосудов. Легкие, желудочно-кишечный тракт имеют обширную капиллярную систему, после операции происходит повреждение этой системы, и вероятно, выход фермента в кровяное русло, что в итоге приводит к увеличению его активности [60].
При проведении корреляционного анализа (табл. 3), была выявлена отрицательная взаимосвязь между активностью КПN и ХЗФ у больных абдоминального отделения. В процессе свертывания крови калликреин расщепляет высокомолекулярный кининоген до активного кинина, который повышает чувствительность фактора XI к действию фактора XIIа [48]. Известно, что КПN участвует в деградации брадикинина [74], вероятно, увеличение активности этого фермента у данной группы больных может способствовать уменьшению свертывания крови по внутреннему пути. Кроме того, фактор Хагемана может включаться в фибринолиз, снижая время лизиса фибринового сгустка.
Обнаружена положительная корреляционная взаимосвязь между активностью КПN и уровнем фибриногена у пациентов урологического отделения. Фибриноген относится к острофазным белкам, концентрация которого резко возрастает в послеоперационный период, что усиливает тромбообразование на данном этапе [8]. Этот белок определяет вязкость плазмы крови, повышает агрегацию тромбоцитов и эритроцитов. Под действием тромбина из фибриногена образуются фибрин-мономеры, из которых впоследствии образуются фибриновый сгусток. Чрезмерное увеличение фибриногена может приводить к повышенному тромбообразованию. КПN, участвуя в инактивации брадикинина, вероятно, сдерживает активацию свертывания крови по внутреннему пути, тем самым способствуя поддержанию фибриногена на нормальном уровне у данной группы больных.
Таблица 3 Корреляционные взаимосвязи параметров гемостаза и карбоксипептидазы N
| Параметры гемостаза | Активность КПN | ||
Абдоминальная группа |
Торакальная группа |
Урологическая группа | |
| КПN | 1,00 | 1,00 | 1,0 |
| АПФ | -0,7 | 0,23 | 0,19 |
| Тромбоциты | 1,00 | -0,43 | -0,27 |
| Время свертывания по Ли-Уайту | 0,60 | 0,37 | -0,20 |
| АПТВ | 0,23 | -0,15 | 0,62 |
| Протромбин | 0,19 | 0,03 | 0,35 |
| Тромбиновое время | -0,78 | 0,17 | 0,38 |
| Растворимый фибрин-мономерный комплекс | 0,78 | -0,13 | -0,64 |
| Фибриноген | 0,82 | 0,11 | 0,96* |
| Хагеман-зависимый фибринолиз | -0,98* | 0,08 | 0,97* |
Достоверность корреляционных взаимосвязей: *– р < 0,05.
Обнаружена также положительная корреляция между активностью КПNи ХЗФ у больных урологического отделения. Известно, что в почечной ткани вырабатывается большое количество активаторов плазминогена. После оперативных вмешательств, особенно по поводу удаления опухолей, в кровь выделяется большое количество компонентов фибринолиза [44]. Вероятно, в данных условиях активность КПN может быть снижена, чтобы сдерживать антикоагуляционные процессы.
3.2 Исследование активности ангиотензинпревращающего фермента в сыворотке крови онкологических больных в раннем послеоперационном периоде
Результаты исследования показали достоверное увеличение активности АПФ в сыворотке крови онкологических больных урологического отделения по сравнению с пациентами абдоминального и торакального отделения (рис.2).
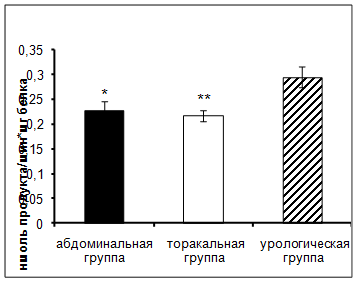
Рис. 2. Активность АПФ у онкологических больных в ранний послеоперационный период (нмоль продукта, образовавшегося за 1 мин инкубации на 1 мг белка, M±m, n=12¸18; достоверность отличий * – р < 0,05, ** – р < 0,01 относительно урологической группы).
АПФ – мембранно-связанный фермент, локализованный преимущественно в тканях почек. Этот фермент является компонентом ренин – ангиотензиновой системы [4, 48]. При повреждении почек, в том числе и хирургического вмешательства, происходит высвобождение АПФ в кровоток, что приводит к увеличению активности фермента.
При проведении корреляционного анализа (табл. 4) была обнаружена отрицательная корреляционная взаимосвязь между активностью АПФ и уровнем РФМК у пациентов абдоминального отделения. У больных, страдающих онкологическим заболеванием, антитромбогенная активность стенок сосудов в процессе роста опухоли снижается, а в раннем послеоперационном периоде обнаруживается повышенная склонность к внутрисосудистому свертыванию крови и тромбообразованию [8, 11, 19, 34, 35].Известно так же, что в эндотелии содержится большое количество активатора плазминогена. Эндотелиальная дисфункция способствует уменьшению этого процесса, что вызывает сдвиг в системе антикоагуляция-коагуляция с преобладанием последней [73]. Участие АПФ в регуляции сосудистого тонуса реализуется через синтез ангиотензина-II, оказывающего мощное вазоконстрикторное действие. Другой механизм, более сопряженный с собственно эндотелиальной дисфункцией, связан со способностью АПФ ускорять деградацию брадикинина. АнгиотензинII является вазопрессором, стимулятором образования свободных радикалов, в частности, супероксидных анионов, которые инактивируют NO, промотируют образование пероксинитрита и снижают эффективность NO-опосредуемой сосудистой дилатации. Т.о., ангиотензин II, способствует развитию эндотелиальной дисфункции, в результате чего усиливается выработка вазоконстрикторов и прокоагулянтов [48]. В результате активируется система свертывания, компонентом которой является РФМК. В то время как брадикинин стимулирует синтез NO в эндотелии, участвуя в дилатациисосудовиусиливаяскоростьместногокровотока. Вероятно,
Таблица 4 Корреляционные взаимосвязи параметров гемостаза и ангиотензинпревращающего фермента
| Параметры гемостаза | Активность АПФ | ||
Абдоминальная группа |
Торакальная группа |
Урологическая группа |
|
| КПN | -0,7 | 0,23 | 0,19 |
| АПФ | 1,00 | 1,00 | 1,00 |
| Тромбоциты | -0,72 | 0,55 | -0,45 |
| Время свертывания по Ли-Уайту | -0,92 | -0,20 | -0,31 |
| АПТВ | -0,54 | 0,24 | 0,78 |
| Протромбин | 0,41 | 0,71* | 0,48 |
| Тромбиновое время | 0,89 | 0,00 | 0,77 |
| Растворимый фибрин-мономерный комплекс | -0,99** | -0,39 | -0,73 |
| Фибриноген | 0,87 | 0,22 | 0,01 |
| Хагеман-зависимый фибринолиз | 0,81 | -0,10 | 0,18 |
Достоверность корреляционных взаимосвязей: *– р < 0,05, ** – р < 0,01. Снижение активности АПФ является компенсаторным механизмом в условиях имеющейся гиперкоагуляции.
Выявлена положительная корреляционная взаимосвязь между активностью АПФ и уровнем ПТИ у больных торакального отделения.
Исследования показали, что у больных злокачественными новообразования легких имеет место активация система гемостаза, осуществляемая преимущественно по внешнему механизму процесса свертывания крови, которая оценивается протромбиновым тестом [44]. Внешний путь начинается с повреждения сосудов и тканей, в результате чего в кровь высвобождается тканевый тромбопластин, которым богата легочная ткань. Этот фактор активирует фактор VII в присутствии ионов Са2+ . Комплекс, состоящий из фактора III, фактора VIIа, ионов Са2+ на поверхности тромбоцитов приводит к активации фактора Х [44]. Известно, что в кровь АПФ попадает из легких. При оперативных вмешательствах, вероятно, инкреция АПФ усиливается, что в свою очередь приводит к генерализованному образованию ангиотензина II, участвующего в агрегации тромбоцитов, на поверхности которых идет процесс внешнего пути свертывания крови. Кроме того, в результате хирургического вмешательства происходит не только высвобождение факторов свертывания крови, но и повреждение эндотелия сосудов, что в свою очередь приводит к изменению активности АПФ, так как он участвует в синтезе коллагена и может таким образом усиливать фиброз [22, 68], активируя тем самым свертывающую систему, компонентом которой является протромбин.
Выводы
1. Обнаружено увеличение активности карбоксипептидазы N у торакальной и абдоминальной групп по сравнению с урологической группой онкологических больных в раннем послеоперационном периоде.
2. Обнаружено увеличение активности ангиотензинпревращающего фермента у урологической группы пациентов по сравнению с абдоминальной и торакальной группами онкологических больных в раннем послеоперационном периоде.
3. Выявлены корреляционные взаимосвязи между активностью карбоксипептидазы N и ангиотензинпревращающего фермента и показателями гемостаза в раннем послеоперационном периоде.
4. Изучаемые ферменты принимают участие в процессах гемостаза у онкологических больных в раннем послеоперационном периоде.
Список литературы
1. Азарян А.В. Пептидгидролазы нервной системы и их биологические функции // Ереван: Анастан, 1989.
2. Акоев И. Г., Биофизика познает рак. — М.: Наука, 1988. —160 с, 17 ил. — (Серия «От молекулы до организма»).
3. Албертс Б., Брей Д., Льюис Дж., Рэфф М., Роберте К., Уотсон Дж.Молекулярная биология клетки: В 3-х т. 2-е изд., перераб. и доп. Т. 3. Пер. сангл. – М.: Мир, 1994. – 504 с.
4. Альтшулер Б.Ю., Ройтман А.П., Долгов В.В. Методические аспекты определения ангиотензинпревращающего фермента // Клиническая лабораторная диагностика. – 2000.–№12. –С. 10– 14.
5. Антонова Л.В., Годенова Н.В., Земнюкова Н.А., Дудкина Н.Е. Опыт использования ортофенантролинового теста в диагностике синдрома ДВС в крови у пациенток с онкологическими заболеваниями репродуктивной сферы. // Медицина в Кузбассе. – 2004. –№11. – С. 26– 27.
6. Бакшеев Н.С., Ильяшенко Н.А.,Миляновский А.И. в кн. Злокачественные новообразования женских половых органов. – М., 1987. –С. 85– 187.
7. Баркаган З.С. Введение в клиническую гемостазиологию. – М.: Ньюдиамед, 1998. – 290 с.
8. Баркаган З. С.Патогенез и терапия нарушений гемостаза у онкологических больных // Терапевтический архив.– 1997. – №7. – С. 65– 67.
9. Баркаган З. С.Антитромботическая профилактика и терапия в онкологии. // MateriaMedica. – 1997. –№ 1 (13). – С. 5-14.
10. Баркаган З. С., Момот А.П. Диагностика и контролируемая терапия нарушений гемостаза. – М.: Ньюдиамед, 2001. – 298 с.
11. Баркаган Л.З. Нарушение гемостаза у детей. – М., 1993.
12. Биохимия: Учеб. Для вузов / В.П. Комов., В.Н. Шведова. – М.: Дрофа, 2004. – 640с.
13. Веремеенко К.Н., Голобородько О.П. Претромботическое состояние. Тромбоз и его профилактика. // Вопр. мед. химии . – 1986. –№ 32. – С. 17– 25.
14. Вернигора А.Н., Генгин М.Т. Протеолитические ферменты: субклеточная локализация, свойства и участие в обмене нейропептидов // Биохимия. –1996,т.6, №5. – С. 771– 785.
15. Гешелин С.А., Вовчук С.В., Близнюк Б.Ф.Нарушения гемостаза и их профилактика в онкологии. // Вопр. Онкологии. – 1986. –№ 30. – С. 9– 18.
16. Гланц С. Медико-биологическая статистика: Пер. с англ. – М, Практика, 1998. – 459с.
17. Городецкий В.М.Неоплазмы и свертывание крови // Гематол. и трансфузиол. – 1994. – № 3. – С.25– 28.
18. Гринштейн Дж., Виниц M., Химия аминокислот и пептидов, пер. с англ., т. 12,M., 1967. – 350 с.
19. Давыдов М. И. Активация гемокоагуляции у больных в критических состояниях // Современная онкология. – 2000. – Т. 2, № 4. – С. 54– 58.
20. Долгов В.В., Сварин П.В. Лабоараторная диагностика нарушений гемостаза. – М. Изд. Триада, 2005. – 270 с.
21. Дэвени Т., Гергей Я.Аминокислоты, пептиды и белки, пер. с англ.- M.: 1976. – 380 с.
22. Елисеева Ю.Е. Ангиотензинпревращающий фермент, его физиологическая роль. // Вопросы медицинской химии. –2001. –№ 1. – С. 53– 60.
23. Ешкайт X. Аминокислоты, пептиды, белки, пер. с нем. – M.: 1985. – 460 с.
24. Золотокрылина Е.С. // Теоретические и клиническиепроблемы современной реаниматологии: Материалы международного симпозиума, посвящ. 90-летию со дня рожд. акад. В. А.Неговского. – М., 1999. – С. 32– 33.
25. Иванов Е.П. Диагностика нарушений гемостаза. Минск, 1983. – 278 с.
26. Калишевская Т. М., Коломина С. М., Кудряшов Б.А. Свертывающая и противосвертывающая системы крови и их значение при развитии злокачественных новообразований. – М., 1992. – 315 с.
27. Киричук В.Ф., Алипов В. В.Возможности диагностики активации системы гемостаза у больных в критических состояниях по уровню фибринопептида А иD-димера. // Кремлевская медицина. Клинический вестник. – 2005. –№ 2. – С. 73– 76.
28. Кудряшов Б.А. Биологические проблемы регуляции жидкого состояния крови и ее свертывания. –М., 1975.
29. Лакин Г.Ф. Биометрия. – М.: Высш. шк., 1990. – 352с
30. Ленинджер А., Основы биохимии, пер. с англ., т. 1 3, M., 1985.
31. Локшина Л.А. Значение внутрисосудистого свертывания крови в формировании полиорганной недостаточности у хирургических больных в критических состояниях. // Новости анестезиологии и реаниматологии. – 2006. –№ 1. –С. 15– 21.
32. Маджуга А. В., Сомонова О.В., Елизарова А. Л., Свиридова С.П., Мазурина, О.Г., Кашия Ш.Р. Нарушения системы гемостаза у онкологических больных с массивной интраоперационной кровопотерей // Анестезиология и реаниматология. – 2001. – № 5. –С. 50– 52.
33. Макацария А. Д., Бицадзе В. О., Баймурадова С. М., Акиньшина С. М.. Тромбофилия и здоровье женщины. // Сибирский медицинский
8-09-2015, 23:30
