Культуры выращивали на жидкой среде рН 7,3 ± 0,2 при температуре от 30 до 350 С в течение 18-20 часов. Культуры разводили 1:1000 в стерильном 0,9% растворе натрия хлорида изотоническом, вносили по 1 мл в чашки с соответствующими элективными питательными средами для изучаемых тест-штаммов и засевали по методу «сплошного газона». После подсушивания на поверхности агара формировали лунки размером 6,0 мм, в которые вносили растворы исследуемых образцов и препаратов сравнения. Посевы инкубировали при 370 С, учет растущих культур проводили через 24 часа.
Антимикробная активность образцов оценивалась по диаметру зон задержки роста тест-штаммов (мм). Диаметр зон задержки роста меньше 10 мм и сплошной рост в чашке оценивали как отсутствие антибактериальной активности, 10-15 мм – слабая активность, 15-20 мм – умеренно выраженная активность, свыше 20 мм – выраженная. Каждый образец испытывался в трех параллельных опытах. Статистическую обработку проводили методами параметрической статистики с вычислением средней арифметической и стандартной ошибки.
3. Разработка состава и технологии фитопленок для лечения термических ожогов
3.1 Разработка состава лекарственной пленки
Для выбора состава лекарственной пленки для лечения термических ожогов нами разработано 4 модели фитопленок на основе натрий-карбоксиметилцеллюлозы, желатина, поливинилпирролидона и поливинилового спирта, обладающих пленкообразующими свойствами, в качестве фитокомплекса использовали смесь сока подорожника, настойки эхинацеи и полифитового масла, которые обладают противовоспалительными, регенеративными, антибактериальными и ранозаживляющими свойствами, в соотношении 1:1:1. Соствы моделей представлены в таблице 1.
Таблица 1
Состав моделей фитопленок
№ модели |
Содержание компонентов, % | |||||||
| Na-КМЦ | Жела- тин |
ПВП | ПВС | Вода | Гли- церин |
Полифитовое масло |
Фитокомп-лекс | |
| 1 | 7 | - | - | - | 73,1 | 2,3 | 6,2 | 11,4 |
| 2 | - | 7 | - | - | 73,1 | 2,3 | 6,2 | 11,4 |
| 3 | - | - | 7 | - | 73,1 | 2,3 | 6,2 | 11,4 |
| 4 | - | - | - | 7 | 73,1 | 2,3 | 6,2 | 11,4 |
Пленкообразователи моделей изготовлены различными способами.
Пленкообразователь модели 1: готовили раствор пленкообразователя: натрий-КМЦ взвешивали на аналитических весах типа ВЛР-200 в количестве 7,0 г. и заливали подогретой до 55±50 С дистиллированной водой в количестве 0,2-0,5 ч. от требуемого, оставляли для набухания на 30 мин. и добавляли остальную уже холодную воду и смесь тщательно перемешивали до получения однородного раствора. Далее приготовление пленки проводили по нижеуказанной методике. Полученные пластины представляли собой однородные, пластичные, прочные без разрывов пленки темно-коричневого цвета, со специфическим запахом и толщиной 0,030 см.
Для получения пленкообразователя модели 2 готовили раствор пленкообразователя: желатин взвешивали на аналитических весах типа ВЛР-200 в количестве 7,0 г. и заливали холодной дистиллированной водой в количестве 0,2-0,5 ч. от требуемого,оставляли для набухания на 40 мин. С истечением времени раствор подогревали на паровой бане и добавляли остальную воду , смесь тщательно перемешивали до получения однородного раствора. Далее приготовление пленки проводили по нижеуказанной методике. Полученные пластины представляли собой прочную, эластичную, однородной структуры, прозрачную пленку светло-желтого цвета и тощиной 0,020 см.
Для получения пленкообразователя модели 3 готовили раствор пленкообразователя: ПВП взвешивали на аналитических весах типа ВЛР-200 в количестве 7,0 г. и заливали холодной дистиллированной водой в количестве 0,2-0,5 ч. от требуемого, оставляли для набухания на 30 мин. Добавляли остальную воду, смесь тщательно перемешивали до получения однородного раствора. Далее приготовление пленки проводили по нижеуказанной методике. Полученные пластины представляли собой пластичную, эластичную, однородной структуры, прозрачную, слегка липкую пленку желтоватого цвета и толщиной 0,032 см.
Для получения пленкообразователя модели 4 готовили раствор пленкообразователя: ПВС взвешивали на аналитических весах типа ВЛР-200 в количестве 7,0 г, заливали холодной дистиллированной водой в количестве 0,2-0,5 ч. от требуемого и раствор подогревали на паровой бане, затем добавляли остальную воду и смесь тщательно перемешивали до получения однородного раствора.
Далее изготовление фитопленки проходит по общей схеме: смесь фильтровали через стеклянный фильтр и в полученный раствор вводили пластификатор – глицерин, предварительно отвешенный в количестве 2,3 г. и смесь сока подорожника, настойки эхинацеи и полифитового масла в равном соотношении 1:1:1, в количестве 17,6 г. Полученный раствор размешивали до гомогенного состояния и разливали на стеклянные подложки, предварительно обработанные этиловым спиртом.
Сушку пленочной массы производили при комнатной температуры до остаточной влажности 5%. Из ФП общей площадью 35 см2 высекали по 6 дисков диаметром 1,5±0,1 см. Полученные пластины представляли собой прочные, эластичные, однородные, без разрывов пленки светло-желтого цвета, со специфическим запахом и толщиной 0,030 см.
Влияние пленкообразователя на качество лекарственной пленки
Учитывая требования, предъявляемые к полимерным основам пленочных лекарственных форм (высокая паро-, газопроницаемость, растворимость в воде и тканевых жидкостях, способность впитывать большое количество влаги, эластичность, достаточная механическая прочность) нами предварительно был произведен подбор полимерных основ.
В первую очередь было изучено влияние состава на органолептические и технологические свойства пленок. Качество пленок оценивали по следующим показателям: эластичность, прочность, однородность и отсутствие разрывов. Результаты исследования представлены в таблице 2.
Таблица 2
Зависимость качества полученной пленки от исходного пленкообразователя
| № модели исходного пленкообразователя | Качество фитопленки |
| 1 Na-КМЦ | Пластичность, однородность, эластичность, прочные, без разрывов. |
| 2 Желатин | Прочность, эластичность, однородность |
| 3 ПВП | Пластичность, однородность, эластичность, слегка липкие |
| 4 ПВС | Жесткие, неоднородные |
Таким образом, по внешнему виду фитопленок можно сделать предварительный вывод о хорошем качестве пленок на основе Na-КМЦ (модели 1) и желатина (модели 2) и несоответствие качества пленок на основе ПВП и ПВС (модели 3 и 4).
Влияние пленкообразователя на антимикробную активность фитопленки
Для дальнейшего подтверждения оптимального состава фитопленки нами были проведены микробиологические исследования.
Определение антимикробной активности проводили по методике представленной в подразделе 2.2.3. Полученные результаты статистически обработаны и представлены в таблице 3.
Таблица 3
Антимикробная активность фитопленок различного состава
№ модели исходного пленкообразователя |
Диаметр региона, который останавливал рост микроорганизма,мм | |||||
S. aureus 505 |
Bacillus Subtilis |
E. coli M-17 |
Ps. aeruginosa |
Candida аlbicans |
||
| 1 Na-КМЦ | 17±0,1 | 16±0,1 | 15±0,2 | 12±0,2 | 16±0,1 | |
| 2 Желатин | - | 12±0,1 | 10±0,2 | - | - | |
| 3 ПВП | - | - | - | - | - | |
| 4 ПВС | - | - | - | - | - | |
| Линкомицина гидрохлорид | 10±0,2 | 24 + 0,1 | 23 ± 0,2 | - | - | |
| Нистатин | - | - | - | 22± 0,1 | - | |
Примечание: « - » - зона задержки роста отсутствует, Диаметры зон задержки роста меньше 10 мм и сплошной рост в чашке оценивали как отсутствие антибактериальной активности, 10-15 мм - слабая активность, 15-20 мм - умеренно выраженная активность, свыше 20 мм - выраженная.
На основе табличных данных построена диаграмма представленная на рисунке 2.
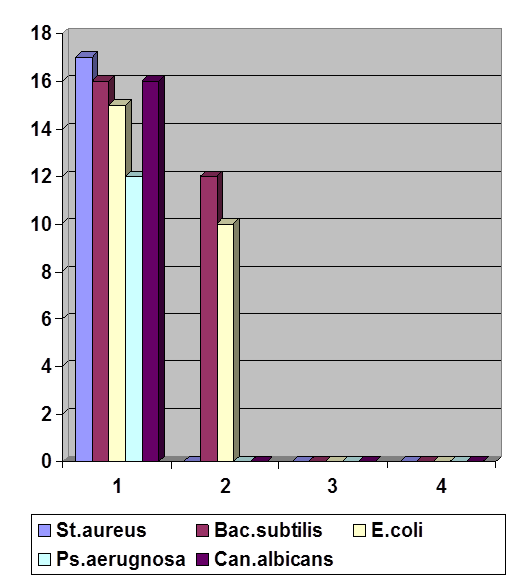
Рисунок 1 – Диаграмма – антимикробная активность фитопленок
В результате исследования установлено, что образцы экспериментальных ФП на основе Nа-КМЦ проявляют умеренно-выраженную антибактериальную активность в отношении грамположительных штаммов Staphylococcusaureus 505, Bacillussubtilis,а также умеренно-выраженное антигрибковое действие в отношении Сandidaalbicans. ФП на основе желатина показали слабую антимикробною активность в отношении Escherichiacoli М-17 и Bacillussubtilis. Образцы ФП на основе ПВП и ПВС показали отсутствие антибактериальной активности.
Из диаграммы видно, что у пленок модели 3 на основе ПВП и модели 4 на основе ПВС антимикробная активность отсутствует, поэтому данные пленкообразователи не могут быть использованы в качестве основы для лекарственной ФП. Наименьшей антимикробной активностью обладают пленки модели 2 на основе желатина с наименьшим показателем диаметра задержки роста 10,0мм по отношению к Escherichiacoli М-17. ФП модели 1 обладает наибольшей антимикробной активностью по всем тест-штаммам, но наиболее активна по отношению к Staphylococcusaureus 505, где диаметр остановки роста составляет 17,0мм, а наименьший 12,0мм.
Таким образом, можно сделать вывод: в связи с тем, что ФП моделей 3 и 4 не проявляют антибактериальную активность, ПВП и ПВС не могут быть использованы как основа для лекарственной ФП. Поэтому данные образцы ФП, согласно полученным результатам, дальнейшим исследованиям не подлежат. Так как ФП модели 2 обладает наименьшей антимикробной активностью, а по отношению к некоторым тест-штаммам антибактериальная активность вообще отсутствует, можно сделать вывод, что наиболее оптимальным составом по данному показателю обладает пленка на основе Na-КМЦ.
Влияние пленкообразователя и остаточной влажности на адгезию пленки
Определение адгезии у фитопленок различного состава проводили по методике, предложенной в подразделе 2.2.2. Среднее значение массы гирек применяли для расчета силы отрыва (F) в Ньютонах (Н) по формуле.
F=mЧg,
где m – масса гирь, вызвавших отклеивание, г; g – ускорение свободного падения, м/с2 . Результаты данных исследований статистически обработаны и представлены в таблице 4
Таблица 4
Зависимость адгезивных свойств фитопленок от основы и остаточной влажности
№ модели |
Сила отрыва, НЧ 10-3 | ||||||||
| Влажность, % | |||||||||
| 47,6 | 41,5 | 37,8 | 32,4 | 29,1 | 24,5 | 18,8 | 12,7 | 5,9 | |
| 1 | 147 | 196 | 245 | 249,9 | 196 | 176,4 | 156,8 | 98 | 87,2 |
| 54,8 | 50,2 | 48,4 | 43,04 | 40,3 | 34,7 | 29,7 | 21,8 | 14,3 | |
| 2 | 98 | 158,76 | 164,15 | 167,58 | 203,84 | 147,88 | 122,5 | 83,3 | 33,3 |
Из данных, приведенных в таблице видно, что ФП модели 2 уступает ФП модели 1 по данному показателю. Т.е. ФП на основе Na-КМЦ обладает наилучшей адгезивной способностю, а следовательно наиболее оптимальным составом по данному показателю. Кроме того, в результате проведенного эксперимента, была установлена оптимальная степень влажности ФП, обеспечивающая наибольшую адгезивную способность данного образца.
Влияние пленкообразователя на влагопоглощение лекарственной пленки
Определение влагопоглощения фитопленок проводили по методике описанной в подразделе 2.2.1. Эксперименту подвергали пленки на основе Na- КМЦ и желатина.
Результаты исследования влагопоглощения статистически обработаны и представлены в таблице 3.
Таблица 3
Результаты набухания фитопленок различных моделей
| № | Общая масса поглощения воды, г | |||||||||
| Время, мин. | ||||||||||
| 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 | |
| 1 | 1,8 | 2,14 | 2,64 | 3,05 | 2,75 | 2,44 | 2,09 | 1,23 | Пленка растворилась | |
| 2 | 1,09 | 1,45 | 1,5 | 2,4 | 2,73 | 3,1 | 3,29 | 3,59 | 3,92 | 4,1 |
Из таблицы видно, что за весь период наблюдения ФП модели 2 не растворилась и обладает меньшей влагопоглощающей способностью по сравнению с ФП модели 1. У ФП на основе Na- КМЦ количество поглощенной воды выше, чем у ФП модели 2 и растворение ее наступило через 80 мин. после начала эксперимента.
Таким образом, из проведенного эксперимента можно сделать вывод: в связи с тем, что ФП модели 2 не растворилась в течение всего времени, желатин не может использоваться как основа для биорастворимой ФП. Следовательно, оптимальным вариантом для создания биорастворимой ФП пролонгированного действия может быть пленка модели 1.
На основании табличных данных была построена диаграмма, представленная на рис. 2, характеризующая антимикробную активность, адгезивные и влагопоглощающие свойства экспериментальных образцов ФП.
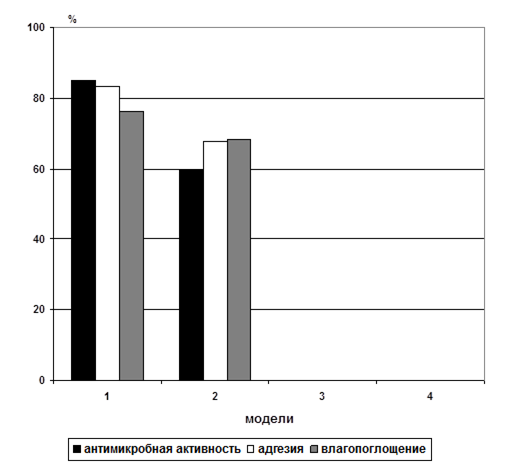
Рисунок 2 – Диаграмма свойств моделей фитопленок
Таким образом, исследования по выбору модели показали, что состав ФП модели 1 обладает наилучшими антибактериальными, адгезивными и влагопоглощающими свойствами. Модель 2 обладает низкими антибактериальными, адгезивными и влагопоглощающими свойствами, поэтому в качестве рационального и оптимального состава мы выбрали модель 4.
Таким образом, разработан состав лекарственной ФП для лечения термических ожогов с условным названием «Фитоплен».
Состав лекарственного препарата
«Фитодермопласт»
Состав на 1 пленку (г):
Настойка эхинацеи 0,468
Сок подорожника 0,468
Полифитовое масло 0,468
Na- КМЦ 1,0
Глицерин 1,14
Вода очищенная 17,14
3.2 Разработка технологии лекарственной фитопленки
На основе лабораторной технологии приготовления фитопленок, которая удовлетворяет всем требованиям, можно порекомендовать вынести лабораторное производство на промышленные масштабы и изготавливать фитопленку по схеме указанной на рисунке 3.
Технология процесса производства пленочной лекарственной формы
Технология производства пленочной лекарственной формы включает в себя следующие этапы:
ВР 1 Подготовка сырья
Отвешивание пленкообразователя, пластификатора и спиртовых извлечений проводят на весах.
ТП 1 Приготовление поливочного раствора
ТП 1.1 Приготовление раствора полимера. Осуществляется следующим образом: исходные компоненты (пленкообразователь, вода) отвешивают на весах, полимер обрабатывают водой, нагретой до 80-900 С, взятой в количестве 0,2-0,5 ч. от требуемого для получения раствора количества. При этом полимер смачивается и набухает, увеличиваясь в объеме в 40 раз.
ТП 1.2 Введение в раствор полимера пластификатора и фитокомплекса. В качестве пластификатора вводят глицерин, настойки зверобоя, прополиса и календулы смешивают друг с другом и вводят в раствор полимера.
ТП 1.3 Гомогенизация поливочного раствора проводят на смесителе с якорной мешалкой после снижения температуры массы до комнатной. Смесь тщательно перемешивают до получения однородного раствора.
ТП 1.4 Фильтрование поливочного раствора. Полученный поливочный раствор фильтруют через слой бязи.
ТП 1.5 Деаэрация поливочного раствора. Центрифугирование раствора в течение 2 часов для удаления пузырьков воздуха.
ТП 2 Приготовление пленок
ТП 2.1 Полив полимерной матрицы на подложки. Полученный раствор с помощью специальной установки наносят в два слоя (через щель) на поверхность металлической ленты, обработанную этиловым спиртом и движущейся со скоростью 0,13-0,14м/мин.
ТП 2.2 Сушка пленок. Полученную пленку сушат в камере с пятью зонами сушки от 40 до 480 С, охлаждают до 380 С и снимают пленку с металлической ленты в виде рулона диаметром 30см.
ТП 2.3 Снятие пленок с подложки и дозирование. Полученную пленку разрезают на полоски и с помощью штампа получают лекарственную пленку требуемого размера.
ТП 2.4 - Стерилизация. Стерилизацию осуществляют облучением при дозе 20 кГр или обработкой смесью этиленоксида с углеродом диоксида. Стерильность сохраняется в течение года.
УМО 1. Контроль качества и оформление готовой продукции
УМО 1.1 Контроль качества пленок. Оценка качества пленок проводится по физико-химическим свойствам: шероховатость поверхности, наличие трещин, разрывов, эластичность, прочность, адгезия, влагопоглощение и антимикробная активность.
УМО 1.2 Фасовка доз в пеналы дозаторы Готовые ЛП упаковывают по 30 штук в специальные пеналы-дозаторы, обеспечивающие герметичность и условия асептики при хранении и использовании. Применяют также контурно-ячейковую упаковку в алюминиевую фольгу или полихлорвиниловую пленку по 10 ЛП, которую укладывают в картонные коробки по 20-100 штук.
УМО 4.3 Упаковка и маркировка. Пеналы-дозаторы упаковывают в картонные коробочки с текстом маркировки.
![]()
Рисунок 3 – Схема технологического производства фитопленки для лечения термических ожогов
Заключение
В настоящее время ТТС нашли широкое признание из-за простоты употребления и высокой эффективности. Они используется для оказания как местного, так и резорбтивного воздействия в различных отраслях медицины.
Новым этапом в лечении термических ожогов является использование лекарственных фитопленок на основе биорастворимых полимеров медицинского назначения с включенными в них субстанциями природного происхождения, которые позволяют ускорить процесс заживления и препятствовать воспалительным процессам в местах ожога.
Для лечения термических ожогов наибольший терапевтический эффект наблюдается при местном применении лекарственного препарата, но применяемые в настоящее время различные растворы, мази, пасты, гели и т.д., недостаточно эффективны , поэтому разработка состава и технологии фитопленок для лечения термических ожогов является актуальной проблемой.
В пользу использования для лечения термических ожогов аппликационных лекарственных форм свидетельствуют многочисленные публикации о результатах апплицирования новых и стандартно используемых лекарственных пленок в лечении термических ожогов.
Анализ литературы свидетельствует в пользу использования тактики местного лечения термических ожогов лекарственными средствами с пролонгированным воздействием лекарственных веществ на патологический очаг, поэтому мы решили разработать рациональный состав и технологию лекарственных пленок с фитокомплексом.
В результате исследований выбран оптимальный состав фитопленки для лечения термических ожогов и проведена следующая работа: изучено влияние пленкообразователя - на качество фитопленки, антимикробную активность, адгезию и влагопоглощение. Кроме того, была установлена оптимальная степень влажности ФП, обеспечивающая ее наибольшую адгезивную способность На основании полученных данных можно сделать следующие выводы.
Выводы:
1.Разработан состав фитопленки на основе натрий-карбоксиметилцеллюлозы, которая представляет собой прочную, эластичную, однородную, без разрывов пленку светло-желтого цвета, со специфическим запахом, кислую на вкус, площадью 49 см2 и толщиной 0,038см.
.2. В результате микробиологических исследований методом диска установлено, что данная фитопленка обладает хорошей антимикробной активностью и может быть использована для лечения термических ожогов.
3. Изучены адгезионные свойства, наибольшей силой сцепления обладает пленка на основе натрий-карбоксиметилцеллюлозы со сепенью влажности 32,4%.
4. Полученная фитопленка обладает хорошей влагопоглощающей способностью и растворяется в течение 80 минут.
5. Разработана технология приготовления пленок, с условным названием «Фитоплен».
Список использованных источников
1. П.Г. Мизина, В.А. Куркин, Л.В. Куравель, В.А. Быков. Взаимосвязь структуры поверхности фитопленок и их адгезивных свойств // Фармация.-2001.-№6.- С. 26 – 27.
2. Б.А. Жубанов, Е.О. Батырбеков, Р.М. Искаков. Полимерные материалы с лечебным действием.-Алматы: «Комплекс», 2000.-220С.
3. С.Ф. Горячев. Безопасность жизнедеятельности и медицина катастроф.- Ростов н/Д.: «Феникс», 2006.-576С.
4. Ю.А. Синявский, М.К. Кошимбеков, И.Г. Цой, А.Я. Бекмуратов. Применение бальзама «Возрождение» при лечении ожоговых ран // Фармация Казахстана.- 2005.-№2.-С. 17-19.
5. М.И. Штильман. Полимеры медико-биологического назначения.- Москва: ИКЦ «Академ-книга», 2006.- 400С.
6. Н.А. Абсадыков, А.З. Карибжанова, С.К.Амзеева. «Фортум» в комплексном лечении ожоговой болезни // Фармация Казахстана.-2007.-№4.-С. 24-256.
7. С.А. Джумабеков, К.С. Сарбанова, Р.Х. Фозилов. Актовегин гель в терапии обширных ожоговых ран // Фармация Казахстана.-2005.-№9.- С. 33-35.
8. П.Г. Мизина. Фитопленки в фармации и медицине // Фармация -2000.-№5.-6.-С.38-40.
9. Т.Н. Юданова, И.В. Решетов. Современные раневые покрытия : получение и свойства (обзор) // Хим.-фармац. Журн.-2006.-№2.-С.24-30.
10. Т.Н. Юданова, И.В.Решетов. Современные раневые покрытия с иммобилизованными протеолитическими ферментами (обзор) // Хим.-фармац. Журн.-2006.-№8.-С.24-28.
11. Алексеева И.В. Разработка лекарственных форм для лечения ран. «Фармация», 2003.- С.43-45.
12. П.Г. Мизина, В.А. Куркин, В.А. Быков, О.И. Авдеева. Влияние вспомогательных веществ на влагопоглощение и адгезию фитопленок // Фармация.-2000.-№2.-С.12-14.
13. К.У. Ушбаев, С.А. Абдрахманов, Л.Е. Токешова. Лекарственные и пищевые растения Казахстана в терапии некоторых заболеваний.- Алматы .-2005.- 158С.
14. П.А Къосев. Полный справочник лекарственных растений.- Москва: «Эксмо», 2002.- 992 С.
15. А.И. Тенцова, М.Т. Алюшина. Полимеры в фармации.- Москва: «Медицина», 1985.-256 С.
9-09-2015, 00:01
