Содержание
Введение
1. Самородные элементы
2. Сульфиды
3. Окислы
4. Карбонаты и сульфаты
5. Силикаты и их аналоги
5.1 Островные силикаты
5.2 Кольцевые силикаты
5.3 Цепочечные и ленточные силикаты
6. Слоистые (листовые) силикаты
7. Каркасные алюмосиликаты
8. Изоморфизм
9. Полиморфизм
Заключение
Литература
минерал кристаллохимический изоморфизм полиморфизм
Введение
Классифицировать минералы можно по ряду признаков. Можно выделять минералы по ведущему или характерному элементу, рассматривая, например, минералы, содержащие медь, свинец и т.д. Существуют генетические классификации, в которых выделяют минералы по их происхождению, например, минералы магматические, пегматитовые, скарновые и т.д. Все эти классификации не удовлетворительны по ряду причин, но могут быть использованы как дополнительный справочный материал.
Наиболее распространённой является химическая классификация минералов. В основу выделения групп в этой классификации положен химический принцип. Классифицировать минералы нужно по химическому принципу (по типам химических соединений, по характеру химической связи) с обязательным учётом структурных особенностей минералов. Ниже изложены краткие химические, кристаллохимические и морфологические особенности основных групп минералов.
1. Самородные элементы
В самородном состоянии в природе известны около 40 химических элементов, но большинство из них встречается очень редко табл. 1.
Таблица 1. Минералы - простые вещества и твердые растворы металлов
| Класс | Группа | Минерал | Сингония | Твердость |
| Металлы и полуметаллы | Меди | Медь Cu Золото (Au, Ag, Cu) Серебро (Ag, Au) |
Куб. ---- ---- |
3 2, 5 3 |
| Железа | Феррит α-Fe Тэнит γ-Fe |
Куб. ---- |
- 5 |
|
| Платины | Платина Pt Осмий Os Иридий Ir Осмирид (Ir, Os) Родий Rh Палладий Pd |
Куб. Гекс. Куб. ---- ---- ---- |
4 - - - - 4, 5 |
|
АлюминияЦинка Свинца Висмута Мышьяка |
Алюминий Al Цинк Zn Свинец Pb Висмут Bi Мышьяк As |
Куб. Гекс. Куб. Триг. ---- |
- - 1, 5 2 3, 5 |
|
| Неметаллы | Серы | Сера S | Ромб. | 1, 5 |
| Углерода | Графит С Алмаз С Лонсдейлит С Чаоит С |
Гекс. Куб. Гекс. ---- |
1, 5 10 - - |
Нахождение элементов в самородном виде связано со строением их атомов, имеющих устойчивые электронные оболочки. Химически инертные в природных условиях элементы называются благородными; самородное состояние для них является наиболее характерным. К ним относятся золото Au, серебро Ag, платина Pt и элементы группы платины. Очень часто в самородном состоянии встречаются углерод С, сера S и медь Cu.
Реже встречаются так называемые полуметаллы: мышьяк As, сурьма Sb, висмут Bi, иридий Ir. Такие минералы как железо Fe, свинец Pb, олово Sn, ртуть Hg, встречаются как самородные крайне редко и нахождение их представляет лишь научный интерес. Некоторые элементы (хром, алюминий) вообще не встречаются в самородном виде.
2. Сульфиды
Сернистых и аналогичных им минералов насчитывают более 200 видов, но общее содержание их в земной коре невелико и не превышает 0.15%.
С химической точки зрения они являются в основном производными сероводорода H2 S. В некоторых редких минералах место серы занимают Se и Te. По аналогии с сульфидами также выделяют арсениды и антимониды. Во всех этих соединениях широко развиты изоморфные замещения одних элементов другими.
Наибольшее распространение имеют дисульфиды и сульфиды железа, на долю которых приходится около 4/5 всех сульфидов табл. 2. Обычными сульфидами являются сульфиды меди, свинца, цинка, серебра, сурьмы и т.д. В виде изоморфных примесей в состав сульфидов входит целый ряд редких и рассеянных элементов, не образующих самостоятельных минералов.
Таблица 2. Главнейшие минералы – сернистые соединенияи их аналоги
| Класс | Структура | Минерал | Формуламинерала |
Син-гония | Твер-дость |
| Простые сульфиды | Координационная | Аргентит Халькозин Галенит Алабандин Сфалерит Троилит Пирротин Никелин |
Ag2 S Cu2 S PbS MnS (Zn, Fe)S FeS FeS NiAs |
Ромб. ---- Куб. ---- ---- Гекс. Мон. Гекс. |
2-2, 5 2-3 2-3 3, 5-4 3-4 3-4 4 5 |
| Цепочечная | Киноварь Стибнит Висмутин |
HgS Sb2 S3 Bi2 S3 |
Триг. Ромб. ---- |
2-2, 5 2-2, 5 2-2, 5 |
|
| Кольцевая | Реальгар Аурипигмент Молибденит |
AsS As2 S3 MoS2 |
Мон. Ромб. Гекс. |
1, 5-2 1-2 1 |
|
| Сложные сульфиды | Координационная Слоистая |
Пентландит Халькопирит Станнин Кёстерит Борнит Ковеллин |
Fe5 Ni4 S8 CuFeS2 Cu2 FeSnS4 Cu4 Zn2 Sn2 S8 Cu5 FeS4 CuS = Cu2 CuS(S2 ) |
3-4 3-4 3-4 4 3 1, 5-2 |
Сульфиды за небольшим исключениями имеют металлический блеск, большую плотность и невысокую твёрдость. Встречаются они в виде кристаллов, друз, чаще - в виде сплошных зернистых масс и вкрапленников.
Происхождение сульфидов главным образом гидротермальное, а также магматическое, скарновое и для некоторых экзогенных - осадочное.
При окислении сульфиды разлагаются и легко переходят в различные вторичные минералы: карбонаты, сульфаты, окислы и силикаты, устойчивые в поверхностных условиях.
Сульфиды имеют большое практическое значение - это важнейшие руды свинца, цинка, меди, серебра, никеля и других металлов.
По структурному принципу среди сульфидов можно выделить сульфиды координационной, цепочечной, слоистой и других структур. Так, например, сульфиды можно классифицировать, выделяя структурные мотивы: координационный, островной, цепочечный, слоистый.
3. Окислы
Окислы - соединения элементов с кислородом, в гидроокислах присутствует также вода. В земной коре на долю окислов и гидроокислов приходится около 17%, из них на долю кремнезёма (SiO2 ) около 12.5%.
Наиболее распространёнными минералами этой группы являются окислы кремния, алюминия, железа, марганца и титана табл. 3.
Таблица 3. Главные минералы – оксиды
| Класс | Минерал | Формула минерала | Сингония | Твердость |
| Простые | Куприт Тенорит Корунд Гематит Уранинит Торианит Кварц Тридимит Кристобалит Стишовит РутилАнатаз Кассситерит Пиролюзит |
Cu2 O CuO Al2 O3 Fe2 O3 UO2 ThO2 SiO2 SiO2SiO2 SiO2TiO2 TiO2 SnO2 MnO2 |
Куб. Мон. Триг. ---- Куб. ---- Триг., гекс. Ромб., гекс. Тетр., куб. Тетр. ---- ---- ---- ---- |
3, 5 –4 3, 5 9 5, 5-6 5-6 6, 5 7 6-7 6, 5-7 - 6 5-6 6-7 5-6 |
| Сложные | ИльменитШпинель Магнетит Хромит |
FeTiO3 MgAl2 O4 FeFe2 O4 FeCr2 O4 |
Триг. Куб. ---- ---- |
5-6 8 5, 5-6 5, 5-7, 5 |
В кристаллических структурах минералов класса окислов катионы металлов находятся в окружении анионов кислорода (в окислах) или гидроксила (в гидроокислах). Среди окислов можно выделить простые окислы, в которых отношения между катионами и анионами изменяются в пределах от 2:1 до 1:2 (R2 O, R2 O3 , RO2 ) и сложные окислы, для которых характерны двойные соединения типа RO*R2 O3 .
Происхождение минералов класса окислов различное - магматическое, пегматитовое, гидротермальное, но большинство окислов образовалось в результате экзогенных процессов в верхних слоях литосферы. Многие эндогенные минералы при выветривании разрушаются и переходят в окислы и гидроокислы.
Физические свойства окислов различны: для большинства из них характерна высокая твёрдость. Минералы класса окислов имеют большое практическое значение.
4. Карбонаты и сульфаты
Карбонаты - многочисленная группа минералов, которые имеют широкое распространение. В структурном отношении все карбонаты относятся к одному основному типу - анионы [CO3 ]2- представляют собой изолированные радикалы в форме плоских треугольников.
Большинство карбонатов безводные простые соединения, главным образом Ca, Mg и Fe с комплексным анионом [CO3 ]2- . Менее распространены сложные карбонаты, содержащие добавочные анионы (OH)- , F- и Cl- . Среди наиболее распространённых безводных карбонатов различают карбонаты тригональной и ромбической сингоний.Карбонаты обычно имеют светлую окраску: белую, розовую, серую и т.д., исключение представляют карбонаты меди, имеющие зелёную или синюю окраску. Твёрдость карбонатов около 3-4.5; плотность невелика, за исключением карбонатов Zn, Pb и Ba.
Важным диагностическим признаком является действие на карбонаты кислот (HCl и HNO3 ), от которых они в той или иной степени вскипают с выделением углекислого газа.По происхождению карбонаты осадочные (биохимические или химические осадки) или осадочно-метаморфические минералы; выделяются также поверхностные, характерные для зоны окисления и иногда низкотемпературные гидротермальные карбонаты.
Сульфаты - соли серной кислоты. Они имеют светлую окраску, небольшую твёрдость, многие из них растворимы в воде.
Основная масса сульфатов имеет осадочное происхождение - это химические морские и озёрные осадки. Многие сульфаты являются минералами зоны окисления, известны сульфаты и как продукты вулканической деятельности.Различают сульфаты безводные, водные и сложные, содержащие кроме общего для всех анионного комплекса [SO4 ]2- также добавочные анионы (ОН)- .
5. Силикаты и их аналоги
Класс силикатов и их аналогов является самым большим по числу минеральных видов – к нему относится 30% от их общего числа. В целом силикаты и алюмосиликаты слагают около 75 об.% земной коры, при этом наиболее распространены полевые шпаты – на их долю приходится около 40-45 об.% литосферы. За ними по распространенности следуют слюды, пироксены, амфибиолы и гранаты. В соответствии с распространенностью химических элементов главными катионами в силикатах и их аналогах являются K, Na, Ca, Mg, Fe. Значительна также роль алюминия, который, как показали рентгеноструктурные исследования, может выступать как в качестве катиона, так и входить в анионный радикал минералов.
Выявлены следующие черты строения силикатов и их аналогов.
1. Во всех силикатах атомы кремния имеют по отношению к кислороду четверную координацию, они образуют вместе с кислородом, как в кварце, кремнекислородные тетраэдры (SiO4 )4- (cм. рис. 1). Связи кремния с кислородом смешанные ионно-ковалентные, с разной степенью ионности в минералах разной структуры и с разными катионами.
2. Кремнекислородные тетраэдры могут быть одиночными, и тогда они соединяются в общей структуре минерала через катионы, но могут и полимеризоваться, образуя различные анионные группировки.
3. Алюминий в силикатах может быть катионом, занимая позиции в октаэдрических пустотах между кислородом, и может входить в тетраэдры (AlO4 )5- , занимая в структуре минералов позиции, адекватные с кремнием. Например, в каолините Al2(Si2O5)(OH)4 алюминий является катионом и имеет координационное число шесть, а в микроклине K(AlSi3O8) он входит в анионный радикал минерала. Есть минералы, в которых алюминий представлен и как катион и входит в анионный радикал, например в слюде мусковите KAl2(AlSi3O10)(OH)2.Размер тетраэдров (AlO4 )5- и его конфигурация иные, чем у групп (SiO4 )4- , характер химических связей также отличен. Поэтому имеется предел замещения Si4+ Al3+
Установлено, что в силикатах может замещаться алюминием не более половины кремния в тетраэдрах. Значит, предельны по составу алюмосиликаты типа анортита Ca(Al2Si2O8), нефелина Na(AlSiO4) и т. п.
4. Помимо кремнекислородных анионных радикалов во многих силикатах и алюмосиликатах есть дополнительные анионы - OH- , (CO3 )2- ,(SO4 )2- ,(S2 )2- , (BO3 )3- , (P2 O7 )4- и др.
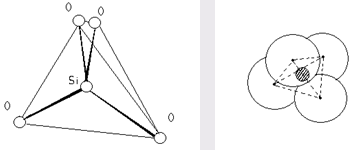
Рис. 1. Тетраэдр (SiO4 ) в двух изображениях.
Классификация силикатов и их аналогов производится по их структурам. Так выделяют шесть подклассов: островные, кольцевые, цепочечные, ленточные, слоистые, каркасные.
5.1 Островные силикаты
Среди силикатов это наиболее многочисленный подкласс минералов. Его характерными представителями являются оливин (Mg, Fe)2(SiO4 ), альмандин Fe3 Al2 (SiO4 )3 , гроссуляр Ca3 Al2 (SiO4 )3 , топаз Al2 (SiO4 )F2 , эпидот Ca2 (Al,Fe)(SiO4 )(Si2 O7 )O(OH). Силикаты это подкласса имеют разнообразный состав – это минералы магния, железа, кальция, марганца, титана, алюминия, редких земель, тория, циркония, ниобия и др., ни в одном другом подклассе нет такого разнообразия катионов. К этому подклассу относятся также совсем особые по составу и структуре минералы, очень редкие в природе – это силикофосфаты, в них имеются дополнительные радикалы (P2 O7 )4- и (PO4 )3- (например, ломоносовит с приблизительной формулой Na5 Ti2 (Si2 O7 )(PO4 )O2 и силикокарбонаты (сперрит Ca5 (SiO4 ) 2 (CO3 ) и др.)).
Кристаллохимическое своеобразие минералов подкласса островных силикатов определяется сочетанием двух факторов: а) присутствием в них орто- и диортогрупп - (SiO4 )4- и (Si2 O7 )6- , б) большой ролью в их составе катионов октаэдрической координации с радиусом от 0,060 до 0,080 нм (Ti4+ -0,064; Fe3+ -0,067; Nb5+ -0,069; Mg2+ -0,078; Fe2+ -0,082 нм, по В. Гольдшмидту), главными из них являются магний и железо. Благодаря такому сочетанию типичных для плотнейшей упаковки её тетраэдрических и октоэдрических полиэдров, структуры островных силикатов наиболее компактны и прочны среди силикатов других подклассов. Кроме перечисленных катионов большую роль, но не во всех, а в некоторых островных силикатах играют относительно крупные катионы восьмерной (и более) координации – Ca2+ (0,016 нм), Na+ (0,098 нм), Ce3+ (0,018 нм). Их координационные полиэдры несоразмерны с октаэдрами и тетраэдрами. Структура таких минералов, за малым исключением (гроссуляр), менее компактна.
Характерная особенность алюминия в островных силикатах заключается в том, что он всегда занимает октаэдрические позиции и является в этих силикатах катионом. Разнообразие катионов, их разные радиусы и свойства приводят к усложнению кристаллических структур островных силикатов и часто к вхождению в них дополнительных анионов F- и (OH)- . Особенно характерны такие анионы для силикатов, содержащих одновременно группы (SiO4 )4- и (Si2 O7 )6- и резко различающиеся по металлическим свойствам катионы: Ca2+ и Ti4+ (титанит), Ca2+ и Al3+ (эпидот), K+ , Na+ и Ti4+ (лампрофиллит). Дополнительные анионы характерны также для силикатов, в состав которых входят только группы (SiO4 ) и алюминий в качестве катиона, - топаз Al2 (SiO4 )F2 , кианита Al2 (SiO4 )Oи др.
Перечень главнейших островных силикатов приведен в табл. 4.
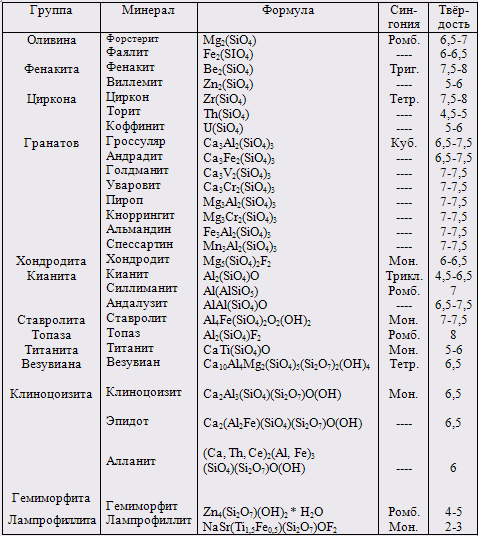
Таблица 4. Главные минералы – островные силикаты
Островные силикаты образуются даже в стесненных условиях роста в виде хороших кристаллов. Это объясняется их большой силой кристаллизации, что обусловлено относительной компактностью и простотой структур этих силикатов, многозарядностью анионных комплексов и значительной силой связей катионов, входящих в их состав. Островные силикаты обладают высокой степенью идиоморфизма (совершенства) кристаллов.
Окраска островных силикатов обычно обусловлена присутствием в их составе в качестве главных и примесных компонентов элементов-хромофоров (Fe, Mn, Ti и Cr). Атомы двух- и трёхвалентного железа вызывают при разных своих соотношениях зелёные (гроссуляр, эпидот), коричневые (андрадит, ставролит, титанит) цвета. Лишь в редких случаях встречаются бесцветные, белые островные силикаты – это химически чистые гроссуляр, форстерит, топаз каламин.
Компактность структуры и наличие в минералах небольших, но высокозарядных катионов проявляются в высокой плотности и твёрдости (от 6 до 8) этих минералов. Из-за большой твердости эти минералы черты не дают (они процарапывают бисквитную пластинку), даже у густо окрашенных минералов она чуть заметна.
5.2 Кольцевые силикат
Подкласс островных силикатов объединяет сравнительно небольшое число редких в природе минералов. Среди них только два минерала – турмалин и берилл – играют в некоторых случаях роль второстепенных, а иногда и даже главных минералов ряда минеральных месторождений.
Главными структурными элементами кольцевых силикатов являются одно- или двухъярусные тройные, четверные, шестерные, девятерные кольца тетраэдров. Турмалин и берилл характеризуются шестерными одноярусными кольцами, но разной конфигурации. В турмалине все тетраэдры в кольце лежат своими основаниями в одной плоскости, вершины обращены в одну сторону, сечение кольца не просто шестиугольное, а дитригональное. В структуре минерала кольца ориентированы одинаково – вершинами тетраэдров вверх, структура получается резко асимметричной по строению и свойствам, а кристалл турмалина имеет дитригональное сечение и не одинаковые концы. Они растут с неодинаковой скоростью, по-разному адсорбируют вещества, в том числе пигментирующие изоморфные примеси, и потому разные концы кристалла нередко различны по цвету; из-за асимметрии структуры в турмалине хорошо проявлен пироэлектрический эффект. В бериллах кольцо гексагональное с горизонтальной плоскостью симметрии, оба конца кристаллов берилла одинаковые по огранке и своим свойствам.
В целом структуры кольцевых силикатов сложные и не плотные. Сингония минералов определяется геометрией их колец. Преобладают тригональные и гексагональные минералы.
Таблица 5. Главные минералы – кольцевые силикаты.
| Группа | Минерал | Формула | Син-гония | Твер-дость |
| Турмалина | Шерл Рубеллит |
NaFe3 Al6 (Si8 O18 )(BO3 )3 (OH)4 Na(Li1,5 Al1,5 )Al6 (Si6 O18 )(BO3 )3 (OH)4 |
Триг. ---- |
7-7,5 7-7,5 |
Берилла Эвдиалита Кордиерита |
Берилл Эвдиалит Кордиерит |
Be3 Al2 (Si6 O18 ) Na12 Ca6 (Fe, Mn)3 Zr3 (Si3 O9 )2 (Si9 O24 (OH3 ))2 (Mg, Fe)2 Al3 (AlSi5 O18 )*nH2 O |
Гекс. Триг. Ромб. |
7,5-8 5-5,5 7-7,5 |
5.3 Цепочечные и ленточные силикаты
К подклассам цепочечных и ленточных силикатов относятся в первую очередь главные породообразующие минералы – пироксены (диопсид, геденбергит, эгирин и др.) и амфибиолы (актинолит, роговая обманка и др.), а также ряд менее распространенных минералов. Имеется много черт подобия пироксенов и амфибиолов по структуре и составу, по морфологии их кристаллов и физическим свойствам, но есть и существенные различия, опять же вытекающие из особенностей структуры и состава.
Пироксены и амфибиолы имеют сходный, довольно простой химический состав. Чаще всего силикаты магния либо двойные соли магния и кальция, во многих минералах кроме них обязательно присутствует натрий. Итак, в основном три элемента – магний, кальций и натрий – в разных сочетаниях. В качестве постоянной изоморфной примеси в позициях магния размещается железо, иногда полностью вытесняя магний. В некоторых случаях, обычно в ассоциации с натрием, в пироксены и амфибиолы входит алюминий, занимая или позиции магния, или внедряясь в радикал в позиции кремния. Наконец, есть редкие литиевые пироксены и амфибиолы.
Главным различием состава пироксенов и амфибиолов является обязательное вхождение в последние конституционной воды в форме дополнительных анионов (OH)- .
В структуре пироксенов имеются одинарные цепочки (Si2 O6 )4- ,в амфибиолах - ленты (Si4 O11 )6- с группами (OH)- в центре каждого кольца этой ленты.
Наиболее простые химические формулы следующих минералов:

Зная эти формулы наизусть можно вывести из них все гипотетические и реальные составы пироксенов и амфибиолов. Так используя простую схему изовалентного изоморфизма Mg2+ Fe2+ , получаем формулы:

Главнейшие пироксены и их формулы приведены в табл. 6. Однако в природе нет химически чистых пироксенов и амфибиолов, состав которых точно отвечал бы приведенным в этой таблице формулам. Он всегда более сложен за счет явлений изоморфизма.
Таблица 6. Главные пироксены и амфибиолы
| Состав | Пироксены | Амфибиолы | ||
| ромбические | моноклинные | ромбические | моноклинные | |
Силикаты: магниевые |
ЭнстатитMg(Si2 O6 ) |
Клиноэнстатит Mg(Si2 O6 ) |
Антофиллит Mg(Si8 O22 )(OH)2 |
Куммингтонит Mg(Si8 O22 )(OH)2 |
| литиевые | ---- | Сподумен LiAl(Si2 O6 ) |
Холмквистит LiMg(Si8 O22 ) (OH)2 |
Клинохолмквистит LiMgAL(Si8 O22 )(OH)2 |
| кальциевые | ---- | Диопсид CaMg(Si2 O6 ) Геденбергит CaFe(Si2 O6 ) |
---- ---- |
Тремолит Ca2 Mg5 (Si8 O22 )(OH)2 Ферроактинолит Ca2 Fe5 (Si8 O22 )(OH)2 |
| натриевые | ---- ---- |
Жадеит NaAl(Si2 O6 ) Эгирин NaFe(Si2 O6 ) |
---- ---- |
Глаукофан Na2 Mg3 Al3 (Si8 O22 )(OH2 Рибекит Na2 Fe3 Fe2 (Si8 O22 )(OH)2 |
| Алюмо-силикаты | ---- ---- |
---- Авгиты |
---- ---- |
Жедрит Mg6 (Al, Fe)(AlSi7 O22 ) (OH)2 Обыкновенные роговые обманки |
Слоистые (листовые) силикаты. К подклассу слоистых (листовых) силикатов и алюмосиликатов относятся известные всем вещества – тальк, слюды, глинистые минералы и др. Многие из них являются породообразующими минералами или используются в промышленности.
Различают листовые силикаты (алюмосиликаты) с простыми и сложными сетками тетраэдров. Последние являются менее распространенными минералами.
Остовом структуры слоистых силикатов являются сетки кремнекислородных тетраэдров. Они располагаются параллельно друг другу и чередуются с плоскими сетками другого состава, образуя пакеты слоёв. Все слоистые силикаты и алюмосиликаты имеют свои структурные разновидности за счет разного смещения (сдвига) и разворота пакетов друг относительно друга, что легко осуществляется в природе из-за малых сил связей между пакетами. В итоге получаются минералы разных сингоний – моноклинной (чаще всего), гексагональной, ромбической, тригональной, триклинной. Такие структурные разновидности слоистых силикатов называют политипами. Некоторые из них устойчивые только при определённых давлениях и температурах и образуются только в определённой химической обстановке. Политипия, как видно, является частным случаем полиморфизма.
Главные группы слоистых силикатов и алюмосиликатов представлены в табл. 7.
Таблица 7. Главные минералы – слоистые силикаты и алюмосиликаты.
| Катионы в тетраэдрах | Межпакетный катион | Внутрипакетный (октаэдрический) катион |
|
| Mg2+ | Al3 + | ||
| Si | Нет ---- |
Серпентин Тальк |
Каолинит Пирофиллит |
| Al + Si | (Комплекс)n + K+ K+ Ca2+ (Комплекс)n + (Комплекс)n + |
Монтмориллонит ФлогопитМусковит Литиевые слюдыХрупкие слюды Гидрослюды Хлориты |
|
Требует пояснения монтмориллонит: некоторые минераллы группы монтмориллонита являются силикатами, другие – алюмосиликатами.
Каркасные алюмосиликаты. Многие из силикатов этого подкласса относятся к числу породообразующих и наиболее распространенных в природе минералов. В первую очередь это полевые шпаты – главные составные части гранитов, габбро, гнейсов и других горных пород. К этому же подклассу минералов относятся нефилин (основной минерал некоторых щелочных горных пород), лейцит (обычная минеральная фаза в базальтоидах). Среди них есть и ценное нерудное сырье (микроклин, цеолиты), и минералы-руды некоторых минералов – нефелин (руда на алюминий), поллуцит (руда на цезий).
В состав каркасных алюмосиликатов большей частью входят катионы калия, натрия, кальция. "Рыхлость" каркасной структуры допускает частое вхождение в них дополнительных анионов (Cl-
,CO3
2-
,SO4
2-
и т. д. )
29-04-2015, 00:44
