Таким чином, дані мікроскопічного дослідження міокарду при АХС і ГІМБГ показують, що в ньому переважають явища розладу кровообігу, дистрофічні зміни й виражена запальна реакція в стромі, порівняно з контрольною групою. При ДКМП і АКМП системного ушкодження з боку інтерстіціальної тканини, а також стінок судин міокарду – не виявлено.
Одним з цитокінів, що обумовлюють розвиток аутоімунних процесів в організмі є TGF-β (рис.6). При дії TGF-β на імунну систему переважають інгібуючі ефекти, але він посилює синтез білків міжклітинного матриксу. Таким чином, TGF-β є елементом зворотної регуляції імунної відповіді. За результатами наших досліджень рівень TGF-β при РКС від АХС і від ГІМБГ зменшився у 7 та 5,7 рази відповідно порівняно з групою контролю.
Таким чином, активація прозапальних цитокінів (TNFα, IL-1β, IL-6) супроводжується підвищенням рівня протизапального цитокіну IL-4, окрім РКС від АКМП. Підвищення концентрації цитокінів у сироватці крові є свідченням активного системного запалення у судинній стінці при АXС та ГІМБГ.
Було досліджено особливості стану АОС та ПОЛ при різних формах РКС. На сучасному етапі доведено, що у міокарді при АХС має місце активна інфільтрація тканин циркулюючими у крові моноцитами та нейтрофілами. Активовані нейтрофіли посилюють утворення супероксид-радикалів і активують перекисне окислення білків і ліпідів.
Як показали результати проведених досліджень у міокарді осіб, що загинули від РКС, від АХС, підвищена активність процесів ПОЛ (вміст МДА збільшився у 1,7 рази, а ДК – у 2,9 рази порівняно з контрольною групою). Вміст SH-груп й активність каталази - зменшені, таким чином у міокарді має місце окислювальний стрес. Підвищується активність ЛДГ – ферменту анаеробного гліколізу, що свідчить про енергодефіцитний стан у міокарді (табл.3).
Вміст SH-груп у міокарді при РКС від АХС, ГІМБГ, АКМП, ДКМП знижується порівняно з контрольною групою, це свідчить про порушення активації антиоксидантної системи й про наявність оксидативного стресу в тканині міокарду при РКС (рис. 7).
При біохімічному дослідженні сироватки крові встановлено, що при РКС, обумовленій ДКМП, у 3 рази зростає вміст первинного продукту ПОЛ - ДК, у 1,8 рази збільшується вміст кінцевого продукту ПОЛ - МДА. При РКС, обумовленій ГІМБГ й АХС, спостерігається активація первинних і кінцевих продуктів ПОЛ: ДК у 4,3 і 2,4 рази та МДА у 2,4 і 1,5 рази відповідно. Зміни біохімічних показників, що вивчались, свідчать про порушення метаболізму.
Таблиця 3
Показники ПОЛ при РКС
| Показник | КГ (n=20) |
Причина РКС | ||||||||
| АХС (n=20) | ГІМБГ (n=20) | ДКМП (n=20) | АКМП (n=20) | |||||||
| сироватка крові | міо кард |
сироватка крові | міо кард |
сироватка крові | міо кард |
сироватка крові | міо кард |
сироватка крові | міо кард |
|
ЛДГ, мккат/л ммоль/хв·г білка |
30 ±1,2 |
27,3 ±0,9 | 33,7 ±0,8 ◘ |
35,7 ±0,7* |
39,9 ±0,8* |
42,8 ±0,6* |
35,9 ±0,9* |
39,3 ±0,9* |
33,7 ±0,7 ◘ |
29,7 ±0,8# |
МДА мкмоль/л мкмоль/г білка |
8,3 ±0,9 |
10,2 ±0,9 | 12,9 ±0,9* |
17,3 ±0,7* |
19,8 ±0,8* |
19,9 ±0,8* |
14,8± 0,8* |
19,8 ±0,6* |
10,2 ±0,7 |
14,9 ±0,6* |
ДК, мкмоль/л мкмоль/г білка |
1,6 ±0,4 |
1,8 ±0,8 |
3,9 ±0,6* |
5,3 ±0,4* |
6,9 ±0,9* |
7,8 ±0,5* |
4,8 ±0,7* |
7,1 ±0,7* |
2,7 ±0,6 |
3,4 ±0,6 |
Каталаза мккат/гНв ммоль/хв·г білка |
12,9 ±1,2 |
22,9 ±1,3 |
8,2 ±0,8* |
10,2 ±0,7* |
5,4 ±0,6* |
6,8 ±0,5* |
6,5 ±0,7 * |
7,5 ±0,5* |
10,6 ±0,9 |
15,8 ±0,9* |
| SH-групи, мМоль/л | - | 98 ±0,9 |
- | 51,9 ±0,8* |
- | 49,1 ±0,6* |
- | 66,13 ±1,3* |
- | 61,3 ±0,9* |
*р<0,001, # р<0,05, ◘ р<0,02порівняно з контрольною групою (КГ) людей, що померли від механічної травми.
Таким чином, у міокарді осіб, що загинули від РКС, підвищений рівень ПОЛ при зниженні активності АОС, в тканині серця має місце окислювальний стрес, який призводить до розвитку енергодефіцитного стану, про що свідчить підвищення активності ЛДГ.
Дослідження синдрому ендогенної інтоксикації при РКС від ССЗ мало відомо. Показано, що ендотоксемія розвивається при всіх патологічних станах, пов`язаних з підвищенням катаболізму або блокадою детоксикаційних систем організму. Першим субстратом, що відповідає за виникнення патологічних ефектів ендогеної інтоксикації при патологічних станах, вважали білкові токсини –молекули середньої ваги (МСВ), що утворюються в процесі протеолізу в ушкоджених тканинах, а також у плазмі при виході в кров протеолітичних ферментів.
Накопичення МСВ не тільки є маркером ендоінтоксикації, і подальше вони поглиблюють перебіг патологічного процесу. МСВ володіють нейротоксичною активністю, пригнічують процеси біосинтезу білка, здатні пригнічувати активність ряду ферментів, , змінюють транспорт іонів через мембрани, фагоцитоз, мікроциркуляцію, лімфодинаміку, викликають стан вторинної імунодепресії.
При біохімічному дослідженні плазми крові встановлено, що при РКС, обумовленій АХС, ГІМБГ, значно збільшується (у 15,8 та 13,6 рази відповідно) рівень МСВ, а при РКС, обумовленій ДКМП у 4,8 рази підвищується МСВ порівняно з контрольною групою (рис. 8). При АКМП практично не збільшується вміст МСВ порівняно з контрольною групою.
Таким чином, проведені дослідження свідчать про активацію вільнорадикальних процесів при РКС, що пов’язано з пригніченням АОС у зв’язку з активацією (стимуляцією) механізмів запалення й аутоімунних реакцій у тканині міокарда при ДКМП і судинах при АХС.
Для розробки алгоритму проведення диференціальної діагностики РКС, обумовленої ГІМБГ, ДКМП, АКМП, АХС, нами проведено узагальнення отриманих результатів досліджень. Патофізиологічним підґрунтям концептуальної моделі диференційної діагностики окремих видів РКС є імунопатологічний механізм інгібіції клітинної ланки імунітету, що призводить до системного обмінного дисбалансу, в якому імунний, цитокіновий та метаболічний стан організму та серцевого м´язу з позиції активації вільнорадикальних процесів ПОЛ призводить до накопичення активних форм кисню, перекисей, вільних радикалів, які руйнують структуру біологічних мембран міокардіоцитів, модулюючи вільнорадикальну патологію. Тривала стимуляція ПОЛ призводить до виснаження АОС, інгібування процесів біоенергетики й пригнічення біосинтетичних процесів у цілому. Ці процеси є визначними в формуванні морфологічних змін у серцевому м´язі. Тому використання комплексного лабораторного дослідження, яке базується, передусім, на з´ясуванні імунного, цитокінового та метаболічного стану організму та серцевого м´язу надасть можливість диференціації конкуруючих причин смерті.
Концепція застосування комплексу лабораторних досліджень для диференційної діагностики РКС, обумовленої АХС, ГІМБГ, ДКМП, АКМП передбачає врахування даних патоморфологічного дослідження (макроскопічне дослідження серця та його судин з мікроскопічним та гістоімунологічним дослідженням міокарду), біохімічного (АОС/ПОЛ, рівень ендогенної інтоксикації) та імунологічного (імунний та цитокіновий статус), що представлено на рис. 10.
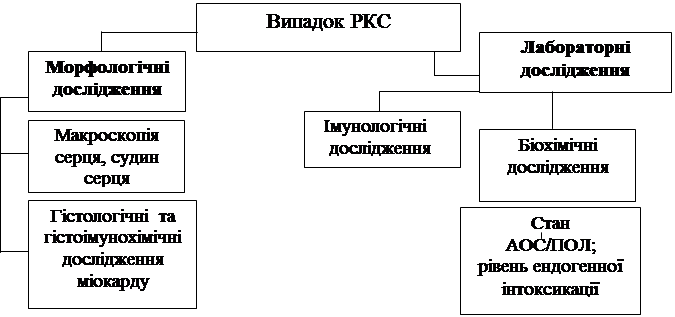
Рис. 10. Алгоритм застосування діагностичних критеріїв при диференціації РКС.
Враховуючи спільні механізми формування патології, нами проведено групування випадків РКС у дві групи: атеросклеротичного (АХС та ГІМБГ) і неатеросклеротичного (ДКМП та АКМП ) ураження.
Морфологічні дослідження. Як відомо, в судово-медичній експертизі з діагностичною метою досить активно використовують морфологічне – макро- та мікроскопічне дослідження. Проведене нами дослідження вказує, що за морфологічними ознаками – макроскопічними: в´ялість міокарду, кровонаповнення, вага серця, гіпертрофія серця та мікроскопічними: набряк інтими судин серця, фіброзно-тканинні бляшки, стан кардіоміоцитів, набряк строми, лейкоцитарна інфільтрація інтерстиції, стан коронарних судин - можливо визначити причину РКС. В той же час для глибокого розуміння як причини морфологічних змін, так і отримання диференційно діагностичних показників, важливо з´ясувати роль та місце обмінних порушень в міокарді та організмі.
Для імуногістохімічного розмежування РКС (табл. 4) з атеросклеротичним механізмом формування змін у міокарді - АХС та ГІМБГ діагностичне значення мають клітини – продуценти лімфоцитів, а також клітини-продуценти цитокінів (р<0,05). Макрофагальну реакцію та реакцію плазмобластної трансформації не можливо вважати діагностичною, оскільки достовірної різниці між групами порівняння не спостерігається.
Для розмежування РКС з неатеросклеротичним механізмом формування змін у міокарді (АКМП і ДКМП) діагностичним критерієм може бути тільки наявність основних клонів клітин-продуцентів цитокінів (р<0,05). Інші імуногістохімічні показники виявились не достовірними.
Таблиця 4
Визначення імуногістохімічних показників для диференціації РКС від ГІМБГ і АХС та РКС від АКМП і ДКМП
| Патогенетичне розмежування причин РКС | з атеросклеротичним ураженням | без атеросклеротичного ураження | ||
| показники | ГІМБГ | АХС | АКМП | ДКМП |
| лімфоцити | 55,0±2,0 | 61,0±2,0 | різниця не достовірна |
|
| р<0,05 | ||||
| клітини- продуценти цитокінів | 39,0±1,0 | 42,0±1,0 | 21,0±1,0 | 18,0±1,0 |
| р<0,05 | р<0,05 | |||
Імунологічні дослідження. Для диференціації РКС з атеросклеротичним ураженням – АХС і ГІМБГ діагностично значущими імунологічними показниками є зміни вмісту Т-цитотоксичних лімфоцитів (CD8), NK-клітин, концентрації сіромукоїдів та цитокінів (TNFα, IL-6, IL-4). Що ж стосується таких показників, як CD3 (загальна популяція Т-лімфоцитів), CD4 (Т-хелпери), CD21 (В-клітини), IL-1β (прозапальний цитокін) та TGF-β (трансформуючий фактор росту), то їх зміни виявились недостовірними, а саме – діагностично не значними для розмежування РКС від АХС і РКС від ГІМБГ.
Для розмежування випадків РКС з неатеросклеротичним механізмом формування патології у міокарді (АКМП та ДКМП) діагностичними критеріями являються зміни вмісту Т-цитотоксичних лімфоцитів (CD8), В-клітин (CD21), цитокінів (TNFα, IL-1β, IL-4, TGF-β), а такі показники, як CD3 (загальна популяція Т-лімфоцитів), CD4 (Т-хелпери), NK-клітини, сіромукоїди, IL-6 – не дозволяє провести їх розмежування між собою.
Визначені імунологічні діагностичні показники для диференціації РКС від ГІМБГ і АХС та РКС від АКМП і ДКМП наведені в таблиці 5.
Таблиця 5
Визначення імунологічних показників для диференціації РКС від ГІМБГ і АХС та РКС від АКМП і ДКМП
| Патогенетичне розмежування причин РКС | З атеросклеротичним ураженням | Без атеросклеротичного ураження | ||
| показники | ГІМБГ | АХС | АКМП | ДКМП |
| CD8, % | 27±2,5 | 17±2,3 | 31±1,9 | 26±1,6 |
| р<0,01 | р<0,001 | |||
| CD21, % | різниця не достовірна | 10±1,6 | 7±1,5 | |
| р<0,05 | ||||
| NK, % | 14±1,5 | 24±2,1 | різниця не достовірна | |
| р<0,001 | ||||
| Сіромукоїди, у.о | 0,057±0,01 | 0,134±0,02 | різниця не достовірна | |
| р<0,001 | ||||
| TNFα, пг/мл | 91,5±5,6 | 73,5±2,3 | 57,23±2,4 | 48,2±2,1 |
| р<0,01 | р<0,01 | |||
| IL-1β, пг/мл | різниця не достовірна | 37,63±1,4 | 31,63±1,8 | |
| р<0,01 | ||||
| IL-6, пг/мл | 99,7 ±1,9 | 73,6 ±1,9 | різниця не достовірна | |
| р<0,001 | ||||
| IL-4, пг/мл | 86,6±4,2 | 64,2±2,5 | 38,9±1,5 | 45,2±1,9 |
| р<0,001 | р<0,01 | |||
| TGF-β, нг/мл | різниця не достовірна | 16,3±0,8 | 20,8±1,3 | |
| р<0,01 | ||||
Біохімічні дослідження. Діагностичними критеріями в тканині серця для диференціації РКС з атеросклеротичним механізмом формування змін у міокарді (АХС та ГІМБГ) є концентрації ЛДГ, МДА, ДК, каталази, а визначення SH-груп виявилось недостовірним. У сироватці крові діагностичними критеріями є вміст ЛДГ, МДА, ДК та каталази.
Показник ендогенної інтоксикації – МСВ є діагностичним критерієм для РКС з неатеросклеротичним механізмом формування змін в міокарді (АКМП і ДКМП), що доречно застосовувати для їх диференціації (табл. 6).
Таблиця 6
Визначення біохімічних показників для диференціації РКС від ГІМБГ і АХС та РКС від АКМП і ДКМП
| Патогенетичне розмежування причин РКС | з атеросклеротичним ураженням | без атеросклеротичного ураження | ||||
| показники | ГІМБГ | АХС | АКМП | ДКМП | ||
| Стан АОС/ПОЛ у міокарді | ||||||
| ЛДГ, ммоль/хв.г білка | 42,8±0,6 | 35,7±0,7 | 29,7±0,8 | 39,3±0,9 | ||
| р<0,001 | р<0,001 | |||||
| МДА, мкмоль/г білка | 19,9±0,8 | 17,3±0,7 | 14,9±0,6 | 19,8±0,6 | ||
| р<0,02 | р<0,001 | |||||
| ДК, мкмоль/г білка | 7,8±0,5 | 5,3±0,4 | 3,4±0,6 | 7,1±0,7 | ||
| р<0,001 | р<0,001 | |||||
| Каталаза, ммоль/хв.г білка | 6,8±0,5 | 10,2±0,7 | 15,8±0,9 | 7,5±0,5 | ||
| р<0,001 | р<0,001 | |||||
| SH-групи | різниця не достовірна | 61±1,8 | 66±1,8 | |||
| р<0,05 | ||||||
| Стан АОС/ПОЛ у сироватці (плазмі) крові | ||||||
| ЛДГ, мккат/л | 39,9±0,8 | 33,7±0,8 | різниця не достовірна | |||
| р<0,001 | ||||||
| МДА, мкмоль/л | 19,8±0,8* | 12,9±0,9* | 10,2±0,7* | 14,8±0,8* | ||
| р<0,001 | р<0,001 | |||||
| ДК, мкмоль/л | 6,9±0,9 | 3,9±0,6 | 2,7±0,6 | 4,8±0,7 | ||
| р<0,01 | р<0,05 | |||||
| Каталаза, мккат/г Нв | 5,4±0,6 | 8,2±0,8 | 10,6±0,9 | 6,5±0,7 | ||
| р<0,01 | р<0,001 | |||||
| Рівень ендогенної інтоксикації | ||||||
| МСВ, у.о | різниця не достовірна | 0,08±0,006 | 0,24±0,009 | |||
| р<0,001 | ||||||
Диференціація РКС з неатеросклеротичним механізмом формування змін у міокарді (АКМП та ДКМП) має враховувати такі діагностичні показники в міокарді, як концентрація ЛДГ, МДА, ДК, каталази, SH-груп, а в сироватці крові - МДА, ДК, каталази. Що ж стосується серцевої фракції ЛДГ, то її зміни виявились недостовірними.
Таким чином, використання імунометаболічних показників дозволяє оптимізувати судово-медичну діагностику випадків РКС при атеросклеротичному ураженні міокарда (АХС та ГІМБГ) й неатеросклеротичному ураженні (АКМП та ДКМП) та обґрунтувати післямортальний діагноз з точки зору патофізіологічних процесів.
ВИСНОВКИ
У дисертації вперше вирішене актуальне завдання, що полягало у підвищенні ефективності судово-медичної діагностики РКС від АХС, ГІМБГ, АКМП, ДКМП з урахуванням морфологічних, імунологічних та біохімічних змін.
1. Середній показник смертності населення регіону, який обслуговує відділ №2 ХОБСМЕ, за період 2001-2006 рр, від ССЗ склав 1,64 на 1000 населення, що у 4 рази нижче за аналогічний показник по Україні, який дорівнював 6,56.
2. Морфологічні макро- та мікроскопічні зміни в міокарді осіб, РКС яких настала від атеросклеротичного (АХС, ГІМБГ) та неатеросклеротичного (АКМП, ДКМП) ураження, є показовими й вірогідними, а їх поява обумовлюється комплексом імунометаболічних порушень в організмі та серцевому м´язі при цих захворюваннях, що може бути використано для обґрунтування причини РКС .
3. Морфологічні зміни в міокарді осіб, РКС яких настала від АХС, ГІМБГ, АКМП та ДКМП, різняться за своєю імуногістохімічною характеристикою.
Імуногістохімічно міокард при АХС характеризується наявністю малочислених нейтрофільних гранулоцитів, плазмоцитів з IgM та IgG, макрофагів, чисельними лімфоцитами й клітинами-продуцентами цитокінів, осередковим світінням колагену. У міокарді осіб, смерть яких настала від ГІМБГ, виявлено клітини–продуценти лімфоцитів, моноцити, підвищену кількість клітин-продуцентів інтерлейкінів. При РКС від АКМП виявлено переваскулярні лімфогістіоцитарні інфільтрати, поодинокі лімфоцити, а при ДКМП – NK-клітини в стромі міокарду, світіння ендотеліоцитів, макрофагальну реакцію та реакцію плазмобластної трансформації, прояви яких зменшені порівняно з контрольною групою.
Для імуногістохімічного розмежування РКС з атеросклеротичним механізмом формування змін у міокарді - АХС та ГІМБГ діагностичне значення мають клітини – продуценти лімфоцитів, а також клітини-продуценти цитокінів.
Для розмежування РКС з неатеросклеротичним механізмом формування змін у міокарді (АКМП і ДКМП) діагностичним критерієм може бути тільки наявність основних клонів клітин-продуцентів цитокінів.
4. Діагностично значущими імунологічними показниками крові при РКС з атеросклеротичним ураженням міокарду (АХС і ГІМБГ) є Т-цитотоксичні лімфоцити (CD8), NK-клітини, сіромукоїди, цитокіни (TNFα, IL-6, IL-4), а при РКС з неатеросклеротичним ураженням міокарду (АКМП і ДКМП) - Т-цитотоксичні лімфоцити (CD8), В-клітини (CD21), цитокіни (TNFα, IL-1β, IL-4, TGF-β).
5. Біохімічна диференціація РКС від АХС порівняно з ГІМБГ базується на виявленні у міокарді ЛДГ, МДА, ДК, каталази, в сироватці крові – ЛДГ, МДА, ДК, каталази; при диференціації РКС від АКМП порівняно з ДКМП враховують вміст у міокарді ЛДГ, МДА, ДК, каталази, SH-групи, в сироватці крові - МДА, ДК, каталази. Що ж стосується МСВ, то їх концентрація як показника ендогенної інтоксикації, дозволяє провести розмежування РКС від АКМП і ДКМП.
6. Використання комплексу імунометаболічних показників дозволяє оптимізувати судово-медичну діагностику випадків РКС при атеросклеротичному ураженні (АХС та ГІМБГ) й неатеросклеротичному ураженні (АКМП та ДКМП) міокарду.
ПРАКТИЧНІ РЕКОМЕНДАЦІЇ
За результатами проведеного дослідження для підвищення ефективності диференціальної діагностики РКС від АХС, ГІМБГ, АКМП, ДКМП пропонуємо для впровадження в практику судово-медичної експертизи окрім загальновідомих методів дослідження:
1.Для диференціальної діагностики РКС, що обумовлена ССЗ, використовувати алгоритм проведення судово-медичного дослідження за допомогою лабораторних методів діагностики.
2.Проводити диференціацію РКС від ДКМП і АКМП за такими лабораторними показниками: визначення CD8, CD21, TNFα, IL-1β, IL-4, клітинного цитокіну з дозозалежною активністю TGF-β, ЛДГ, МДА, ДК, каталази, SH-груп у міокарді, МСВ у плазмі крові, що є достовірними для розмежування цих видів смерті.
3.Проводити диференціацію РКС від АХС і ГІМБГ на підставі достовірних критеріїв, що є CD8, NK, сіромукоїди, TNFα, IL-6, IL-4, ЛДГ, МДА, ДК, каталази у сироватці крові.
4.Диференційна діагностика РКС від АХС, ГІМБГ, ДКМП, АКМП повинна здійснюватись шляхом комплексного використання патоморфологічних, гістологічних, імунологічних та біохімічних методів дослідження, що є доречним, об`єктивним і достовірним критерієм для офіційного висновку про причину смерті.
5. Визначений комплекс імунопатогенетичних причин РКС від АХС, ГІМБГ, ДКМП, АКМП розширює уявлення про виникнення патологічних станів, які призводять до РКС, що доречно впровадити в навчальний процес, лекційні курси та практичні заняття кафедр судової медицини та патологічної анатомії медичних ВУЗів України та в практичну діяльність судово-медичних експертів.
СПИСОК ОПУБЛІКОВАНИХ ПРАЦЬ ЗА ТЕМОЮ ДИСЕРТАЦІЇ
1. Мішин М.Ю. Особливості змін імунного профілю при раптовій кардіальній смерті // Український судово-медичний вісник. - 2006. - №2 (19). – С. 23 – 25.
2. Мішин М.Ю. Особливості процесів перекисного окислення при раптовій кардіальній смерті // Український судово-медичний вісник. - 2007. - №1 (20). – С. 40 – 42.
3. Ольховський В.А., Мишин М.Ю. Статистический анализ динамики кардиальной смертности по данным ХОБСМЭ №2 за 2001 – 2006 годы //Медицина сьогодні і завтра. - 2007. - № 3. – С. 75- 77. (Здобувачем проведено статистичний аналіз динаміки РКС за даними ХОБСМЕ №2 за період 2001 – 2006 рр.).
4. Ольховський В.О., Мішин М.Ю. Сучасний погляд на проблему судово-медичної діагностики нозологічних форм раптової смерті //V Міжнародний конгрес з інтегративної антропології, Вінниця, 3-4 червня 2004. - Biomedical and Biosocial Anthropology, 2004. - №2. – С.66. (Здобувачем проведено аналіз даної проблеми за оглядом сучасної літератури й викреслено аспекти діагностичних досліджень РКС).
5. Цыганенко А.Я., Ольховский В.А., Мишин М.Ю., Мишина М.М. Показатели цитокинового баланса при внезапной сердечной смерти//Матеріали науково-практичної конференції з міжнародною участю, присвяченої 200-річчю з дня заснування ХДМУ «Від фундаментальних досліджень до прогресу в медицині». Харків 17-18 січня, 2005. – Харків, 2005. - С. 68. (Здобувачем узагальнено результати проведених досліджень цитокінового стану при РКС від АХС, ГІМБГ, АКМП, ДКМП та проведено статистична оцінка розходження визначених показників).
6. Ольховский В.А., Мишин М.Ю. Антиоксидантный статус при внезапной кардиальной смерти, обусловленной атеросклеротической болезнью сердца //Матеріали міжнародної науково-практичної конференції судових медиків та криміналістів, присвяченої 200-річчю кафедри судової медицини та основ права ХДМУ «Актуальні питання та перспективи розвитку судової медицини та криміналістики». Харків, 14-16 вересня 2005. – Харків, 2005 – С. 168 – 169. (Здобувачем зібрано фактичний матеріал лабораторних досліджень антиоксидантної системи та стану перекисного окислення ліпідів при РКС та узагальнено результати дослідження).
7. Ольховский В.А. Мишин М.Ю., Вороной Ю.Ю., Карпенко В.А. Критерии цитокинового статуса при внезапной кардиальной смерти //Матеріали Першої міжнародної науково-практичної конференції судових медиків і криміналістів, присвяченої 75-річчю з дня смерті Заслуженого проф. М.С.
8-09-2015, 23:08
