При кількісному динамічному моніторингу концентрації NSEу пацієнтів, що отримували стандартну терапію (1 група), були виявлені наступні зміни (рис. 4). На 2-3 добу відзначався значний підйом концентрації даного білка до 30,8 ± 5,1 нг/мл,що у 2,5 рази більше донорського рівня. У подальшому на 6-7 добу відзначалося достовірне (р = 0,005)зниження концентрації NSEдо рівня 18,8 ± 2,1 нг/мл. Нормалізація концентрації NSEвідзначалася на 13-15 добу посттравматичного періоду. Дана динаміка концентрації нейронспецифічної енолази відповідає концепції вторинних ішемічних ушкоджень головного мозку.
При кількісному динамічному моніторингу концентрації GFAPу пацієнтів, що отримували додатково до стандартної терапії L-лізину есцинат (2 група) були виявлені наступні зміни (рис. 5). На 2-3 та 6-7 добу концентрація даного білка складала 7,8 нг/мл та 11,4 нг/мл відповідно та була достовірно вище донорського рівня (p< 0,05) та достовірно нижче, ніж у пацієнтів 1 групи (p< 0,05). Це свідчить про здатність протинабрякового препарату L-лізіину есцинату зменшувати вторинну загибель астроцитів у період максимально вираженого набряку головного мозку та стабілізувати ГЕБ. У подальшому концентрація GFAPне відрізнялася від пацієнтів 1 групи та була достовірно вище донорського рівня (p< 0,05).
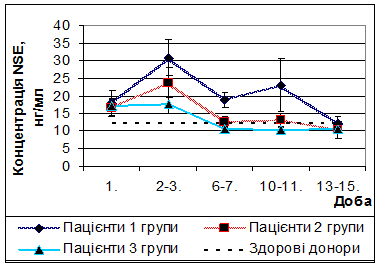
Рис. 4 Динаміка концентрації нейронспецифічної енолази у пацієнтів досліджуваних груп.
При кількісному динамічному моніторингу концентрації NSEу пацієнтів, що отримували додатково до стандартної терапії L-лізину есцинат (2 група) були виявлені наступні зміни (рис. 4). На 2-3 добу відзначався пік концентрації NSE(23,7 ± 4,1 нг/мл),проте на 23% менший, аніж у пацієнтів 1 групи.
Нормалізація концентрації NSEу сироватці крові пацієнтів 2 групи наступала на 6-7 добу, у той час, як у пацієнтів, що отримували стандартну терапію, вона досягала норми лише на 13-15 добу після травми. Це свідчить про здатність L-лізину есцинату у комплексі інтенсивної терапії тяжкої ЧМТ вже на 6-7 добу стабілізувати ГЕБ та зменшувати вторинні ушкодження нейронів.
При кількісному динамічному моніторингу концентрації GFAPу пацієнтів, що отримували додатково до стандартної терапії L-лізину есцинат та мексидол (3 група) були виявлені наступні зміни (рис. 5). На 2-3добу концентрація GFAPбула на 65,6% менше, аніж у пацієнтів 1 групи. У подальшому, на протязі всього періоду спостереження (з 2 до 15 доби), концентрація GFAPу пацієнтів 3 групи була нижче, ніж у пацієнтів 1 групи, та – на 13-15 добу – ніж у пацієнтів 2 групи, проте була вищою за донорський рівень. Це свідчить про здатність у комбінації L-лізину есцинату та мексидолу стабілізувати ГЕБ та зменшувати відстрочену загибель астроцитів.
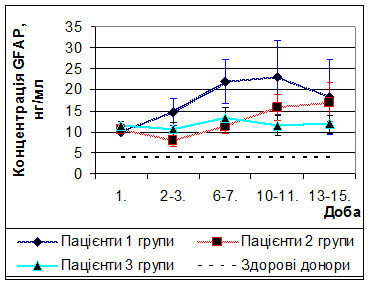
Рис. 5 Динаміка концентрації гліофібрилярного кислого протеїну у пацієнтів досліджуваних груп
При кількісному динамічному моніторингу концентрації NSEу пацієнтів, що отримували додатково до стандартної терапії L-лізину есцинат та мексидол (3 група), були виявлені наступні зміни (рис. 4). На 2-3 добу концентрація NSEу сироватці крові була достовірно (р < 0,05)вищою за донорський рівень та достовірно (р < 0,05)нижчою, аніж у пацієнтів 1 групи. На 6-7 добу концентрація NSEбула у межах норми та була достовірно (р < 0,05) нижчою, аніж у пацієнтів 1 групи. В подальшому концентрація NSEне підвищувалася. Відсутність підйому концентрації нейронспецифічної енолази на 2-3 добу у пацієнтів 3 групи, а також її швидка нормалізація свідчить про значний нейропротекторний ефект у комбінації L-лізину есцинату та мексидолу у комплексі інтенсивної терапії тяжкої ЧМТ.
Для клінічного аналізу ефективності запропонованих методів інтенсивної терапії тяжкої ЧМТ використовувались наступні параметри: динаміка рівня свідомості та тривалість ШВЛ у пацієнтів, що вижили, та летальність.
Рівень порушення свідомості оцінювався в балах шкали ком Глазго в динаміці травматичної хвороби головного мозку.
При надходженні рівень порушення свідомості у пацієнтів 1, 2 та 3 груп складав 7,0 ± 0,18 бала, 7,0 ± 0,16 бала и 6,8 ± 0,20 бала відповідно (табл. 1). На 2-3 добу рівень свідомості збільшився у пацієнтів 1 групи на 0,7 бала, у пацієнтів 2 групи на 1,1 бала та у пацієнтів 3 групи – на 1,3 бала. Дана динаміка корелювала з концентрацією нейронспецифічної енолази (- 0,43 > r> - 0,56). На6-7добу середній рівень свідомості у пацієнтів 1 групи підвищувався на 2 бали, в 2 групі – на 2,2 бали та в 3 групі - на 2,7 бали. Загалом під час спостереження у пацієнтів 1 групи свідомість відновилась на 4,6 бали, у пацієнтів 2 групи – на 4,8 бали, а у пацієнтів 3 групи – на 5,4 бали. Більш швидкий темп відновлення свідомості у пацієнтів 2 та 3 груп, порівняно з 1 групою, що корелює зі ступенем загибелі нейронів, вказує на ефективність оптимізованих методів інтенсивної терапії в профілактиці вторинних ішемічних пошкоджень.
Таблиця 1
Динаміка рівню свідомості (бали ШКГ) у пацієнтів досліджуваних груп, що вижили, M± m
1 доба |
2-3 доба |
6-7 доба |
10-11 доба |
13-15 доба |
|
| 1 група(n=31) | 7,0 ± 0,18 | 7,7 ± 0,25 | 9,0± 0,32 | 10,6 ± 0,38 | 11,6 ± 0,34 |
| 2 група(n=25) | 7,0 ± 0,16 | 8,1± 0,26 | 9,2± 0,36 | 10,9± 0,34 | 11,8± 0,40 |
| 3 група(n=29) | 6,8± 0,20 | 8,0± 0,35 | 9,5± 0,43 | 11,1± 0,50 | 12,2± 0,39 |
Штучна вентиляція легенів у пацієнтів досліджуваних груп проводилась з моменту надходження до моменту відновлення свідомості вище 8 балів ШКГ частотним респіратором PLV-100 в режимі нормовентиляції (ДО = 6 - 7 мл/кг, ЧД = 16-18 в 1 хв, FiO2 = 30%). При проведенні кореляційного аналізу нами було виявлено, що тривалість ШВЛ залежить від первинного рівня порушення свідомості (r= - 0,72) та від віку пацієнта (r= 0,53), а від тривалості ШВЛ залежить частота розвинення вентилятор-асоційованої пневмонії (r= - 0,47).
Враховуючи, що рівень порушення свідомості при надходженні та вік пацієнтів усіх груп співставимі, тривалість ШВЛ визначалась характером та ефективністю інтенсивної терапії, що проводилась.
Таблиця 2
Тривалість ШВЛ у пацієнтів досліджуваних груп, що вижили, M± m
| Кількістьтрахеостом | Кількість вентилятор-асоційованих пневмоній | ТривалістьШВЛ, діб, M± m |
|||
| Кількість пацієнтів | % | Кількість пацієнтів | % | ||
| 1 група(n=31) | 11 | 35,5 | 11 | 35,5 | 8,9±0,21 |
| 2 група(n=25) | 9 | 36,0 | 8 | 32,0 | 7,4±0,28 |
| 3 група(n=29) | 10 | 34,4 | 8 | 27,6 | 6,3±0,17 |
При порівнянні термінів переходу на самостійне дихання нами було встановлено (табл. 2), що у пацієнтів 1 групи середня тривалість ШВЛ становила 8,9 ± 0,21 діб, при цьому вентилятор-асоційована пневмонія виявлена в 35,5% випадків. У пацієнтів 2 групи середня тривалість ШВЛ становила 7,4 ± 0,28 доби, вентилятор-асоційована пневмонія виявлена у 32% пацієнтів. Пацієнти 3 групи знаходились на ШВЛ, в середньому, 6,3 ± 0,17 діб та вентилятор-асоційованапневмоніярозвивалася у них в 27,6% випадків. Таким чином, нами встановлено, що у пацієнтів, які отримували L-лізину ецинат додатково до стандартної терапії, тривалість ШВЛ була на 16,9% менше, аніж у пацієнтів, що отримували стандартну терапію, частота розвитку пневмонії у них, у зв’язку з цим, була на 9,8% менше, ніж у пацієнтів 1 групи. Пацієнти, що отримували комплекс препаратів L-лізинуесцинатта мексидол, знаходились на ШВЛ на 29,2% менше часу (p< 0,05), ніж пацієнти, що отримували стандартну терапію. Частота розвитку пневмонії, у зв’язку з цим, в них була на 22,3% менше, ніж у пацієнтів 1 групи. Це свідчить про ефективність обох варіантів інтенсивної терапії у порівнянні із стандартною терапією та про більшу ефективність у комбінації препаратів L-лізина есцинат та мексидол в порівнянні з L-лізину есцинату без мексидолу.
При аналізі летальності було встановлено, що загальна летальність у пацієнтів, що досліджувались, склала 55,5%. Найбільша кількість пацієнтів (37%) померли впродовж перших 10 діб на фоні набряку головного мозку.
У пацієнтів, що померли після 10 діб, відзначалося зростання поліорганних порушень: пневмонія виявлена у 62% пацієнтів, нефропатія – у 35,5% пацієнтів, ознаки печінкової недостатності – у 19% пацієнтів. Проаналізувавши фактори, що впливають на результати хвороби, ми отримали наступні дані: негативні наслідки залежать від первинного рівня порушень свідомості (r= 0,71), віку пацієнта (r= 0,54) та не залежить від розвитку пневмонії.
Враховуючи, що рівень порушення свідомості при надходженні та вік пацієнтів усіх груп співставимі, летальність визначалася характером та ефективністю інтенсивної терапії, що проводилась.
Летальність в 1 групі становила 59,3%, з яких 71% пацієнтів помер в продовж перших 10 діб, летальність в 2 групі становила 56,9%, з яких 72% пацієнтів померло в строк до 10 діб, а в 3 групі померло 49,2% пацієнтів, з яких 57% в строк до 10 діб.
Таким чином, летальність при тяжкій ЧМТ на 3,1% нижче в групі пацієнтів, що отримували L-лізина есцинат, а також достовірно (p< 0,05) нижче на 10,1% в групі пацієнтів, що отримували комплекс препаратів L-лізину есцинат та мексидол, в порівнянні з пацієнтами, що отримували стандартну терапію. Зниження летальності в 3 групі пов’язане зі зменшенням ранньої летальності, обумовленої набряком головного мозку та вторинною його ішемією. У пізні строки (після 10 діб) у пацієнтів 3 групи рідше відзначалися пневмонія, нефропатія та порушення функцій печінки.
ВИСНОВКИ
В дисертації наведене узагальнення та нове розв’язання актуального наукового завдання – визначення діагностичної ролі нейроспецифічних білків нейронспецифічної енолази та гліофібрилярного кислого протеїну при ушкодженні гематоенцефалічного бар’єру у хворих на тяжку черепно-мозкову травму, - та вирішення актуальної клінічної задачі – удосконалення інтенсивної терапії тяжкої черепно-мозкової травми завдяки уведенню до її складу комплексу препаратів L-лізину есцинату та мексидолу.
1. Ізольована тяжка черепно-мозкова травма найбільш часто зустрічається в осіб, що страждають на хронічний алкоголізм (67,5 %), в результаті падіння з висоти росту (84,8 %). Найбільш характерними її проявом є субдуральна гематома (64,9 %).
2. У сироватці крові умовно здорових донорів виявляються нейроспецифічні білки в концентраціях, що не перевищують: 4,1 нг/мл для гліофібріляторного кислого протеїна та 12,4 нг/мл для нейронспецифічної енолази.
3. У перші 6 годин тяжкої черепно-мозкової травми має місце підвищення концентрації нейроспецифічних білків порівняно з донорським рівнем. Це дозволяє припустити наявність прориву гематоенцефалічного бар’єру у гострому періоді тяжкої черепно-мозкової травми.
Нейронспецифічна енолаза (NSE), що є маркером нейронального ушкодження, підвищується у першу добу в 1,4 рази в порівнянні з верхньою межею норми. Концентрація нейронспецифічної енолази корелює з рівнем порушення свідомості (r= - 0,57), що дозволяє вважати її маркером тяжкості нейротравми.
Гліофібрілярний кислий протеїн (GFAP), що є маркером ушкодження астроглії, підвищується у першу добу в 2,5 рази в порівнянні з верхньою межею норми.
4. У пацієнтів, що отримували стандартний комплекс інтенсивної терапії тяжкої черепно-мозкової травми динаміка концентрації нейроспецифічних білків була такою:
- концентрація нейронспецифічної енолази була максимальною в перші 2-3 доби, що свідчить про найбільший загибель нейронів в цей період, з наступним достовірним (р = 0,005) зниженням до 6-7 доби та нормалізацією на 13-15 добу;
- концентрація гліофібрілярного кислого протеїну найбільш значно підвищувалась після 7 доби, без тенденції до нормалізації до кінця дослідження (13-15 доба), що є свідоцтвом розвитку реактивного астрогліозу в цей період.
5. Раннє (з першої доби) призначення препарату L-лізину есцинату в дозі 20 мл/добу у комплексі інтенсивної терапії тяжкої черепно-мозкової травми дозволяє зменшити елімінацію в кров гліофібрилярного кислого протеїну на 46,9%, а нейронспицефічної енолази на 23%, в порівнянні із стандартною терапією, та припинити надходження NSEу кров до 6-7 доби.
Раннє (з першої доби) призначення препарату L-лізину есцинату в дозі 20 мл/добу одночасно з мексидолом 800 мг/добу в комплексі інтенсивної терапії тяжкої черепно-мозкової травми дозволяє зменшити елімінацію в кров нейронспецифічної енолази на 44,2 %.
6. Включення до складу інтенсивної терапії L-лізину есцинату в дозі 20 мл/добу дозволяє зменшити летальність на 2,4%, прискорити відновлення свідомості на 4,2%, зменшити тривалість ШВЛ на 16,9%, у порівнянні із стандартною терапією. Найбільш істотне зниження летальності відзначалося в період до 10 діб, коли прояви набряку головного мозку є максимальними.
Включення до складу інтенсивної терапії комплексу препаратів L-лізину есцинату в дозі 20 мл/добу та мексидолу 800 мг/добу дозволило зменшити летальність на 10,1%, прискорити відновлення свідомості на 17,4%, зменшити тривалість ШВЛ на 29,2%, у порівнянні зі стандартною терапією.
ПРАКТИЧНІ РЕКОМЕНДАЦІЇ
Для оцінки проникності гематоенцефалічного бар’єру та оцінки ефективності інтенсивної терапії тяжкої черепно-мозкової травми:
- використання методу іммунохімічного аналізу нейроспецифічних білків гліофібрилярного кислого протеїну та нейронспецифічної енолази в сиворотці крові у комплексі. Якщо концентрація GFAPперевищує 4,1 нг/мл, а також концентрація NSEперевищує 12,4 нг/мл діагностують порушення проникності гематоенцефалічного бар’єру при тяжкій черепно-мозковій травмі.
Для підвищення ефективності інтенсивної терапії тяжкої черепно мозкової травми:
- раннє (з перших годин) включення комплексу препаратів L-лізину есцинату в дозі 20 мл/добу одночасно з мексидолом 800 мг/добу до схеми інтенсивної терапії пацієнтів тяжкою черепно-мозковою травмою.
ПЕРЕЛІК ПРАЦЬ, ОПУБЛІКОВАНИХ ЗА ТЕМОЮ ДИСЕРТАЦІЇ
1. Лизогуб Н.В. Возможности исследования нейроспецифических белков в сыворотке крови больных с тяжёлой черепно-мозговой травмой/ Н.В. Лизогуб, О.И. Гурина // Матеріали IVз’їзду нейрохірургів України, (Дніпропетровськ, 27-30 травня 2008 р.) // Дніпропетровськ, ТОВ «ЕНЕМ», 2008. – С. 209.
Дисертантом особисто проводилось обстеження хворих, лікування, забір матеріалу для дослідження, узагальнення результатів дослідження, написаний та представлений текст доповіді.
2. Лизогуб М.В. Імуноферментний аналіз нейроспецифічних антигенів у діагностиці важкої черепно-мозкової травми / М.В. Лизогуб, А.А. Хижняк, О.І. Гуріна // Врачебная практика. – 2007. - №5(59). – С. 72-75.
Дисертантом особисто зібраний клінічний матеріал, написаний текст статті.
3. Лизогуб Н.В. Влияние L-лизина эсцината и мексидола на проницаемость гематоэнцефалического барьера при тяжёлой черепно-мозговой травме / Н.В. Лизогуб, А.А. Хижняк, О.И. Гурина // Український журнал екстремальної медицини ім. Г.О. Можаєва. – 2007. –Т.8, №4. – С. 45-47.
Дисертантом особисто визначена мета наукової роботи, зібраний клінічний матеріал, написано розділ, де викладено результати дослідження.
4. Хижняк А.А. Нейроспецифічні білки – перспективні маркери ураження головного мозку при черепно-мозковій травмі /А.А. Хижняк, М.В. Лизогуб // Біль, знеболювання та інтенсивна терапія. – 2006. - №2. – С. 23-28.
Дисертантом особисто проведений літературний пошук, написаний розділ, що присвячений нейроспецифічним білкам.
5. Клініко-імунохімічне визначення впливу препарату L-лізину есцинат на проникність гематоенцефалічного бар’єру при важкій черепно-мозковій травмі / А.А. Хижняк, В.П. Чехонін, О.І. Гуріна, М.В. Лизогуб // Біль, знеболювання та інтенсивна терапія. – 2006. - №1(д). – С. 245-246.
Дисертантом особисто визначена мета наукової роботи, зібраний клінічний матеріал, написано розділ, де викладено результати дослідження.
6. Хижняк А.А. Эффекты глюкокортикоидов и терапия при тяжёлой черепно-мозговой травме / А.А. Хижняк, С.В. Курсов, Н.В. Лизогуб // Біль, знеболювання та інтенсивна терапія. – 2004. - №1. – С. 29-40.
Дисертантом особисто проведений літературний пошук, написаний розділ, що присвячений інтенсивній терапії.
7. Лікування хворих на важку черепно-мозкову травму в умовах відділення інтенсивної терапії / Ієвлева В.І., Курсов С.В., Лизогуб М.В. [та ін.] // Неотложная медицинская помощь: зб. наук. праць. – Харьков: “Основа”, 2004. – С. 278-281.
Дисертантом особисто проводилось обстеження хворих, лікування, написаний розділ, що присвячений інтенсивній терапії.
8. Хижняк А.А. Вторинні ішемічні ушкодження головного мозку та алгоритм боротьби із ними при тяжкій черепно-мозковій травмі : [метод. рекомендації] / А.А. Хижняк, М.В. Лизогуб. – Київ, 2008. – 12 с.
Дисертантом особисто описані результати досліджень та сформульовані висновки та практичні рекомендації.
9. Пат. 32463 Україна, МПК G01 N33/00.Спосіб діагностики стану гематоенцефалічного бар’єру при тяжкій черепно-мозковій травмі / Хижняк А.А., Гуріна О.І., Лизогуб М.В.; заявник та патентовласник Харківський національний медичний університет. - № u200801906 ; заявл. 14.02.08 ; опубл. 12.05.08, Бюл. №9
АНОТАЦІЯ
Лизогуб М.В. Клініко-імунохімічна оцінка ефекту «захисту мозку» при тяжкій черепно-мозковій травмі. – Рукопис.
Дисертація на здобуття наукового ступеня кандидата медичних наук за спеціальністю 14.01.30 – анестезіологія та інтенсивна терапія. – Донецький національний медичний університет, Донецьк, 2008.
Дисертація присвячена питанням діагностики пошкодження гематоенцефалічного бар’єру та інтенсивній терапії тяжкої черепно-мозкової травми (ТЧМТ). Проаналізовано результати лікування 191 пацієнта з ТЧМТ, наведені особливості епідеміології та клінічних проявів. Нами був розроблений імуноферментний аналіз нервовоспецифічних білків гліофібрилярного кислого протеїну та нейронспецифічної енолази та було проведене дослідження цих білків у сироватці крові 45 здорових донорів та 46 пацієнтів з ТЧМТ у динаміці. Показано, що у гострому періоді ТЧМТ має місце прорив гематоенцефалічного бар’єру з елімінацією у кров нервовоспецифічних білків, та визначено їх роль у діагностиці ТЧМТ. Була удосконалена схема інтенсивної терапії ТЧМТ за допомогою включення до її складу L-лізину есцинату та мексидолу. Запропонована схема інтенсивної терапії дозволила знизити летальність при тяжкій ЧМТ на 10,1%, прискорити відновлення свідомості на 17,4% та зменшити тривалість ШВЛ на 29,2%, а також зменшити елімінацію у кров нервовоспецифічних білків гліофібрилярного кислого протеїну та нейронспецифічної енолази.
Ключові слова: тяжка черепно-мозкова травма, гліофібрилярний кислий протеїн, нейронспецифічна енолаза, L-лізину есцинат, мексидол.
АННОТАЦИЯ
Лизогуб Н.В. Клинико-иммунохимическая оценка эффекта «защиты мозга» при тяжёлой черепно-мозговой травме. – Рукопись.
Диссертация на соискание учёнойстепени кандидата медицинских наук по специальности 14.01.30 – анестезиология и интенсивная терапия. – Донецкий национальный медицинский университет, Донецк, 2008.
Диссертация посвящена вопросам диагностики целостности гематоэнцефалического барьера и интенсивной терапии при тяжёлой черепно-мозговой травме (ТЧМТ). В исследование включены 191 пациент с тяжёлой ЧМТ и 45 здоровых доноров. Пациентам проводилось общеклиническое, биохимическое исследование, МРТ головного мозга, иммунохимические (определение концентрации нейроспецифических белков
8-09-2015, 22:15
