Опухолевые клетки в плевральной жидкости обнаруживают лишь у 20-30% больных мезотелиомой. В большинстве случаев верификация диагноза становится возможной после проведения торакоскопии и биопсии париетальной плевры.
Плевральный выпот при аллергических и аутоиммунных заболеваниях и синдромах
Многие аллергические и аутоиммунные заболевания и синдромы могут сопровождаться развитием неинфекционного (асептического) воспалительного процесса в плевре и образованием плеврального выпота, который носит характер экссудата. Таким образом, формируются аллергические и аутоиммунные экссудативные плевриты неиифекционного генеза.
Экссудативный плеврит при постинфарктном синдроме Дресслера является наиболее типичным примером аутоиммунного механизма образования плеврального выпота. Напомним, что синдром Дресслера развивается у части больных инфарктом миокарда на 2-6 неделе от начала заболевания и включает в себя типичную триаду — перикардит, плеврит, пневмонит.
Плеврит может быть как двусторонним, так и односторонним. В начале возникновения этого осложнения появляются боли в грудной клетке, усиливающиеся при дыхании, выслушивается шум трения плевры. Когда в полости плевры накапливается экссудат, боли прекращаются, и шум трения плевры не выслушивается. При объективном исследовании может определяться небольшое притупление перкуторного звука и ослабление дыхания па стороне поражения. Диагноз плеврального выпота подтверждается при рентгенологическом исследовании. В части случаев наблюдается небольшой лейкоцитоз и увеличивается СОЭ.
Плевральный выпот носит характер серозного или серозно-геморрагического экссудата лимфоцитарного или нейтрофильно-лимфоцитарного состава.
Под влиянием терапии глюкокортикоидами и НПВП экссудат рассасывается в большинстве случаев в течение 1-2 недель, хотя в отдельных случаях этот процесс затягиваетсяна несколько месяцев.
Экссудативные плевриты при системных заболеваниях соединительной ткани.
Поражение плевры может возникнуть при любом системном заболевании соединительной ткани. Однако наиболее часто (в 40-50% случаев) экссудативный плеврит развивается у больных системной красной волчанкой (СКВ), причем у части из них поражение плевры может явиться первым клиническим проявлением заболевания.
В большинстве случаев имеется двустороннее поражение плевры. Экссудат носит серозный характер, в нем содержится большое количество лимфоцитов. При биопсии плевры обнаруживают неспецифические признаки хронического воспаления и фиброза, ведущих к утолщению листков плевры. Природу выпотного плеврита устанавливают при обнаружении клинико-лабораторных признаков СКВ, в частности противоядерных антител и LE-клеток. Следует помнить, что выпотной плеврит при СКВ хорошо поддается терапии глюкокортикоидами, что может служить даже дифференциально-иагностическим признаком.
При ревматоидном артрите (РА) экссудативный плеврит развивается в 4-5% случаев. Нередко он носит рецидивирующий характер, плохо поддается терапии глюкокортикоидами и сопровождается образованием массивных плевральных спаек. В экссудате преобладают лимфоциты и мезотелиальные клетки, значительно снижена концентрация глюкозы и повышены титры ревматоидного фактора. При торакоскопии и пункционной биопсии выявляются признаки хронического воспаления, фиброза и васкулита.
Экссудативный плеврит при ревматизме выявляется в 2-3% случаев, часто сочетаясь артритом, перикардитом, миокардитом и эндокардитом аутоиммунного происхождения. Серозный экссудат содержит большое количество лимфоцитов и мезотелиальных клеток. При торакоскопии и биопсии плевры, так же как и при СКВ и РА, определяют хроническое воспаление и фиброз плевральных листков.
Экссудотивные плевриты при системных заболеваниях соединительной ткани характеризуются следующими особенностями:
- плевральный выпот носит характер серозного экссудата с высоким содержанием лимфоцитов и клеток мезотелия;
- при СКВ в экссудате можно обнаружить противоядерные антитела и LE-клетки, а при РА — высокие титры ревматоидного фактора;
- при торакоскопии и пункционной биопсии обычно обнаруживают признаки хронического воспаления и фиброза, тогда как специфические маркеры этих заболеваний (ревматоидные или ревматические узелки, типичная картина волчаночного васкулита и др.) выявляются крайне редко;
- в большинстве случаев природа плеврального выпота устанавливается на основании оценки всех, в том числе — внеплевральных, клинических проявлений заболевания и при исключении других возможных причин выпота (опухоль, инфекция и др.)
Панкреатогенный (ферментогенный) плевральный выпот
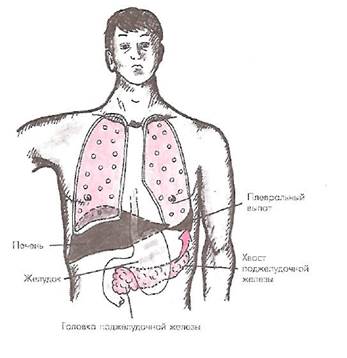
Папкреатогенный плевральный выпот обнаруживается примерно у 20-30% больных с острым или обострением хронического панкреатита (B.C. Савельев, 1983). Он развивается вследствие раздражающего действия панкреатических ферментов, проникающих в плевральную полость по лимфатическим сосудам через диафрагму. Благодаря близкому взаимному расположению хвоста поджелудочной железы и левого купола диафрагмы чаще встречается левосторонний плевральный выпот (рис. 38).
Рис. 38. Близкое расположение хвоста поджелудочной железы и левого купола диафрагмы, объясняющее частое возникновение левостороннего плеврального выпота при поражении поджелудочной железы.
При плевральной пункции получают серозный или серозно-геморрагический экссудат с высоким содержанием амилазы, концентрация которой превышает таковую в сыворотке крови.
Панкреатогенный экссудативный плеврит нередко выявляется только при рентгенологическом исследовании и имеет наклонность к рецидивированию.
Уремический плевральный выпот
При уремии плевральный выпот обусловлен раздражающим действием азотистых шлаков (мочевины, креатинина и др.), в большом количестве выделяющихся серозными оболочками и вызывающих их асептическое воспаление (плеврит, перикардит и т.д.). В плевральной полости накапливается серозно-фибринозный или геморрагический экссудат с небольшим количеством клеточных элементов и повышенным содержанием креатинина. Обычно прогностическое значение уремического плеврита, так же как и перикардита, весьма серьезное, и его появление свидетельствует о терминальной стадии почечной недостаточности.
Посттравматический плеврит
Механическая закрытая травма грудной клетки может сопровождаться развитием экссудативного плеврита, возникающего через несколько дней после травмы. У больных появляются боли в грудной клетке, связанные с дыханием, слабость, потливость, повышается температура тела. В анализах крови определяется небольшой лейкоцитоз и увеличение СОЭ.
Во время пункции плевральной полости в большинстве случаев получают геморраги ческий экссудат с высоким содержанием белка (более до 40-50 г/л), высокой относительной плотностью. В экссудате преобладают лимфоциты, количество мезотелиальных клеток понижено. В начале заболевания экссудат, как правило, стерилен. Однако, если профилактически не проводится рациональная антибактериальная терапия, экссудат может инфицироваться, и заболевание приобретает характер бактериального экссудативного плеврита. В отдельных случаях возможно образование гнойного плеврита (эмпиемы плевры).
Плевральные выпоты невоспалительного генеза
Застойный плевральный выпот (гидроторакс)
Застойный плевральный выпот (гидроторакс) возникает у больных с правожелудочковой и бивентрикулярной сердечной недостаточностью. Он обусловлен повышением гидростатического давления преимущественно в венозном русле большого круга кровообращения, что создает условия для повышения продукции и нарушения резорбции плевральной жидкости. Чаще наблюдается правосторонний плевральный выпот.
Клиническая картина характерна для больных с сердечной недостаточностью (одышка, отеки нижних конечностей, увеличение печени, цианоз, асцит и т.п.). Появление плеврального выпота у больных с сердечной недостаточностью обычно ассоциируется с тяжелым течением заболевания. В то же время значительный его объем, сопровождающийся коллабированием легкого, приводит к усугублению дыхательной недостаточности и усилению одышки.
При плевральной пункции в большинстве случаев (около 85%) получают серозный транссудат, хотя в ряде случаев возможно появление серозно-геморрагического и геморрагического выпота. Во всех случаях, относительная плотность плеврального выпота меньше 1,015, а содержание белка — меньше 30 г/л. Характерны также низкая активность ЛДГ (< 1,6 ммоль/л х ч, небольшой коэффициент «ЛДГ выпота/ЛДГ сыворотки» (< 0,6) и высокие значения отношения «глюкоза выпота/глюкоза сыворотки» (> 1,0). При микроскопии осадка определяется большое количество лимфоцитов и клеток мезотелия.
Следует добавить, что застойный плевральный выпот по понятным причинам не сопровождается болевым синдромом и не приводит к образованию плевральных сращений.
Плевральный выпот при тромбоэмболии легочной артерии (ТЭЛА)
При тромбоэмболии легочной артерии (ТЭЛА) плевральный выпот может быть обусловлен несколькими причинами. При массивной ТЭЛА, сопровождающейся развитием острого легочного сердца и правожелудочковой недостаточности, причиной плеврального выпота является остро возникшее повышение гидростатического давления в венозном русле большого круга кровообращения. В этих случаях плевральный выпот представляет собой типичный транссудат.
Если у больных с ТЭЛА развивается инфаркт легкого и инфарктная пневмония, плевральный выпот может носить характер экссудата, нередко геморрагического.
Таким образом, в каждом конкретном случае следует уточнять преобладающие механизмы образования плеврального выпота.
Плевральный выпот при уменьшении коллоидно-осмотического давления крови
Уменьшение коллоидно-осмотического давления крови, обусловленное гипопротеинемией, может сопровождаться развитием выраженного отечного синдрома в виде распространенных отеков подкожно-жировой клетчатки и водянки полостей (асцита, гидроторакса, гидроперикарда и т.д.). Наиболее частыми причинами гипопротеинемии являются нефротический синдром и заболевания печени с нарушением ее белковосинтетической функции, например циррозы печени.
В этих случаях плевральный выпот представляет собой транссудат с низкой относительной плотностью и содержанием белка. Выпот развивается постепенно и обычно маскируется другими симптомами основного заболевания. При значительных объемах выпота появляется и нарастает дыхательная недостаточность.
Хилезный плевральный выпот (хилоторакс)
Хилезный плевральный выпот — это скопление в плевральной полости лимфы, возникающее при сдавлении грудного лимфатического протока и вен средостения опухолью, увеличенными лимфатическими узлами или при механическом повреждении протока во время операций на пищеводе, легком, аорте, а также при травмах грудной клетки.
Заболевание, как правило, развивается остро. В плевральной полости быстро накапливается значительное количество лимфы, происходит сдавление легкого (компрессионный ателектаз) и развивается одышка, в пораженной половине грудной клетки появляется ощущение тяжести. Результаты физикального и рентгенологического исследования позволяют выявить плевральный выпот, характер которого распознают с помощью анализа результатов торакоцентеза.
Хилезный выпот представляет собой мутную беловатую непрозрачную жидкость без запаха, напоминающую по виду молоко вследствие большого содержания жира. При биохимическом анализе в плевральном содержимом определяют большое количество нейтрального жира (триглицеридов), жирных кислот и хиломикронов. Концентрация триглицеридов превышает 1,1 г/л.
При длительном существовании хилоторакса и частых плевральных пункциях больной теряет с лимфой большое количество белка, жиров, клеток крови, электролитов, в связи с чем постепенно нарастает слабость, уменьшается работоспособность, снижается масса тела, развиваются интеркуррентные инфекции.
Хилусоподобный плевральный выпот
Хилусоподобный плевральный выпот по виду напоминает таковой при «истинном» хилотораксе. Это мутная непрозрачная беловатая жидкость с высоким содержанием липидов. Однако в отличие от хилоторакса, в хилусоподобном выпоте содержится большое количество холестерина, тогда как концентрация триглицеридов — ниже 1,1 г/л, а хиломикроны не обнаруживаются вообще.
Таким образом, хилусоподобный плевральный выпот (также как и хилезный) содержит сравнительно большое количество жира, который и придает плевральной жидкости своеобразный внешний вид. Однако, в отличие от хилезного выпота, жир появляется в плевральном содержимом не за счет примеси лимфы и повреждения грудного лимфатического протока, а благодаря распаду клеток, претерпевающих жировое перерождение, что чаще наблюдается при хроническом воспалении серозных оболочек и длительном (не менее 3-5 лет) нахождении в плевральной полости экссудата (Н.С. Тюхтин). Такая ситуация может возникнуть (правда, достаточно редко) при туберкулезе или ревматоидном артрите.
Интересно, что при добавлении к хилусоподобной плевральной жидкости 1-2 мл этилового эфира плевральная жидкость становится прозрачной, тогда как при «истинном» хилезном выпоте она остается мутной.
Лечение
Лечение больных с плевральным выпотом должно быть комплексным и включать медикаментозные и немедикаментозные воздействия как на причину болезни, так и на основные звенья патогенеза и механизмы, определяющие ее клинические проявления. Результаты лечения во многом зависят от полноты диагностического поиска и правильного и адекватного соотношения общих и местных воздействий на патологический процесс.
Лечение плевральных выпотов, осложняющих течение самых разнообразных заболеваний внутренних органов, прежде всего, должно предусматривать адекватные терапевтические воздействия на основное заболевание (этиологическое лечение). Так, при плевральных выпотах невоспалительной природы (транссудатов) этиологическое лечение направлено, прежде всего, на восстановление сердечной деятельности, функции печени, почек, щитовидной железы или коррекцию нарушений коллоидно-осмотического давления крови и т.п. У больных с воспалительными (асептическими) плевритами неинфекционной природы необходимо адекватное лечение аллергических, аутоиммунных и других патологических процессов, лежащих в основе различных клинических проявлений этих заболеваний, в том числе плеврального выпота.
Особое место этиотропная терапия занимает в лечении многочисленных и наиболее распространенных в клинической практике плевритов инфекционного, в первую очередь бактериального, генеза. Ниже приведено описание основных принципов комплексного лечения именно этого вида плеврального выпота па примере ведения больных с парапневмоническим плевритом и эмпиемой плевры. Эти принципы в полной мере могут быть использованы при лечении других воспалительных плевральных выпотов инфекционного генеза.
Этиотропное и патогенетическое лечение
Антибактериальная терапия
Антибактериальная терапия больных с парапневмотическим плевритом назначается с учетом выявленного возбудителя и его чувствительности к антибиотикам. Однако в реальной клинической практике лечение часто приходится начинать с эмпирического назначения антибиотиков. При этом следует учитывать возможный спектр микроорганизмов — наиболее вероятных возбудителей заболевания в данном конкретном случае и клинико-эпидемиологические условия его возникновения (внебольничная, нозокомиальная, аспирационная пневмония, пневмония у больных, находящихся па ИВЛ и т.п.).
Выше было показано, что в настоящее время наиболее частыми возбудителями парапневмонических плевритов, в том числе эмпиемы плевры, являются:
- аэробные грамположительные { Staphylococcus aureus , Streptococcus pyogenes и др.) и грамотрицательные { Klebsiella spp ., Escherichia coli , Haemophilus influencae , Pseudo monas aeruginosa и др.) бактерии;
- анаэробные бактерии {Prevotella spp., Fusobacterium nucleatum, Bactenoides spp., Streptococcus intermedius и др.).
Частой причиной возникновения парапневмонических плевритов являются полимикробные ассоциации аэробных и анаэробных бактерий, которые путем аспирации попадают из ротовой полости в легочную ткань и оттуда лимфогенным или гематогенным путем — в плевральную полость. Причем все клинико-эпидемиологические факторы, способствующие возникновению микроаспирации (остаточные явления нарушения мозгового кровообращения, алкоголизм, эпилептические припадки, использование ИВЛ, наличие у больных сопутствующих бронхоэктазов, инфаркта легкого, обструкции дыхательных путей опухолью или инородным телом, дисфагии и т.п.), увеличивают риск полимикробных ассоциаций или инфицирования анаэробами.
В последние годы показаны существенные преимущества клиндамицина в лечении гнойных заболеваний органов дыхания (абсцесса легкого и эмпиемы плевры) по сравнению с пенициллинами. Клиндамицин, являющийся хлорпроизводным линкомиципа, рекомендуют для лечения анаэробных инфекций различной тяжести, вызванных бактероидами и другой неспоробразующей и клостридиалыюй флорой, а также смешанных {аэробно-анаэробных) инфекций. Кроме того, клиндамицин активен в отношении грамположительных стафилококков и стрептококков, за исключением энтерококков.
В тяжелых случаях клиндамицин назначается в комбинации с метронидазолом, также проявляющем высокую активность в отношении анаэробных грамположительных и грамотрицательных бактерий. Комбинация «клиндамицин + метропидазол» считается «золотым стандартом» лечения тяжелой анаэробной инфекции (10.Б.Белоусов, СМ. Шатунов).
Высокой активностью против анаэробов обладают также:
- имипенем;
- хлорамфеникол;
- бета-лактамы в комбинации с ингибиторами бета-лактамаз.
При возникновении экссудативного плеврита на фоне нозокомиальной пневмонии следует использовать антибактериальные препараты, обладающие расширенным спектром действия, в том числе влиянием на грамотрицательные бактерии и стафилококки. Так, грамотрицательные бактерии чувствительны к ряду антибиотиков, в том числе к имипенему, цефалоспоринам II и III поколения и бета-лактамам в комбинации с ингибиторами бета-лактамаз. Хорошей активностью против метициллин-чувствительных стафилококков обладают клиндамицин, синтетические пенициллины и цефалоспорины.
В большинстве случаев эмпирическую антибактериальную терапию больных с парапневмоническим плевритом начинают с назначения следующих препаратов или их комбинаций:
- клиндамицин + цефалоспорины III поколения;
- бета-лактамы + ингибиторы бета-лактамаз;
- имипенем.
После получения результатов выделения возбудителя и определения его чувствительности к антибиотикам проводится коррекция терапии.
Следует также помнить, что аминогликозиды обычно не назначают больным с экссудативиым плевритом, поскольку препараты этой группы антибиотиков плохо проникают в плевральную полость.
Дезинтоксикационная терапия
Дезинтоксикационная терапия, как правило, в сочетании с форсированным диурезом в той или иной степени показана всем больным с эмпиемой плевры и осложненным экссудативным плевритом. Терапия направлена на выведение из организма токсических веществ, улучшение реологических свойств крови и микроциркуляции, коррекции нарушений белкового обмена и устранение нередко возникающей при этой патологии гиповолемии.
С этой целью больным показаны внутривенные капельные инфузии изотопических растворов солей, 5-10% раствора глюкозы, а также низкомолекулярных растворов (гемодеза, неокомпенсана, реополиглюкина и др.). Форсированный диурез обеспечивается внутривенным введением 20-40 мг лазикса или других салуретиков и мочегонных.
Коррекция нарушений белкового обмена
С целью коррекции нарушений белкового обмена больным назначают полноценное питание с повышенным содержанием белка. В тяжелых случаях внутривенно несколько раз вводят 150 мл 10% раствора альбумина, 200-400 мл нативной плазмы, а также анаболические гормоны (ретаболил 1 раз в 10-14 дней).
Повышение общей резистентности организма
Важным компонентом лечения больных экссудативным плевритом и эмпиемой плевры является применение веществ, повышающих общую резистентность организма. С этой целью используют:
- средства экстракорпоральной детоксикации (ультрафиолетовое и лазерное облучение крови, гемосорбция, плазмаферез);
- внутримышечное введение поливалентного иммуноглобулина человека по 2,0 мл через 1-3 дня (всего 3-5 инъекций);
- при значительной недостаточности антителообразования — внутривенно или внутримышечно у-глобулип по 1,2-1,8 мг/кг массы тела (1 раз в месяц);
- внутривенные инфузии гипериммунной плазмы и бактериофагов (антистафилококковая плазма, антисинегнойная плазма, плазма с повышенным содержанием антител к протею и др.) по 200-250 мл 2-3 раза с интервалом в 3 дня;
- способы активной иммунизации, например введение стафилококкового анатоксина (3 инъекции по 0,5-1,0 анатоксина с интервалом в 2-3 дня);
- стимуляция Т-системы и неспецифических защитных сил организма (левамизол, тимизол, иммунал и др.).
Противовоспалительное и гипосенсибилизирующее лечение
В ряде случаев дополнительное применение гипосенсибилизирующих и противовоспалительных средств способствует уменьшению местного воспалительного процесса в плевре, коррекции повышенной проницаемости сосудов, уменьшению сенсибилизации плевры и устранению гиперергической реакции листков плевры на воздействие возбудителя заболевания.
С этой целью используют современные НПВП (вольтарен, диклофенак, мовалис, пайс), а в ряде случаев, особенно при наличии «бурной» гиперергической реакции плевры, — глюкокортикостероиды (преднизолон, метипред и др.) в дозе 30-40 мг в сутки (коротким курсом). При этом следует помнить, что гормоны при экссудативных плевритах всегда следует назначать с большой осторожностью и «под защитой» антибактериальных средств.
Местное лечение
9-09-2015, 00:14
