Стосовно змін в м’язовій оболонці, в преатретичних сегментах кишок спостерігали значну гіпертрофію циркулярного м’язового шару у порівнянні з поздовжнім (товщина 351,4 мкм проти 40,2 мкм в нормі), гіперплазію гладеньких міоцитів, ділянки фіброзу зі значною кількістю елементів фібробластичного ряду сполучної тканини, ділянки поліморфноядерної лейкоцитарної інфільтрації за ходом кровоносних судин та у прошарках сполучної тканини між шарами м’язової оболонки. Разом із значною гіпертрофією спостерігається розшарування м’язової оболонки, її набряк. Часто виявляються ділянки роз’єднання м’язових шарів на окремі м’язові клітини внаслідок значного набряку. Таким чином, гістологічні та гістохімічні зміни в стінці преатретичного сегмента кишки свідчать про його високе функціональне навантаження та декомпенсаторні зміни. До декомпенсаторних проявів, поряд зі змінами в слизовій оболонці, слід віднести також і значну гіпертрофію м’язових елементів, що охоплює як м’язову пластинку слизової оболонки, так і м’язову оболонку кишки, а також функціональне перевантаження кровоносних судин.
В преатретичних сегментах тонкої кишки спостерігаються значні зміни з боку нервових клітин та їх відростків. Як компенсаторна реакція на гіпертрофію м’язової оболонки кишки розвиваються явища гіперфункції нейроцитів, що часто носить ознаки декомпенсації. На цьому фоні виявляється зниження активності АТФ-ази та кислої фосфатази в нейроцитах стінки кишки, як наслідок декомпенсованої гіпертрофії, що призводить до нестачі енергетичних субстратів. Морфологічними субстратами, що характеризують стан гіперфункції нервових елементів, є збільшення та зміна форми нейроцитів, потовщення їх відростків та їх варикозитет, значні потовщення на кінцях дендритів, нерівномірне сприйняття солей срібла тілом нейроцита та його відростками.
В преатретичних сегментах клубової кишки число нервових волокон, що мають ознаки подразнення, дещо менше. Це, можливо, пояснюється реституцією раніше змінених нервових волокон, яка, зокрема, проявляється їх дегідратацією. Нервові волокна, що не зазнали розпаду, лише зрідка мають залишкові явища дисхромії та місцевого набряку.
Морфометричне дослідження нервових елементів преатретичного сегмента кишки показує збільшення як мінімального та максимального, так і середнього розміру нейронів (мінімальний розмір – 44,35±6,78 мкм проти 42,34±5,56 мкм в нормі, максимальний розмір – 76,32±16,67 мкм проти 60,36±11,24 мкм в нормі). Для стану реактивного подразнення в умовах декомпенсованої гіперфункції це природньо. На це вказує і збільшені розміри та площа гангліїв, хоча і не такою значною мірою (розмір ганглія 857,34±78,29 мкм проти 755,67±98,36 в нормі, площа ганглія 15318,92±688,22 мкм2 проти 12342,23±559,63 мкм2 в нормі). Відповідно, зростає і відсоток дегенеративних форм нейронів (30,2% проти 10,1% в нормі). Але ці зміни є вторинними, зумовленими гіпертрофією преатретичного сегмента та реакцією нейронів на гіперфункцію кишки. За даних умов ця гіперфункція є декомпенсованою, на що вказує і відсоток дегенеративних форм нейронів. За умов гіперфункції збільшуються також розміри та площа гангліїв.
В сегментах тонкої кишки, що зазнала атрезії, були виявлені суттєві зміни в гемомікроциркуляторному руслі, що забезпечують живлення стінки кишки, та, особливо, в її інтрамуральних нервових сплетеннях. Діаметри більшості інтрамуральних артеріол звужені до 20 мкм, а деяких до 16 мкм. Контури їх звивисті. Капілярні петлі гангліїв, в основному, правильної форми, але деякі з них мають незначну звивистість контурів. У звивистих клубочках гангліїв посткапіляри та венули розширені (діаметр останніх сягає 23-25 мкм, капілярні петлі дещо деформовані). Судинний рисунок на фоні нервових вузлів підсилений. При цьому ємність кровоносних судин на одиницю площі нервових сплетень складала 6120000 мкм3 (при р<0,001) та в розрахунку на одиницю гангліонарної клітини (7320 мкм3 при р<0,001). Капіляри, що йдуть вздовж нервових волокон та гангліїв, розширені, звивисті. Артеріоли стають ширше 30 мкм, деякі гілочки нерівномірно звивисті. Венули розширені до 30-60 мкм, деякі з них звивисті, що особливо характерно для анастомозуючих, причому, чим ближче до нервових вузлів, тим це більш помітно. Кількість артеріоловенулярних анастомозів зростає. Різко розширюються та стають звивистими співустя між окремими венозними гілочками.
У судинному сплетенні гангліїв венозні, капілярні та венулярні стовбури розширені та звивисті, часто з колбоподібним здуттям стінок. Ємність кровоносних судин гангліїв збільшується майже в 2 рази – 7012000 мкм3 при р<0,001 на одиницю площі ганглія та 8440 мкм3 при р<0,001 в розрахунку на одну гангліонарну клітину.
Таким чином, компенсаторні механізми, що розвиваються в стінці преатретичного сегмента кишки, стосуються відносного збільшення ємності кровоносного русла нервових вузлів стінки кишки взагалі за рахунок розширення судин, головними чином, венозної ланки та капілярів. Циркуляторна гіпоксія зумовлює кисневе голодування тканин та венозний застій, а утруднення венозного відтоку, в свою чергу, викликає розширення капілярів. В даному випадку внаслідок компенсаторної гіпертрофії спостерігаються різні зміни нервового апарату, які, в свою чергу, здійснюють вплив на гемодинаміку в стінці кишки.
Постатретичні сегменти тонкої кишки характеризується множинними дистрофічними змінами в усіх оболонках стінки кишки. В слизовій оболонці спостерігається виражена деструкція ворсинок та десквамація епітелію їх верхівок. У власній пластинці слизової оболонки часто спостерігається поліморфноядерна лейкоцитарна інфільтрація, більш виражена в області ворсинок. Крипти слизової оболонки мають нерівномірний вузький простір.
Постатретичні сегменти клубової кишки характеризуються такими патологічними змінами: слизова оболонка з підслизовою основою в стані набряку, в деяких ділянках відшарована. Наявні множинні ділянки десквамації епітелію. М’язова оболонка потоншена, спостерігається зменшення розмірів міоцитів при збільшенні їх кількості, що є ознакою патологічної гіперплазії м’язової оболонки. Досліджувані патологічні прояви у постатретичному сегменті свідчать про функціональну ненавантаженість його, адже гіперплазія міоцитів не супроводжується збільшенням їх розмірів, наявний лише поділ.
Постатретичні сегменти ободової кишки характеризуються менш вираженими змінами анатомічної будови. Вони менше зазнають функціональної навантаженості. Ворсинки слизової оболонки в деяких ділянках збережені, вони короткі, ущільнені, реактивні зміни слизової оболонки виражені менше та носять більш різноманітний характер.
У стінках кровоносних судин постатретичного сегмента відмічається зниження активності АТФ-ази, кислої та лужної фосфатаз, що може бути пов’язане з дистрофічними змінами постатретичного сегмента внаслідок функціональної ненавантаженості. Хоча фосфатазна активність в стінках кровоносних судин нерівномірна, в основному, вона знижена, як відносно групи порівняння, так і, звичайно, в порівнянні з такими змінами в преатретичних сегментах. Таким чином, в морфофункціональному дослідженні добре виявляють ознаки функціональної ненавантаженості постатретичних сегментів. І хоча дистрофічні прояви в даному випадку менш виражені, ніж в преатретичних сегментах, викликає сумнів функціональна придатність даних сегментів.
У постатретичних сегментах при обробці зрізів методом імпрегнації нітратом срібла за Більшовським-Грос спостерігаються нейроцити з вираженою деформацією тіла та утворенням множинних відростків. Комплекс морфологічних змін в нейроцитах інтрамурального нервового сплетення постатретичного сегмента тонкої кишки, описаний в даному дослідженні, є не тільки ознакою функціональної ненавантаженості нервових елементів даної ділянки кишки, але й проявом дегенеративних змін нейроцитів в умовах їх функціональної ненавантаженості. Особливо ці зміни виражені в постатретичних сегментах дванадцятипалої кишки. Крім того, спостерігаються ознаки хронічного подразнення нейроцитів. Можлива причина хронічного подразнення – деструктивні зміни в нефункціонуючих належним чином тканинах. Ознаками хронічного подразнення в даному випадку є: гідропія та вакуолізація цитоплазми, різні ступені тигролізу, а також двоядерцевість нейроцитів.
Велика кількість нейроцитів мають ознаки дегенерації. Ядра в цих клітинах можуть бути розташовані по периферії. Відростки деяких нервових клітин, особливо великого розміру, часто потовщені. В інтрацелюлярному просторі нервових сплетень виявляються звивисті нервові волокна у стані дегенерації. В постатретичних сегментах ободової кишки спостерігаються менш виражені дегенеративні зміни. Вміст РНК в нейроцитах зменшений у порівнянні з нормою. Вивчення РНК в нейроцитах інтрамурального нервового сплетення постатретичного сегмента ободової кишки вказує, що деяка частина нейроцитів знаходиться на межі функціонального виснаження, проте деякі нейроцити виходять від цієї крайньої межі функціонального виснаження. Це свідчить про значні компенсаторні можливості інтрамуральних нервових клітин, а також про вторинність змін нервових елементів в даних сегментах кишки. Проте в деяких нейроцитах все ж таки спостерігаються реактивні зміни.
Постатретичні сегменти дванадцятипалої кишки характеризуються такими патологічними змінами гемомікроциркуляторного русла: артеріальні та венозні стовбури першого та другого порядків за діаметром не відрізняються від таких у нормі, хід їх в основному прямолінійний. Судинна мережа гангліїв дещо збіднена. По напрямку до середини сегмента ці зміни згладжуються. Ємність кровоносних судин вузлів складає 4550000 мкм3 при р<0,001, а в розрахунку на одну клітину 5800 мкм3 при р<0,001. На препаратах, імпрегнованих за Більшовським-Грос, багато нейроцитів гіперімпрегновані, їх ядра погано контуруються. Не у всіх клітин чітко виявляються відростки. Зустрічаються молоді форми клітин, зменшені в розмірах, округлої форми, з маленьким ядром без відростків. Збільшується кількість клітин-сателітів. В постатретичних сегментах порожньої кишки спостерігалися ознаки функціональної ненавантаженості гемо-мікроциркуляторного русла. Перигангліонарна судинна мережа складається з капілярів, діаметр яких коливається від 6 до 10 мкм. Вони мають невелику звивистість та утворюють навколо клітин дуги, петлі або кільця.
В стінці постатретичного сегмента ободової кишки відбуваються незначні зміни у порівнянні з нормою. Помітна гіпотрофія гладеньких міоцитів з потоншенням залозистого апарату. Частина капілярів, як і в нормі, лежить у межах 5-10 мкм від нейроцита. Судинна мережа гангліїв складається з капілярів, діаметр яких коливається від 6 до 10 мкм. Зрідка ганглії оточені розширеними та сильно звивистими капілярами. Більшість капілярів, як і в нормі, розташовується на відстані 5-10 мкм від нейроцита. Ємність кровоносних судин, як правило, нижче норми, але зустрічаються нервові вузли з підвищеною васкуляризацією. Нейроцити тут мають виражені ознаки деструкції. Показники сумарного діаметра судин ганглія загалом наближаються до норми або понижені. Всі ці зміни в нервовому апараті та гемомікроциркуляторному руслі постатретичного сегмента свідчать про дистрофічні структурні зміни навіть у цій функціонально ненавантаженій ділянці.
Дослідження ділянок кишкових анастомозів у випадках їх неспроможності при хірургічному лікуванні кишкових атрезій показує важливе практичне значення морфологічного дослідження атрезій кишечника. Виявлені дані свідчать про функціональну неповноцінність кишки на рівні накладання анастомозу. Тому було застосовано метод оцінки функціональної придатності кишки до накладання анастомозу залежно від патогенетичних типів атрезій кишки. Основою запропонованої методики стали критерії класифікації атрезій кишки, розроблені за патогенетичним принципом на основі проведеного морфофункціонального дослідження. За даними критеріями можна виявити такі основні патогенетичні типи атрезій кишки, взаємозв’язані з формами загальноприйнятої класифікації за макроморфологічними ознаками:
1. Патогенетичний тип атрезій кишки з первинними порушеннями розвитку кишкового епітелію. Цей тип відповідає мембранозній формі атрезії, яка найчастіше вражає дванадцятипалу кишку.
2. Патогенетичний тип атрезій кишки з первинними порушеннями розвитку судин брижі. Цей тип відповідає двом формам атрезії: атрезії з фіброзними тяжами та повній формі атрезії, які вражають як тонку, так і товсту, зокрема ободову, кишку.
3. Патогенетичний тип атрезій кишки з первинними порушеннями повороту кишкової трубки. Цей тип відповідає множинним формам атрезії зокрема, синдромові “пагоди”, що вражає практично весь кишечник.
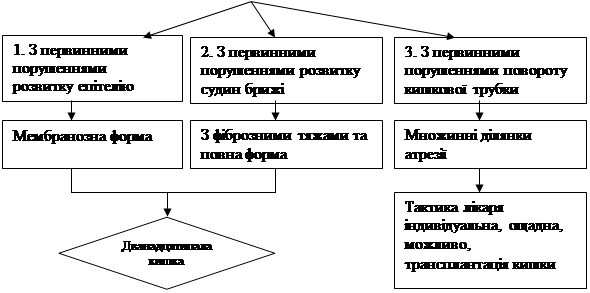
Виходячи з даних дослідження, розроблено критерії нової класифікації атрезій кишки за патогенетичним принципом. Відповідно до класифікації рекомендована диференційована лікарська тактика при різних типах атрезій (рис. 1).
1. Патогенетичний тип з первинними порушеннями розвитку епітелію. Так як цей тип відповідає мембранозній формі атрезії, що найчастіше вражає дванадцятипалу кишку, зважаючи на досвід хірургічного лікування цієї форми атрезії та необхідність економної резекції дванадцятипалої кишки, рекомендується:
а) при локалізації ураження в дванадцятипалій кишці необхідна економна резекція, зважаючи на розмір та анатомічне положення цього органу. Тому резекції підлягають лише пре- та постатретичний сегменти з ділянкою атрезії;
б) при локалізації першого патогенетичного типу (що відповідає мембранозній формі атрезії) в порожній, клубовій або ж ободовій кишках рекомендовано тактику, як при наступному патогенетичному типі.
2. Патогенетичний тип з первинними порушеннями розвитку кровоносних судин брижі відповідає атрезії з фіброзними тяжами та повній формі атрезії із судинною ланкою в патогенезі. Для цих форм застосоване вивчення морфофункціонального стану кишки на різних рівнях візуально незміненої ділянки (межі пре- та постатретичного сегментів). Виявлено, що лише на рівні найближчої до анастомозу порожньокишкової або клубовокишкової артерії стінка кишки має нормальну гістологічну будову у всіх зразках. Тому рівень резекції з приводу атрезій кишки у новонароджених має відповідати рівню найближчих до преатретичного та постатретичного сегментів порожньокишкових або клубовокишкових артерій. Якщо атрезія даного типу вражає дванадцятипалу кишку, рекомендується діяти так, як при мембранозній формі атрезії органа, тобто економну резекцію пре- та постатретичного сегментів, беручи до уваги розмір та анатомічне положення дванадцятипалої кишки.
3. При патогенетичному типові атрезій кишки з первинними порушеннями розвитку повороту кишкової трубки, що відповідає множинним ділянкам атрезії і зустрічається у вигляді, в основному, синдрому “пагоди”, лікарська тактика має бути індивідуальною. З одного боку, необхідно видалити всі патологічно змінені ділянки кишки; з іншого, значний обсяг резекції може призвести до так званого синдрому “короткої кишки”, що супроводжується значними функціональними порушеннями (“кишкова недостатність”). Тому рекомендовано діяти відповідно до обсягу та ступеня ураження кишки. Можливою операцією вибору в перспективі має стати трансплантація кишки.
|
||
 |
||
![]()
![]()
![]()
![]() Так Ні
Так Ні
|
|
|
Рис. 1. Орієнтовний алгоритм дій лікаря при кишкових атрезіях.
Таким чином, дане дослідження відрізняється від відомих тим, що характеризує зміни анатомічної будови та функціонального стану кишки на основі їх комплексної оцінки. Найсуттєвішими результатами дослідження є розроблені критерії класифікації атрезій кишки за патогенетичним принципом. Пріоритет даного дослідження полягає в тому, що воно має важливі для клінічної практики результати – розроблений метод оцінки придатності кишки до анастомозування при лікуванні кишкових атрезій.
ВИСНОВКИ
1. У дисертації наведене теоретичне узагальнення і нове вирішення конкретної наукової задачі, що виявляється в характеристиці будови та функціонального стану кишки при атрезіях у новонароджених на основі комплексної оцінки змін будови кишки з використанням макро- та мікроскопічних, гістохімічних, морфометричних та статистичних методів дослідження, а також розроблено критерії класифікації кишкових атрезій за патогенетичним принципом.
2. Зміни анатомічної будови кишки при атрезіях локалізуються не тільки в ділянці атрезії, але й охоплюють суміжні сегменти кишки – преатретичний (проксимальний) та постатретичний (дистальний). Ступінь змін будови кишки залежить також від відділу кишечника, де локалізована атрезія.
3. Дистрофічні зміни будови найбільше виражені в ділянці атрезії та преатретичному сегменті кишки, менше виражені в постатретичному сегменті.
4. Для кишкових атрезій властивий краніокаудальний градієнт ступеня анатомічних змін, тобто чим вищий рівень ураження кишечника, тим істотніші зміни анатомічної будови кишки.
5. В ділянці атрезії спостерігаються такі дистрофічні зміни: множинні вогнища фіброзу та некрозу, розшарування оболонок кишки, десквамація епітелію слизової оболонки, розширення судин підслизової основи з множинними екстравазатами, вторинні явища запального характеру, зниження функціональної активності нейроцитів міжм’язового сплетення, фрагментація та дисхромія нервових волокон, значне порушення нейровазальних взаємовідношень, явища вторинного ангіогенезу, що свідчить про поєднання первинних порушень ангіогенезу та вторинних дистрофічних змін всіх елементів кишкової стінки.
6. Виснаження компенсаторних механізмів у преатретичному сегменті кишки полягає в декомпенсованій гіпертрофії м’язової оболонки, особливо циркулярного м’язового шару (351,4 мкм проти 40,2 мкм в нормі), потоншанні слизової оболонки кишки (256,2 мкм проти 510,7 мкм в нормі), десквамації її епітелію, гіперфункції нейроцитів міжм’язового нервового сплетення, гіпертрофії та гіперхромії нервових волокон, підсилення кровопостачання нервових апаратів стінки кишки (ємність кровоносних судин в розрахунку на одну гангліонарну клітину 7320 мкм3 проти 4500 мкм3 в нормі), ознаках вторинного ангіогенезу.
7. Дистрофічні зміни у постатретичному сегменті полягають в потоншанні слизової оболонки кишки, атрофії м’язової оболонки, дегенерації нейроцитів нервових сплетень та зменшенні кровопостачання гангліїв, що є наслідком функціональної ненавантаженості даного сегмента.
8. Істотне порушення анатомічної будови кровоносних судин кишки в ділянці атрезії з поширенням на преатретичний сегмент, дезінтеграція нейросудинних взаємовідношень в ділянці атрезії, наявність вторинного ангіогенезу та дегенеративних змін в нейронах свідчать про первинне виникнення порушень ангіогенезу при кишкових атрезіях.
9. На основі отриманих даних розроблено критерії класифікації атрезій кишки за патогенетичним принципом, що передбачає три основні шляхи патогенезу атрезій кишки: 1) з первинними порушеннями розвитку епітелію слизової оболонки кишки, 2) з первинними порушеннями розвитку кровоносних судин кишки та 3) з первинними порушеннями повороту кишкової трубки.
список Публікацій за темою дисертації
У фахових виданнях
1. Єршов В.Ю. Зміни інтрамурального нервового апарату кишки при атрезіях у новонароджених // Вісник наукових досліджень. – 2006. – №3. – С. 24-26.
2. Єршов В.Ю. Оцінка придатності кишки до анастомозування при хірургічному лікуванні атрезій кишки у новонароджених // Клінічна анатомія та оперативна хірургія. – 2007. – №4. – С. 53-58.
3. Єршов В.Ю., Ковальський М.П. Морфометрична характеристика кишки при атрезіях у новонароджених // Науковий вісник Національного медичного університету імені О.О. Богомольця. – 2007. – №4. – С. 40-47.
(Єршов В.Ю. зібрав та проаналізував матеріал, підготував до друку).
4. Ковальський М.П., Даншин Т.І., Єршов В.Ю. Досвід вивчення морфології атрезій кишечнику // Клінічна анатомія та оперативна хірургія. – 2004. – №2. – С. 39-43.
(Єршов В.Ю. зібрав матеріал, провів його аналіз та узагальнення).
Тези доповідей
5. Єршов
8-09-2015, 22:26
