АКАДЕМІЯ МЕДИЧНИХ НАУК УКРАЇНИ
ДЕРЖАВНА УСТАНОВА "ІНСТИТУТ НЕЙРОХІРУРГІЇ ІМЕНІ АКАДЕМІКА А.П.РОМОДАНОВА"
ЧОМОЛЯК ЮРІЙ ЮРІЙОВИЧ
УДК 616.833.15-091.934-003.93-085:615.357.001.4
ЛОКАЛЬНИЙ ВПЛИВ АПЛІКАЦІЇ ПРОГЕСТЕРОНУ НА РЕМІЄЛІНІЗАЦІЮ ЗОНИ ВХОДУ ТРІЙЧАСТОГО НЕРВА В ЕКСПЕРИМЕНТІ
14.01.05 – нейрохірургія
Автореферат дисертації на здобуття наукового ступеня
кандидата медичних наук
Київ – 2008
Дисертацією є рукопис.
Робота виконана в Ужгородському національному університеті Міністерства освіти і науки України.
Науковий керівник – доктор медичних наук, професор Смоланка Володимир Іванович, Ужгородський національний університет, завідувач кафедри неврології, нейрохірургії та психіатрії
Офіційні опоненти: доктор медичних наук, професор Трош Рустем Меметович, ДУ “Інститут нейрохірургії імені академіка А.П.Ромоданова АМН України”, завідувач відділення субтенторіальної нейрохірургії
доктор медичних наук, професор Сон Анатолій Сергійович, Одеський державний медичний університет МОЗ України, завідувач кафедри нейрохірургії і неврології
Захист відбудеться “26” лютого 2008 р. о 12 годині на засіданні Спеціалізованої вченої ради Д 26.557.01 в ДУ “Інститут нейрохірургії імені академіка А.П.Ромоданова АМН України” (04050, м.Київ, вул. Мануїльського, 32).
З дисертацією можна ознайомитись у бібліотеці ДУ “Інститут нейрохірургії імені академіка А.П.Ромоданова АМН України” (04050, м.Київ, вул. Мануїльського, 32).
Автореферат розісланий “25” січня 2008 р.
Вчений секретар Спеціалізованої вченої ради,
доктор медичних наук Л.Л.Чеботарьова
ЗАГАЛЬНА ХАРАКТЕРИСТИКА РОБОТИ
Актуальність теми. Лікування невралгії трійчастого нерва є актуальною медичною проблемою. За даними різних досліджень в країнах Євросоюзу щорічно виявляється від 4 до 27 нових випадків цього захворювання на 100 тис. населення (Manzoni G.C. et al., 2005; Hall G.C. et al., 2006). Виражений больовий синдром у пацієнтів з цим захворюванням, описаний більш ніж 300 років тому (Bausch J.L., 1671), нерідко залишається стійким до сучасних медикаментів. З розвитком мініінвазивних технологій своє місце в лікуванні невралгії трійчастого нерва зайняли хірургічні методи (Цимбалюк В.І. та співавт., 2001). Так, метод вибору хірургічного лікування даного захворювання – мікроваскулярна декомпресія трійчастого нерва – забезпечує відмінні результати протягом першого тижня після втручання у 82% пацієнтів. Проте, через 10 років відсутність больового синдрому без додаткового медикаментозного лікування спостерігається лише у 63,5% оперованих (Barker F.G. II, Jannetta P.J., 1996). Підвищення ефективності хірургічних втручань при невралгії трійчастого нерва можливе завдяки розвитку знань про патогенез цього захворювання.
За допомогою проведених наприкінці ХХ століття досліджень встановлено, що одним з основних чинників розвитку типової невралгії трійчастого нерва є локальна демієлінізація, яка виникає в його корінці під впливом стиснення судиною (Hilton et al., 1994; Love S., Coakham H., 2001; Broggi et al, 2005). Водночас існує припущення, що рідкісні випадки спонтанного видужання пацієнтів з невралгією пов’язані з повноцінною ремієлінізацією трійчастого нерва (Love S., Coakham H., 2001), тоді як недостатнє відновлення мієлінової оболонки розглядається як основна причина рецидивів захворювання після хірургічних втручань (Kitt S. et al., 2000). Відповідно до цього, пошук засобів для повноцінного відновлення мієлінової оболонки нервових волокон є пріоритетним напрямком сучасних досліджень. Рядом авторів доведено, що місцеве застосування прогестерону призводить до посилення ремієлінізації нервових волокон периферичної нервової системи як in vitro, так in vivo (Koenig H. et al., 1995, 2000; Schumacher M. et al., 2001; Ghoumari A. et al., 2005). Виявлено вплив прогестерону на ремієлінізацію також в центральній нервовій системі (Mellon S. et al., 2001).
Вищезазначене обумовлює можливість та доцільність місцевого використання прогестерону під час мікроваскулярної декомпресії трійчастого нерва з метою забезпечення більш повноцінного відновлення мієлінової оболонки корінця трійчастого нерва і, відповідно, покращення результатів хірургічного лікування. Проте переваги такого комбінованого мікрохірургічного лікування можуть бути оцінені з достатнім ступенем вірогідності лише в умовах експерименту на лабораторних тваринах. Отже, необхідним є експериментальне обґрунтування вказаного нейрохірургічного втручання з аплікацією прогестерону та використанням мікрохірургічної техніки.
Зв’язок роботи з науковими темами і програмами. Дисертаційне дослідження пов’язане з темою науково-дослідної роботи кафедри неврології, нейрохірургії та психіатрії медичного факультету Ужгородського національного університету в 2005-2007 рр. і є фрагментом теми: “Вторинна профілактика і прогнозування інсультів та судинних компресійних синдромів, спричинених церебральним атеросклерозом”, номер держреєстрації 0104U010447.
Мета і завдання дослідження. Метою роботи є посилення ремієлінізації корінця трійчастого нерва шляхом аплікації прогестерону в хронічному експерименті задля вдосконалення мікрохірургічного втручання при невралгії трійчастого нерва.
Для досягнення мети поставлено такі завдання:
1. Розробити експериментальну модель сегментарної демієлінізації корінця трійчастого нерва.
2. На моделі сегментарної демієлінізації трійчастого нерва провести серії експериментальних досліджень аплікації прогестерону з використанням мікрохірургічної техніки та наступним морфологічним дослідженням процесу ремієлінізації зони входу корінця трійчастого нерва.
3. Встановити оптимальний варіант місцевого застосування прогестерону з метою посилення ремієлінізації зони входу трійчастого нерва в експерименті.
Об’єкт дослідження – процеси демієлінізації та ремієлінізації корінця трійчастого нерва.
Предмет дослідження – особливості ремієлінізації зони входу корінця трійчастого нерва в експерименті з використанням комбінованого мікрохірургічного втручання.
Методи дослідження. Для реалізації мети та завдань роботи проведено наступні дослідження:
1. Хронічний експеримент – змодельовано фокальну демієлінізацію та ремієлінізацію корінця трійчастого нерва морської свинки.
2. Морфологічні – досліджено гістологічні особливості де- та ремієлінізації зони входу корінця трійчастого нерву в експерименті.
3. Гістохімічні – визначено рецептори до КІ-67 у клітин Шванна корінця трійчастого нерва в експерименті.
4. Статистичні – виконано математичну обробку результатів.
Наукова новизна одержаних результатів. Уперше розроблено доступ до корінця трійчастого нерва морської свинки з використанням мікрохірургічної техніки.
Вперше встановлено, що застосування 0,1% розчину броміду етидію вірогідно відтворює локальну дегенерацію мієлінової оболонки корінця трійчастого нерва у морської свинки із збереженням цілісності аксонів.
Вперше розроблено експериментальну модель локальної сегментарної демієлінізації корінця трійчастого нерва морської свинки з використанням розробленого доступу до трійчастого нерва та 0,1% розчину броміду етидію.
Вперше експериментально відтворено процес відновлення мієлінової оболонки корінця трійчастого нерва після його сегментарної демієлінізації.
З’ясовано вплив різних чинників на ремієлінізацію корінця трійчастого нерва лабораторних тварин та вперше встановлено, що аплікація 2,5% розчину прогестерону на демієлінізовану ділянку покращує відновлення мієлінової оболонки.
Практичне значення отриманих результатів. Практична цінність отриманих результатів полягає у методологічному обґрунтуванні запланованого хронічного експерименту.
Розроблена модель сегментарної демієлінізації є необхідною для дослідження цього процесу в корінці трійчастого нерва, а також для визначення можливостей посилення ремієлінізації даної частини нервової системи.
Експериментально підтверджено стимулюючий вплив аплікації 2,5% розчину прогестерону на ремієлінізацію трійчастого нерва, що обґрунтовує подальші клінічні дослідження місцевого застосування прогестерону під час хірургічних втручань у хворих з невралгією трійчастого нерва.
Особистий внесок здобувача. Дисертація є самостійним науковим дослідженням автора. Дисертанту належить його ідея, він самостійно провів інформаційно-патентний пошук і аналіз літератури, організував наукове дослідження, разом з науковим керівником професором Смоланкою В.І. сформулював мету, завдання та план дисертаційної роботи. Автором самостійно розроблено модель сегментарної демієлінізації корінця трійчастого нерва, самостійно виконано експериментальну частину роботи, спільно з завідувачем відділу патоморфології ДУ "Інститут нейрохірургії імені академіка А.П.Ромоданова АМН України", д.мед.н., професором М.І. Шамаєвим та старшим науковим співробітником цього відділу, к.мед.н. Т.А.Малишевою здійснено морфологічні та імуногістохімічні дослідження. Дисертант особисто провів статистичну обробку отриманих результатів, разом з науковим керівником піддав аналізу результати дослідження, сформулював висновки. Автор самостійно оформив дисертаційну роботу.
Апробація результатів дисертації. Основні положення дисертації були представлені на конференції нейрохірургів України "Нові технології в нейрохірургії" (Ужгород, 2006), науково-практичній конференції неврологів України (Харків, 2007), спільному засіданні Закарпатського осередку Асоціації нейрохірургів України та обласного товариства неврологів (Хуст, 2007). Дисертація пройшла апробацію на розширеному засіданні Вченої ради ДУ "Інститут нейрохірургії ім. акад. А.П. Ромоданова АМН України" сумісно з кафедрами нейрохірургії Національної медичної академії післядипломної освіти ім. П.Л. Шупика МОЗ України та Національного медичного університету ім. О.О.Богомольця МОЗ України, членами Української асоціації нейрохірургів 13 липня 2007 року.
Публікації. Результати дисертаційної роботи представлені у 6 публікаціях, з них дві статті у фахових наукових журналах, один патент України (2007 р.), дві статті у фахових виданнях, що містять огляд літератури та власні спостереження, одні тези доповіді на конференції нейрохірургів України, один позитивний висновок на патент України (2007 р.).
Обсяг і структура дисертації. Дисертація складається зі вступу, чотирьох розділів, висновків, списку використаних джерел. Загальний обсяг дисертаційної роботи становить 136 сторінок, з яких 120 сторінок тексту, а також 51 ілюстрація та 6 таблиць, які займають менше однієї сторінки. Список використаних джерел нараховує 152 найменування.
ОСНОВНИЙ ЗМІСТ ДИСЕРТАЦІЇ
Дизайн дослідження. Дослідження ремієлінізації зони входу корінця трійчастого нерва проведено у вигляді експерименту, який складався із двох етапів (рис.1).
На першому етапі розроблено експериментальну модель сегментарної токсичної демієлінізації корінця трійчастого нерва – особливої форми дегенерації мієлінової оболонки, яка характерна для пацієнтів з невралгією – з підтвердженням цього процесу на світлооптичному та електронномікроскопічному рівнях. Крім того, модель дозволяла якнайкраще оцінити вплив прогестерону на процес ремієлінізації. Відомо, що перші ознаки демієлінізації при місцевому застосуванні броміду етидію виявляються на 7 добу після введення цього гліотоксину з максимально вираженими змінами на 14 добу. В цей строк під час морфологічних досліджень вже виявляють ознаки початкової ремієлінізації у вигляді поодиноких клітин Шванна поміж аксонів, оточених базальною мембраною та колагеновими волокнами (Woodruff R., Franklin J., 1999; Riet-Correa G., 2002). Вплив прогестерону на ремієлінізацію найбільш ефективний саме в цей період, оскільки відомо, що його дія спрямована на стимуляцію вже існуючої ремієлінізації, а не на ініціалізацію цього процесу (Koenig H.L. et al., 1995).
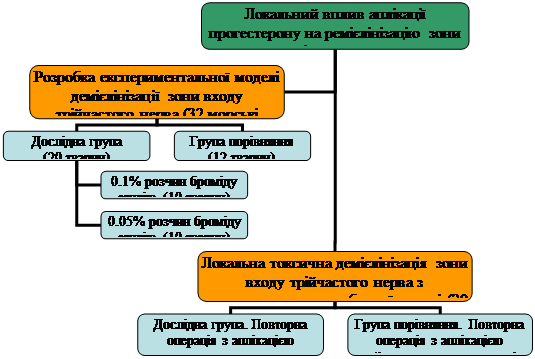
Рис. 1. Дизайн дослідження.
Другий етап був присвячений дослідженню впливу прогестерону на відновлення мієлінової оболонки після експериментальної демієлінізації. Розроблена експериментальна модель дозволила застосувати розчин прогестерону в момент початкової ремієлінізації, тобто на 14 добу після введення розчину броміду етидію. Протягом 15 наступних діб лабораторні тварини знаходились під спостереженням у звичному для них середовищі. На 29 добу після початку експерименту морські свинки обох груп були виведені з експерименту, препарати їх трійчастих нервів досліджені за допомогою світлової та електронної мікроскопії. Отримані результати порівняно з даними імуногістохімічних досліджень у цих групах.
Статистична обробка результатів. Відповідно до кількості вибірок (дві групи морських свинок) та характеру даних всередині груп (кількісні та якісні ознаки з нормальним розподілом варіант) оптимальними способами статистичної обробки результатів нашого дослідження були: один з варіантів t-критерію Стьюдента та критерій ч2 Пірсона. Враховуючи те, що значення частот виявлення якісних показників інколи були менше 5, а кількість спостережень – 20, замість критерію ч2 Пірсона було використано точний критерій Фішера-Ірвіна (Бабич П.Н. та ін, 2004). Вказані обчислення виконувались за допомогою статистичних комп’ютерних програм. Статистична обробка частини морфометричних даних проводилась з використанням пакета стандартних ліцензійних програм до програмно-апаратного комплексу “Leica Microsystems CMS GmbH” (Німеччина, 2007).
Етичні норми. План та зміст експериментальних досліджень розроблялися у відповідності до українських (наказ МОЗ України № 281 від 01.11.2000 р. "Про міри по подальшому вдосконаленню організаційних норм роботи з використанням експериментальних тварин") та міжнародних (General Laboratory Practice (1981), конвенція Ради Європи про охорону хребетних тварин, що використовуються в експериментах та інших наукових цілях № 123 (1986), директива Єврокомісії № 86/609 (1986)) стандартів, були схвалені етичною комісією Ужгородського національного університету (протокол № 6 від 04.12.2006).
Лабораторні тварини. При порівнянні різних видів експериментальних тварин найбільш зручним виявилось використання статевозрілих морських свинок (Cavia porcellus) вагою 200-350 г обох статей. Тварини були виведені у віварії Ужгородського національного університету і утримувались в стандартних умовах з вільним доступом до води та корму. Загальна кількість тварин становила 52 особини з однаковою кількістю самок та самців. Необхідний рівень знеболення та знечулення досягався внутрішньом’язовим введенням розчину кетаміну, в якому містилося близько 10 мг діючої речовини в комбінації з інфільтрацією шкіри в ділянці розрізу 2% розчином лідокаїну. Виведення морських свинок з експерименту виконувалось шляхом інгаляції токсичних доз етилового ефіру після внутрішньом’язевої ін’єкції 0,1 мл 5% розчину кетаміну.
Спосіб демієлінізації. За матеріалами огляду літератури нами було встановлено, що для запланованого дослідження експериментальна демієлінізація корінця трійчастого нерва може бути відтворена шляхом аплікації 0,1 та 0,05% розчинів броміду етидію об’ємом 1 мкл на вказану ділянку нерва. При подальшому порівнянні патоморфологічних змін корінців трійчастих нервів у відповідь на застосування вказаних вище речовин встановлено, що ушкодження мієлінової оболонки в залежності від концентрації броміду етидію характеризувалося частковим (локальним) або поширеним розволокненням і порушенням впорядкованості ламел на тлі вогнищевого або поширеного міжламелярного набряку різного ступеню виразності, злипанням ламел з наступним гомогенним їх набуханням на певному відрізку, частковим розщепленням ламел з прийманням спотворених у порівнянні з контролем форм (хвилясті, спіралеподібні, везикулярні утворення), повним розщепленням та лізисом мієлінових оболонок на певному відрізку корінця. Виявлено деякі гліоцити, які беруть участь у фагоцитозі мієліну. Останній розміщується у їх цитоплазмі у вигляді спіралеподібних або кільцеподібних утворень. Патологічні зміни в аксонах виявляються в помірному зморщуванні осьового циліндра на тлі явищ периаксонального набряку, реактивно-деструктивних змінах ультраструктурних органел, зокрема, мітохондрій (фрагментації крист та вогнищевої їх вакуолізації) і частковому просвітленні аксоплазми внаслідок втрати окремих нейрофіламентів (таб. 1).
Таблиця 1
Ознаки демієлінізації під впливом броміду етидію на субмікроскопічному рівні
| Ознака демієлінізації, ступінь значимості різниці між групами за критерієм Фішера-Ірвіна |
Концентрація розчину броміду етидію |
|
| 0.1% n=10 |
0.05% n=10 |
|
| Поширене розволокнення і порушення впорядкованості ламел мієліну, p<0.003 |
+ |
- |
| Виражений міжламелярний набряк, р<0.01 |
+ |
- |
| Повне розщеплення та лізис мієлінових оболонок, р<0.001 |
+ |
- |
| Часткове просвітлення аксоплазми, p<0.003 |
+ |
- |
| Зморщення осьового циліндра на тлі явищ периаксонального набряку |
+ |
+ |
| Фрагментація та вогнищева вакуолізація крист мітохондрій |
+ |
+ |
Дані, наведені в таб. 1, свідчать про залежність дегенеративних змін мієлінової оболонки від концентрації розчину броміду етидію. При цьому слід звернути увагу на те, що тільки 0,1% розчин вказаного гліотоксину викликає повне розщеплення та лізис мієлінових оболонок одночасно із збереженням структури осьових циліндрів. Це найбільш адекватно відтворює процес сегментарної демієлінізації зони входу корінця трійчастого нерва в ділянці стиснення артерією у хворих з невралгією, дозволяючи проводити експериментальні дослідження способів посилення ремієлінізації трійчастого нерва.
Хірургічний доступ до зони входу корінця трійчастого нерва. Для розробки мікрохірургічного доступу до корінця трійчастого нерва морської свинки було порівняно підходи до цієї структури через середню та задню черепні ямки. Порівнювались відстань від шкіри до тріґемінального корінця, наявність важливих для життєдіяльності тварини структур при виконанні доступу та простір для виконання маніпуляцій поблизу трійчастого корінця. Виявилось, що відстань від шкіри до корінця трійчастого нерва є меншою при доступі через середню черепну ямку. Доступ через задню черепну ямку передбачає маніпуляції із стовбуром мозку, каудальною групою черепно-мозкових нервів, сигмовидним синусом, що суттєво ускладнює хірургічну техніку втручання. Окрім вищевказаного, перевагою доступу через середню черепну ямку є більший об’єм простору для маніпуляцій поблизу тріґемінального корінця.
Було розроблено хірургічний доступ до зони входу вказаного нерва морської свинки, при якому трепанація черепа здійснювалась за допомогою мінідрелі та стоматологічних борів, використовувався операційний мікроскоп Carl Zeiss OPMI із збільшенням 14Ч та мікроінструментарій. Доступ передбачає трепанацію черепа експериментальної тварини в тім’яно-скроневій ділянці діаметром до 0,8 см. При цьому зручним орієнтиром є скронева лінія, як вентральна межа трепанаційного вікна. Розтин твердої мозкової оболони виконувався мікроскальпелем паралельно поперечному синусу. В субдуральному просторі цієї ділянки знаходиться невелика кількість ліквору. Після ретракції скронево-потиличної частки головного мозку морської свинки медіально добре видно поперечний синус із впадаючими в нього венами, тенторіум та мозочок. Водночас з’являється значна кількість церебро-спінальної рідини, аспірація якої давала змогу продовжувати ретракцію. На певному етапі візуалізувався трійчастий вузол та вирізка намету мозочка. Після розтину останнього значно збільшувався простір для маніпуляцій поруч з корінцем трійчастого нерва. Між наметом мозочка, стовбуром мозку та проксимальною частиною корінця трійчастого нерва за допомогою мікропінцета встановлювався матеріал з волокнистого тефлону.
В результаті розтину лабораторних тварин та макроскопічного дослідження їх головного мозку виявлено, що прокладка з волокнистого тефлону, яка була встановлена морським свинкам за допомогою розробленого доступу знаходиться навколо ділянки входу трійчастого нерва у стовбур мозку та щільно прилягає до його корінця. Тканина головного мозку морських свинок, яка оточувала тефлонову прокладку, звичайного кольору та консистенції, її судинний малюнок не змінений. Таким чином, запропонований мікрохірургічний доступ до корінця трійчастого нерва морських свинок забезпечує необхідний простір для виконання маніпуляцій у
9-09-2015, 00:23
