МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВ'Я УКРАЇНИ
ІВАНО-ФРАНКІВСЬКИЙ ДЕРЖАВНИЙ МЕДИЧНИЙ УНІВЕРСИТЕТ
ШОРІКОВА Діна Валентинівна
УДК: 616.12-008.331.1: 616.12-005.4] -085.22: 577.1
ВПЛИВ ЛЕРКАНІДИПІНУ І БІСОПРОЛОЛУ НА ФУНКЦІЇ ЕНДОТЕЛІЮ У ХВОРИХ НА ГІПЕРТОНІЧНУ ХВОРОБУ, ПОЄДНАНУ З ІШЕМІЧНОЮ ХВОРОБОЮ СЕРЦЯ
14.01.11. - кардіологія
АВТОРЕФЕРАТ
на здобуття наукового ступеня
кандидата медичних наук
Івано-Франківськ - 2008
Дисертацією є рукопис.
Робота виконана в Буковинському державному медичному університеті МОЗ України
Науковий керівник: доктор медичних наук, професор
ТАЩУК Віктор Корнійович,
Буковинський державний медичний університет МОЗ України,
кафедра кардіології, функціональної діагностики, лікувальної
фізкультури та спортивної медицини, завідувач кафедри
Офіційні опоненти: доктор медичних наук, професор
ЯЦИШИН Роман Іванович,
Івано-Франківський державний медичний університет
МОЗ України, кафедра факультетської терапії,
професор кафедри
доктор медичних наук, професор
БУГАЄНКО Веніамін Вікторович,
Національний науковий центр
“Інститут кардіології ім. акад. М.Д. Стражеска”
АМН України, м. Київ
відділ атеросклерозу та хронічної ішемічної хвороби серця, провідний науковий співробітник
Захист дисертації відбудеться “11” квітня 2008 року о 13 годині на засіданні спеціалізованої вченої ради Д 20.601.01 при Івано-Франківському державному медичному університеті МОЗ України (76018, м. Івано-Франківськ, вул. Галицька 2)
З дисертацією можна ознайомитись у бібліотеці Івано-Франківського державного медичного університету за адресою: 76018, м. Івано-Франківськ, вул. Галицька, 7
Автореферат розісланий “6“ березня 2008 р.
Вчений секретар
спеціалізованої вченої ради Д 20.601.01,
доктор медичних наук, професор О.І. Дєльцова
ЗАГАЛЬНА ХАРАКТЕРИСТИКА РОБОТИ
Актуальність теми. Гіпертонічна хвороба (ГХ) та ішемічна хвороба серця (ІХС) залишаються основною проблемою охорони здоров’я в більшості країн унаслідок їх впливу на показники смертності та захворюваності населення [Горбась І.М. 2005; Коваленко В.М., Сіренко Ю.М. 2005]. Прогноз у хворих на ГХ залежить від наявності уражень органів-мішеней [Guidelines for the management of arterial hypertension 2007], зокрема, серця та судин [Гаман С.А. и др. 2005; Bard R. L. et al. 2004]. На даний час гіпертрофія лівого шлуночка (ГЛШ) вважається незалежним фактором ризику ГХ та ІХС [Радченко Г.Д., Сіренко Ю.М. 2006; Devereux R. et al. 2004; Harris K. M. et al. 2006]. Іншою важливою мішенню, що вражається при ГХ є сонні артерії (СА) [Гуляев С.А. и др. 2004]. Одним із механізмів, що впливають на ремоделювання судин є дисфункція ендотелію [Бабак О.Я. и др. 2006; Deanfield J. et al. 2005], тому поширюється зацікавленість у вивченні його функціонального стану, як маркера ураження серцево-судинної системи [Нейко Є.М. 2005; Яцишин Р.І. 2003; Pollock 2005; Becker R. C. 2005; Gössl M. et al. 2006].
Також постає питання про можливість підвищення ефективності лікування ІХС у хворих на ГХ шляхом застосування антигіпертензивних препаратів, які мають органопротекторні та ендотеліопротекторні властивості [Амосова К.М. 2004; Лутай М.И. и др. 2004]. Ефективність застосування β-адреноблокаторів та блокаторів кальцієвих каналів (БКК) у хворих на ГХ та ІХС доведено в чисельних багатоцентрових дослідженнях [COPERNICUS, SENIORS, CIBIS I-III, INVEST, ELSA та ін.]. У трайлах CIBIS I-III продемонстровано ефективність бісопрололу щодо зменшення смертності, частоти госпіталізації у хворих із хронічною серцевою недостатністю (ХСН) через вплив на параметри ремоделювання ЛШ. Проте вплив препарату на показники судинного ремоделювання та ендотеліальної дисфункції практично не досліджувався. У трайлах INSIGHT та ELSA доведено антиатерогенну дію БКК дигідропіридинового ряду, водночас дослідження відповідного ефекту лерканідипіну та вивчення його впливу на функцію ендотелію, параметри ремоделювання ЛШ не проводились.
Таким чином, розширення діагностичного підходу щодо ГХ, поєднаної з ІХС, дослідження додаткових ефектів лерканідипіну та бісопрололу зумовлює актуальність даної роботи.
Зв'язок роботи з науковими програмами, планами, темами. Дисертація є фрагментом науково-дослідної роботи кафедри кардіології, функціональної діагностики, ЛФК та спортивної медицини Буковинського державного медичного університету (БДМУ) на тему “Клініко-патогенетичні та нейромесенджерні механізми розвитку та реалізації серцевої недостатності в умовах гострого коронарного синдрому та стабільної стенокардії (СС) з оптимізацією лікувальної тактики та визначенням прогностичних предикторів” (№ держреєстрації 0107U004053).
Мета і задачі дослідження. Визначити особливості дисфункції ендотелію, ремоделювання серця та сонних артерій у хворих на ГХ за поєднаного перебігу зі стабільною стенокардією (СС), а також оцінити ефективність лерканідипіну та бісопрололу щодо корекції виявлених порушень.
Для досягнення даної мети були сформульовані наступні задачі:
Визначити особливості ремоделювання ЛШ та СА, а також ступінь впливу ГХ та СС на параметри ремоделювання, встановити взаємозв’язки між структурними змінами серця та судин.
Дослідити зміни проліферативної, антикоагулянтної, фібринолітичної функцій ендотелію в пацієнтів із поєднаним перебігом ГХ та СС.
Оцінити стан протеолітичної системи плазми крові, ліпідної ланки гомеостазу та морфофункціональних властивостей еритроцитів у хворих на ГХ за поєднаного перебігу зі СС.
Дослідити вплив та оцінити вірогідність ефектів лерканідипіну та бісопрололу на процеси судинного та серцевого ремоделювання, а також функціональний стан ендотелію у хворих на ГХ за поєднаного перебігу зі СС.
Об’єкт дослідження – функціональний стан ендотелію, ремоделювання лівого шлуночка та сонних артерій у хворих на ГХ зі стабільною стенокардією напруження.
Предмет дослідження - показники, які характеризують функціональний стан ендотелію, параметри ремоделювання лівого шлуночка та сонних артерій, їх динаміка на тлі лікування лерканідипіном та бісопрололом.
Методи дослідження – клініко-лабораторні, функціональні, біохімічні, імуноферментні.
Наукова новизна отриманих результатів. У роботі вперше встановлено, що у хворих на ГХ за поєднаного перебігу зі СС визначається вірогідно нижчий рівень фактора ангіогенезу відносно практично здорових осіб, доведено більш істотне зниження антикоагулянтної та фібринолітичної функцій ендотелію в пацієнтів із ГХ та СС на відміну від хворих на ГХ без СС. Встановлено, що раннім проявом ремоделювання внутрішніх СА (ВСА) у хворих на ГХ є збільшення діаметра судин, а більш значне потовщення комплексу інтима-медіа (КІМ) СА встановлено в осіб із поєднаним перебігом ГХ та СС.
Уперше встановлено, що через 12 тижнів антигіпертензивної терапії лерканідипіном та бісопрололом вірогідно підвищився рівень фактора ангіогенезу, лерканідипін перевищував бісопролол за здатністю підсилювати антикоагулянтний потенціал ендотелію та інтенсивністю впливу на зворотній розвиток ремоделювання внутрішніх СА (патент України №25030), водночас, бісопролол більш істотно сприяв регресу ГЛШ та підсилював фібринолітичну активність ендотелію.
Уперше проведено оцінку міри впливу ГХ та СС, за умов їх поєднаного перебігу, на показники структурних змін ЛШ та внутрішніх СА шляхом моделювання за методом Снедекора кількісних показників – маси міокарда (ММ), відносної товщини стінок лівого шлуночка (ВТСЛШ), діаметрів СА та величини КІМ.
Практичне значення одержаних результатів. Робота є комплексним дослідженням, в якому патогенетично обгрунтовано необхідність застосування дуплексного сканування СА та ехокардіографії (ЕхоКГ) для підвищення якості діагностики уражень серця та судин у хворих на ГХ за поєднаного перебігу зі СС. Водночас, застосування цих методів дозволило встановити органопротективні властивості лерканідипіну та бісопрололу та підвищити ефективність лікування хворих на ГХ. Доведено, що вміст судинного ендотеліального фактора росту в сироватці крові, показники агрегаційної здатності тромбоцитів, активність протеїну С та потенційна активність плазміногену є вірогідними маркерами для оцінки ступеня дисфункції ендотелію. Розроблено підхід до диференційованого застосування лерканідипіну та бісопрололу у хворих на ГХ за поєднаного перебігу зі СС.
Основні результати дисертації використовуються в навчальному процесі на кафедрах терапевтичного профілю Буковинського та Івано-Франківського державних медичних університетів, впроваджено в практику профільних відділень міської клінічної лікарні №3 м. Винниці, Хотинської, Сокирянської, Кельменецької ЦРЛ, Закарпатського обласного кардіологічного диспансеру, лікарні швидкої медичної допомоги та госпіталю інвалідів Великої Вітчизняної війни м. Чернівці.
Особистий внесок здобувача. Особистий внесок автора в отриманні наукових результатів є основним. Дисертант особисто проаналізувала наукову літературу, що дозволило визначити напрямок дослідження. Самостійно проводила підбір та обстеження хворих, призначала лікування. Сформувала базу даних дисертації. Статистичну обробку отриманих результатів і написання всіх розділів дисертаційної роботи автор провела самостійно. Висновки та практичні рекомендації сформульовані разом із керівником.
Апробація результатів дисертації. Матеріали дисертації доповідались та обговорювались на спільних засіданнях терапевтичних кафедр Буковинського державного медичного університету, ХІ конгресі світової федерації Українських лікарських товариств (Полтава, 28-30 серпня 2006), ІV міжнародній науково-практичній конференції студентів та молодих вчених (Ужгород, 18-20 квітня 2006), ІІІ Міжнародній медико-фармацевтичній конференції студентів та молодих вчених (Чернівці, 2006), Міжнародній науковій конференції студентів та молодих вчених “Молодь – медицині майбутнього” (м. Одеса, 20-21 квітня 2006), Всеукраїнській науково-практичній конференції “Здобутки та перспективи внутрішньої медицини” (Тернопіль, 19-20 жовтня, 2006), науково-практичній конференції молодих вчених, присвяченій 145-річчу Харківського медичного товариства “Медична наука: сучасні досягнення та інновації”(Харків, 23 листопада 2006), 18th European Students’ Conference (Berlin, 7th-11th October, 2007).
Публікації. За матеріалами дисертаційної роботи опубліковано 14 наукових праць, із них 5 статей - у фахових виданнях, рекомендованих ВАК України (2 - одноосібні), 9 тез у матеріалах наукових конгресів, пленумів, конференцій, отримані один деклараційний патент України на корисну модель та посвідчення на раціоналізаторську пропозицію.
Структура та обсяг дисертації. Дисертація викладена на 161 сторінці основного тексту і складається зі вступу, огляду літератури, матеріалів і методів дослідження, результатів власних досліджень, викладених у чотирьох розділах, аналізу та узагальнення результатів, висновків та практичних рекомендацій. Роботу ілюстровано 72 таблицями та 18 рисунками. Бібліографічний вказівник містить 322 джерела, із них 75 – кирилицею та 247 - латиною.
ОСНОВНИЙ ЗМІСТ РОБОТИ
Матеріал та методи дослідження. Відповідно до завдань дослідження під спостереженням знаходились 158 пацієнтів на ГХ, які були поділені на п’ять груп: 1 група – хворі на ГХІ ст. (15 осіб), 2 група – хворі на ГХ ІІ ст. (16 осіб), 3 група – пацієнти з ГХІІ ст. та стабільною стенокардією ІІ функціонального класу (ГХІІССІІФК - 50 осіб), 4 група – хворі на ГХІІ ст. та стабільну стенокардію ІІІ ФК (ГХІІССІІІФК - 39 осіб), 5 група – пацієнти з ГХІІІ ст. та стабільною стенокардією ІІІ ФК (ГХІІІССІІІФК - 38 осіб).
Дослідження проводилось в умовах кафедри кардіології, функціональної діагностики, ЛФК та спортивної медицини БДМУ, обласного кардіологічного диспансеру, поліклініки профоглядів та обласного діагностичного центру м. Чернівців. Контрольну групу склали 25 осіб, репрезентативні за віковим та статевим розподілом основній групі. Верифікацію діагнозу СС та визначення стадії ГХ проводили з використанням критеріїв, рекомендованих Українською асоціацією кардіологів (2004) та Європейським товариством гіпертензії та кардіології. Залежно від антигіпертензивної терапії в усіх групах виділяли дві підгрупи: хворі, які отримували бісопролол (“Конкор”, Nycomed, № 3364 від 25.01. 2005) та пацієнти, що отримували лерканідипін (“Леркамен”, Berlin-Chemie, № UA/0583/01/01 від 20.02. 2004); титрування доз препаратів проводилось згідно консенсусу по застосуванню β-адреноблокаторів (2004) та Європейських рекомендацій по лікуванню артеріальної гіпертензії (2003). Незалежно від антигіпертензивного препарату всі хворі на ГХ та СС отримували стандартне лікування згідно рекомендацій Європейського товариства кардіологів по лікуванню стабільної стенокардії (2006). Загальна тривалість контрольованого лікування складала 12 тижнів .
Ехокардіографія (ЕхоКГ) проводилась за стандарною методикою на ультразвукових сканерах “INTERSPEС XL”(USA) та “EnVisor HD” (Philips Ultrasound System, USA), маса міокарда (ММ) ЛШ визначалась за формулою R. Devereux та N. Reicheck у модифікації ASE: (ММ = 0.8 х {1.04 х ([КДР + ТЗСд + ТМПд] 3 - [КДР] 3) }+ 0,6 (г)). Стан загальних, зовнішніх та внутрішніх СА досліджувався системою “EnVisor HD” (Philips, USA) обласного діагностичного центру м. Чернівці за методикою В.Г. Лелюк (2003). Для встановлення функціонального класу СС проводилась велоергометрична проба.
Рівень холестерину (ХС) та β-ліпопротеїнів (β-ЛП) визначали методом Златкіс-Зака (“Danish Ltd. ”, Україна). Для дослідження проліферативної активності ендотелію визначали вміст у крові фактора ангіогенезу (твердофазний імуноферментний метод, реактив BioSource International (USA), аналізатор Rayto-2100C (China)), агрегаційні властивості тромбоцитів досліджувались на агрегометрі АР-2110 (Solar, Беларусь) турбідиметричним методом за J. Born (1962). Рівень фібриногену в плазмі крові, активність антитромбіну III (АТ III), інтенсивність Хагеманзалежного фібринолізу (ХЗФ), вміст XIII фактора (ХІІІФ), потенційну активність плазміногену (ПАП), сумарну фібринолітичну активність (СФА), ферментативний (ФФА), неферментативний фібриноліз (НФА) та протеолітичну активність за лізисом азоальбуміну, азоказеїну, азоколу визначали за допомогою реактивів “Danish Ltd. ” (Україна) та фотоелектроколориметру КФК-3. Активність протеїну С встановлювали коагулометричним методом (НПО “РЕНАМ”, Москва). Морфофункціональний стан еритроцитів оцінювали методом З.Д. Федорової, М.О. Котовщикової (1989).
Для статистичного аналізу використовували пакет програм Statistica for Windows версії 6.0 (Stat Soft inc., США) та EpiInfo 2000, версія 3.3.2. Вірогідність різниці визначали t-критерієм Стьюдента та F-критерієм Фішера для параметричних даних. При непараметричному розподілі використовували для множинного порівняння – Н-критерій Краскела-Уоліса, для парного – ранговий U-критерій Манна-Уітні (у випадку незалежних вибірок) та Т-критерій Вілкоксона (у випадку залежних груп). Для оцінки міри залежності між перемінними використовували кореляційний аналіз за Пірсоном та коефіціент рангової кореляції Спірмена. Для оцінки ступеня факторного впливу використовували метод Снедекора. Оцінка ефективності лікування проводилась із урахуванням виходів лікування, абсолютного (АЕ,%) та відносного (ВЕ) терапевтичних ефектів, терапевтичної користі (різниця АЕ), а також відношення шансів (ВШ) препаратів, із розрахунком довірчих інтервалів та критерію вірогідності щодо ВЕ та ВШ. При р<0,05 розбіжності вважали статистично вірогідними.
Результати дослідження та їх обговорення. За аналізу кардіогемодинаміки було встановлено, що у хворих на ГХ зі СС більш суттєво зменшуються показники систолічної функції ЛШ: фракція викиду (ФВ), ударний об’єм, ударний індекс, хвилинний об’єм крові, серцевий індекс порівняно з хворими на ГХ без СС (р<0,05). Маса міокарда (ММ), індекс маси міокарда (ІММ) та відносна товщина стінок лівого шлуночка (ВТСЛШ) у хворих із поєднаним перебігом ГХ та СС перевищували відповідні показники у хворих на ГХ без СС (р1-3<0,05). Враховуючи таку тенденцію, у пацієнтів із ГХ та СС частіше, ніж у хворих на ГХ без СС, визначались патологічні типи геометрії ЛШ, із переважанням концентричної гіпертрофії міокарда. За результатами кореляційного аналізу встановлено вірогідний (p=0,02) зворотній кореляційний зв’язок середньої сили (r=-0,27) між ММ та ФВ ЛШ. При визначенні міри факторного впливу ГХ та СС на параметри ремоделювання ЛШ встановлено, що зміна ММ та ІММ залежить більшою мірою від ГХ (37,9%, p<0,001), ніж від СС (28,4%, p<0,001), а зміни ВТСЛШ обумовлені асоційованим впливом ГХ та СС (55,7%, p<0,001).
За результатами ультразвукового дослідження ЗСА було встановлено, що величина КІМ ЗСА у хворих на ГХІІ без СС не відрізнялась від контролю (p>0,05), однак мала місце асиметрія КІМ правої та лівої ЗСА (22,0%, р<0,05). У хворих із поєднаним перебігом ГХ та СС відмічається збільшення величини та ступеня асиметрії КІМ ЗСА відносно групи хворих на ГХ без СС (р1-3<0,05). У ВСА величина КІМ у хворих на ГХ без СС вірогідно збільшувалась відносно контролю лише справа (p<0,05), у хворих із поєднаним перебігом ГХ та СС дані зміни реєструвались з обох сторін (p<0,05), при чому товщина КІМ у ВСА та ступінь асиметрії залежали від стадії ГХ та ФК стенокардії (рис.1).

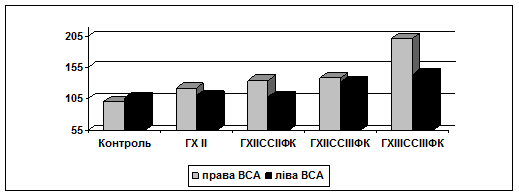
Рис.1. Величина комплексу інтима-медіа (%) внутрішніх сонних артерій у хворих на неускладнену гіпертонічну хворобу та гіпертонічну хворобу зі стабільною стенокардією.
При моделюванні міри факторного впливу встановлено, що ступінь впливу стенокардії на величину КІМ переважав ступінь впливу ГХ у ЗСА (41,3 проти 24,5% справа, 38,3% проти 23,0% зліва), ВСА (38,0 проти 21,6% справа та 42,1 проти 27,0% зліва) та Зов. СА (46,1 проти 21,6% справа та 40,7 проти 29,7% зліва) СА.
Діаметри ЗСА у хворих на ГХ без СС не відрізнялись від контролю (p>0,05), проте вірогідно перевищували норму при поєднаному перебігу ГХ та СС (р<0,05). Водночас, як у пацієнтів з ГХ без СС, так і за поєднаного перебігу ГХ та СС (p<0,05) діаметр ВСА вірогідно перевищував контроль, причому збільшення діаметру ВСА виявлялось навіть за незміненого КІМ. У всіх випадках був встановлений прямий кореляційний зв’язок між ММ ЛШ, діаметром та КІМ СА (табл.1).
Таблиця 1. Кореляційний зв’язок між масою міокарда лівого шлуночка, діаметром та комплексом інтима-медіа зовнішніх і внутрішніх сонних артерій
| Права ЗСА | Ліва ЗСА | Права ВСА | Ліва ВСА | |||||
| КІМ | діаметр | КІМ | діаметр | КІМ | діаметр | КІМ | діаметр | |
| ММЛШ | r=0,36* | r=0,50* | r=0,24 | r=0,45* | r=0,36* | r=0,43* | r=0,40* | r=0,30* |
* – вірогідний кореляційний зв’язок.
При дослідженні функціонального стану ендотелію, зокрема, судинно-тромбоцитарного гемостазу було встановлено, що у хворих на ГХ без СС та ГХ зі СС спостерігається зростання ступеня спонтанної агрегації тромбоцитів відносно такої в практично здорових осіб (p<0,05), із більш значними змінами за наявності ГХ зі СС (p1-3<0,05), у той час, як АДФ-індукована агрегація вірогідно підвищувалась лише у хворих на ГХ зі СС (p<0,05). Час агрегації тромбоцитів та швидкість агрегації вірогідно не відрізнялись у хворих на ГХІ, ГХІІ, ГХІІССІІФК та контролем, проте змінювались (час скорочувався, швидкість зростала) у хворих на ГХІІССІІІФК та ГХІІІССІІІФК (p<0,05). Окрім того, у хворих із ГЛШ зареєстрований більш високий рівень АДФ-індукованої (р=0,051) агрегації тромбоцитів та вірогідне зменшення часу агрегації (p<0,05) відносно пацієнтів без ГЛШ, причому за наявності концентричної ГЛШ ці зміни були більш значними (p<0,05), ніж у хворих із іншими типами ремоделювання міокарда. Також встановлено пряму кореляційну залежність між величиною КІМ ЗСА (r=0,38, p<0,05) та ВСА (r=0,44, p<0,05) та ступенем АДФ-індукованої агрегації тромбоцитів.
Оцінку стану антикоагулянтної активності за рівнем протеїну С (PtC) проводили шляхом кластерного аналізу, у результаті чого було отримано 3 кластери з достовірною різницею між
8-09-2015, 21:55
