Міністерство охорони здоров’я України
Державний вищий навчальний заклад
Тернопільський державний медичний університет
імені І.Я. Горбачевського
ПОРОХОВСЬКА НАТАЛІЯ ВАСИЛІВНА
УДК: 616-056.3-036.11:616.127]-092.9:599.324.7
МЕМБРАНОЗАЛЕЖНІ ПРОЦЕСИ В ТКАНИНІ МІОКАРДА МОРСЬКИХ СВИНОК ЗА УМОВ ГОСТРОЇ ГІПЕРІМУНОКОМПЛЕКСНОЇ ПАТОЛОГІЇ
14.03.04 – патологічна фізіологія
АВТОРЕФЕРАТ
дисертації на здобуття наукового ступеня
кандидата медичних наук
Тернопіль – 2008
Дисертацією є рукопис.
Робота виконана у Львівському національному медичному університеті
імені Данила Галицького МОЗ України
Науковий керівник:доктор медичних наук, професор Бідюк Мартин Миколайович.
Офіційні опоненти:доктор медичних наук, професор Мисула Ігор Романович, Державний вищий навчальний заклад «Тернопільський державний медичний університет імені І.Я. Горбачевського МОЗ України», завідувач кафедри медичної реабілітації та спортивної медицини;
доктор медичних наук, професор Казімірко Ніла Казімірівна, Луганський державний медичний університет МОЗ України, завідувач кафедри патологічної фізіології.
Захист відбудеться 18 квітня 2008 р. о 12 годині на засіданні спеціалізованої вченої ради Д 58.601.01 у Державному вищому навчальному закладі «Тернопільському державному медичному університеті імені І.Я. Горбачевського» МОЗ України (46001, м. Тернопіль, Майдан Волі, 1).
З дисертацією можна ознайомитися у бібліотеці Державного вищого навчального закладу «Тернопільського державного медичного університету імені І.Я. Горбачевського» МОЗ України (46001, м. Тернопіль, вул. Січових Стрільців,8).
Автореферат розісланий 12 березня 2008 р.
Вчений секретар спеціалізованої вченої ради
доктор медичних наук, професор Я.Я. Боднар.
ЗАГАЛЬНА ХАРАКТЕРИСТИКА РОБОТИ
Актуальність теми. Аналіз даних ВООЗ доводить, що алергічні захворювання залишаються найважливішою медико-соціальною проблемою (Чучалин А.Г., 2000), оскільки за останні 10 років кількість хворих на алергію і аутоімунні захворювання збільшилися з 10–15% до 20–30%. Це пов’язано з тим, що імунна система не завжди може адекватно прореагувати на постійне зростання антигенного навантаження (хімічні, синтетичні, фізичні та біологічні чинники, медикаменти, вакцини та ін.) та динамічну зміну складу антигенів. Сьогодні важко знайти нозологічну одиницю, в розвитку якої не була б зацікавлена імунна система. Однією з таких патологій є імунокомплексна хвороба, розвиток якої спричинений імунними комплексами. Вона включає велику кількість нозологій: ревматоїдний артрит, системний червоний вовчак, гломерулонефрит і тубулоінтерстиціальний нефрит, системні васкуліти, хвороба Рейно, велика група інфекційних захворювань, параонкологічні захворювання, ускладнення трансплантації нирок тощо (Аванесов А.М., 1999, Кузнецов С.А., 2000, Волосянко А.Б., 2000, Сааб Халед Зейн-Эддин, 1995, Чоп’як В.В., 1998, Kawana S., 1998). Вони характеризуються запальними ураженнями судин, нирок, серця, суглобів (Аванесов А.М., 1999; Сааб Халед Зейн-Эддин, 1995; Чоп’як В.В., 1998; Kawana S., 1998). Однак зусилля більшості дослідників проблеми імунокомплексної патології зосередженні на вивченні змін у нирках, суглобах та судинах і лише поодинокі роботи присвячені дослідженню змін у серці (Мойбенко А.А., 1992; Сааб Халед Зейн-Эддин, 1995; Bachetti T., 1998). А саме, Мойбенко О.О. зі співавт. досліджували імуногенні порушення скоротливої функції серця при різних типах алергічних реакцій.
Вивчення різноманітних сторін патогенезу захворювань серцево-судинної системи є не менш актуальною проблемою медицини, оскільки смертність від них невпинно зростає (Гуревич М.А., 1998; Мойбенко О.О., 2002; Angelini A., 2000; Hufnagel G., 2000).
Проте, на сьогодні залишаються не з’ясованими структурно-метаболічні зміни у міокарді. Невирішеними залишаються питання корекції можливих змін у кардіоміоцитах при імунокомплексних захворюваннях. Тому питання про мембранозалежні процеси у кардіоміоцитах за умов гострої гіперімунокомплексемії та пошук можливої їх корекції є відкритим, що свідчить про актуальність нашого дослідження і заслуговує експериментальних розробок з метою подальших методичних рекомендацій для використання їх у терапії імунокомплексної патології.
Зв’язок роботи з науковими програмами, планами, темами. Дисертаційна робота є складовою частиною планової наукової кафедральної теми «Імуно-ендотеліально-залежні механізми в розвитку гіперімунокомплексного синдрому в експерименті та клініці», яку виконує кафедра патологічної фізіології Львівського національного медичного університету імені Данила Галицького (№ держреєстрації 0101U009233). Автор був відповідальним виконавцем зазначеної науково-дослідної роботи. Тема дисертації затверджена Проблемною комісією МОЗ та АМН «Патологічна фізіологія та імунологія» (протокол № 16 від 5 березня 2002 року).
Мета дослідження. З’ясувати вплив гострої імунокомплексної патології на морфо-функціональний стан мембран кардіоміоцитів, дати їм патофізіологічну оцінку і з’ясувати можливість корекції виявлених змін мембранопротекторами тіотріазоліном і корвітином з метою подальших розробок методичних рекомендацій для використання їх у терапії імунокомплексної патології.
Завдання дослідження.
1. На моделі гострого імунокомплексного процесу дослідити рівень циркулюючих імунних комплексів та загальну комплементарну активність сироватки крові.
2. З’ясувати вплив циркулюючих імунних комплексів на систему пероксидне окиснення ліпідів – антиоксидантний захист при гострій сироватковій хворобі.
3. Дослідити ступінь метаболічних змін у міокарді за даної патології.
4. З’ясувати можливі зміни в системі енергопостачання клітин серця за умов гострої сироваткової хвороби.
5. Дослідити структурні зміни у міокарді за умов гострої сироваткової хвороби.
6. З’ясувати можливість фармакокорекції виявлених метаболічних та структурних змін у міокарді тіотріазоліном та корвітином.
Об’єкт дослідження – гіперімунокомплексний процес, відтворений у морських свинок з використанням моделі гострої сироваткової хвороби.
Предмет дослідження – прямі та опосередковані показники процесів у мембранах кардіоміоцитів морських свинок за умов гострої сироваткової хвороби та при введенні цим тваринам тіотріазоліну і корвітину.
Методи дослідження:
– імунологічні: визначення циркулюючих імунних комплексів різних розмірів та гемолітичної активності комплементу сироватки;
– біохімічні: визначення у сироватці крові концентрації органоспецифічних ферментів (лактатдегідрогеназа, креатинфосфокіназа, аспартатамінотрансфераза), дослідження активності пероксидного окиснення ліпідів (ПОЛ) за вмістом у сироватці крові малонового діальдегіду, дослідження антиоксидантної активності за вмістом у сироватці крові супероксиддисмутази та каталази, визначення кількості сульфгідрильних груп в ендокарді, міокарді та сироватці, визначення пероксидного гемолізу еритроцитів; визначення активності гліколізу за вмістом у сироватці лактату та пірувату;
– морфологічні: загальна світлова та електронна мікроскопія;
– математичні: обробка цифрових даних методом варіаційної статистики з використанням критерію Стьюдента.
Наукова новизна отриманих результатів. Вперше на сучасному методичному рівні вивчено структурні та метаболічні зміни в мембранах кардіоміоцитів за умов гострого імунокомплексного процесу у морських свинок. Вперше досліджено активність мембранних ферментів та органоспецифічних ферментів ураженого міокарда в аналогічних умовах. Вперше досліджено структуру міокарда при імунокомплексній патології і виявлено морфологічні зміни. Виявлені зміни корелюють з прямими та непрямими показниками пошкодження міокарда. Вперше вивчено вплив на ці зміни корвітину та тіотріазоліну. Доведена виражена коригуюча дія обох препаратів на метаболічні та структурні порушення, що виникли за умов гострої сироваткової хвороби (знижується рівень циркулюючих імунних комплексів малих та середніх розмірів, нормалізується гемолітична активність комплементу, знижується активність пероксидного окиснення ліпідів, підвищується антиоксидантна активність, що призводить до стабілізації мембран і активності мембранозалежних ферментів).
Практичне значення отриманих результатів. Результати виконаних досліджень розширюють існуючі уявлення про патогенез імунокомплексних уражень, а також роль у цих механізмах циркулюючих імунних комплексів та продуктів пероксидного окиснення ліпідів, глибину та серйозність метаболічних та морфологічних змін у серці і вплив на ці процеси корвітину та тіотріазоліну. Виражена імуномодулююча, антиоксидантна та мембранопротекторна дія корвітину вказує на доцільність його подальшого вивчення з метою корекції цих порушень за умов патології імунокомплексного ґенезу і розробки методичних рекомендацій.
Результати дослідження впроваджені у навчальний процес на кафедрах патологічної фізіології Львівського національного медичного університету імені Данила Галицького, Державного вищого навчального закладу «Тернопільського державного медичного університету імені І.Я. Горбачевського», Харківського державного медичного університету, Луганського державного медичного університету, на кафедрах патологічної анатомії Львівського національного медичного університету імені Данила Галицького та Державного вищого навчального закладу «Тернопільського державного медичного університету імені І.Я.Горбачевського», а також у практичну медицину у Львівському обласному патанатомічному бюро дитячій патанатомічній лабораторії, що підтверджено відповідними актами впровадження.
Особистий внесок здобувача. За пропозицією нині покійного д.м.н., професора Бідюка М.М. нами проведено дослідження морфо-метаболічних змін у міокарді морських свинок за умов гострої сироваткової хвороби. Наукова робота зроблена та написана, завдячуючи постійній увазі професора Бідюка М.М., його цінним порадам та науковому керівництву. Дисертаційна робота є особистою науковою працею здобувача. Проведено інформаційний і патентний пошук. На основі проведеного літературного огляду автор оцінила сучасний стан проблеми, обґрунтувала актуальність роботи, мету і завдання, вибрала обсяг і методи дослідження, експериментальних тварин, підібрала та опрацювала адекватні моделі і методики. Самостійно виконала всю експериментальну частину роботи. Підготувала матеріал для морфологічних досліджень. Статистично обробила, проаналізувала і узагальнила отримані результати, а також оформила їх у вигляді таблиць та рисунків, сформулювала висновки. В опублікованих зі співавторами наукових працях здобувачу належать основні ідеї, практичний матеріал та їх узагальнення. У тій частині актів впровадження, що стосується науково-практичної новизни, викладено фактичні дані отримані дисертантом.
Апробація результатів дисертації. Основні результати роботи були оприлюднені і обговорені на Пленумі патофізіологів України (Одеса, 2002); Міжнародній науково-практичній конференції присвяченій пам’яті професора І.В. Шостаковської (Львів, 2002); IV Українській науково-практичній конференції з клінічної фармакології (Вінниця, 2004); студентській науково-практичній конференції (Львів, 2005); науково-практичній конференції студентів та молодих вчених (Івано-Франківськ, 2006).
Публікації. Результати дисертації викладено у 10 друкованих працях, з них 5 – у наукових фахових виданнях та 5 – у матеріалах і збірниках конференцій та конгресів.
Обсяг і структура дисертації. Дисертаційна робота викладена на 160 сторінках машинописного тексту і складається зі вступу, 6 розділів, висновків, списку використаних джерел, що нараховує 323 найменування, а також 8 додатків. Робота ілюстрована 20 таблицями, 23 рисунками. Бібліографічний опис літературних джерел та додатки викладені на 42 сторінках.
ОСНОВНИЙ ЗМІСТ РОБОТИ
Матеріали та методи дослідження. Досліди виконані на 120 статевозрілих морських свинках-самцях, масою 380–400 г, яких утримували на стандартному раціоні віварію, у зимову пору року. Досліди на тваринах виконувалися з дотриманням ухвали Першого національного конгресу з біоетики про захист хребетних тварин, які використовуються для експериментальних та наукових цілей (Київ, 2001). Комісією з біоетики Львівського національного медичного університету імені Данила Галицького (протокол № 4від 23 квітня 2007 року) порушень морально-етичних норм при проведенні науково-дослідної роботи не виявлено. Усіх тварин поділили на групи по 20 тварин у кожній: 1 група – інтактні тварини; 2 група – інтактні тварини, які отримували розчин корвітину; 3 група – інтактні тварини, які отримували розчин тіотріазоліну; 4 група – тварини з викликаною гострою сироватковою хворобою; 5 група – тварини з викликаною гострою сироватковою хворобою, які отримували розчин корвітину; 6 група – тварини з викликаною гострою сироватковою хворобою, які отримували розчин тіотріазоліну.
Гострий імунокомплексний процес відтворювали на моделі гострої сироваткової хвороби, яка викликається одноразовим введенням у гомілкову вену задньої лапи морської свинки великої дози бичачого сироваткового альбуміну з розрахунку 500 мг/кг маси (Dixon F.J., Feldman I.D., 1961). Лабораторними критеріями гострої сироваткової хвороби було збільшення вмісту у сироватці крові циркулюючих імунних комплексів малих і середніх розмірів.
Імунологічні зміни оцінювали за кількістю у сироватці крові циркулюючих імунних комплексів різних розмірів (Haљkova V., 1977) та гемолітичною активністю комплементу (Вавилова М.М., 1984).
Особливості метаболічних процесів у міокарді аналізували за прямими та опосередкованими показниками. До прямих показників ураження міокарда належать органоспецифічні ферменти серця (лактатдегідрогеназа, креатинфосфокіназа, аспартатамінотрансфераза, які визначали за загальноприйнятими методами).Опосередкованими показниками змін у міокарді були: активність пероксидного окиснення ліпідів –вміст у сироватці крові малонового діальдегіду (Тимирбулатов Р.А., Селезнев Е.И, 1981), антиоксидантна активність – вміст у сироватці крові супероксиддисмутази (Костюк В.А., 1990) та каталази (Королюк М.А., 1988); індекс антиокисної активності біологічного матеріалу (Мартинюк В.Б., Ковальчук С.Н., 1991); кількість сульфгідрильних груп в ендокарді, міокарді та сироватці (Фоломеев В.Ф., 1981); стан клітинних мембран оцінювали за відсотком гемолізованих еритроцитів (Гжегоцький М.Р., Ковальчук С.М., 2002); показники активності гліколізу – вміст у сироватці лактату та пірувату (Horost H.J., 1965).
Ступінь структурних змін оцінювали за результатами світлової та електронної мікроскопії (за загальноприйнятими методами).
Виявлені зміни коригували тіотріазоліном і корвітином. Обидва препарати вводили доочеревинно 1 раз на добу, протягом 10 днів: корвітин вводився в разовій дозі 40 мг/кг (Максютина Н.П., Мойбенко О.О., 2000), а тіотріазолін – в разовій дозі 50 мг/кг (Піняжко О.Р., Кайдашев І.П., 1997).
Досліджуваний середник тіотріазолін (Т) виробляється АТ «Галичфарм» у місті Львові. Він є гепато- і кардіопротектором. Його фармакологічна дія зумовлена: антиішемічними, мембраностабілізуючими, антиоксидантними і імуномодулюючими властивостями (Визир А.Д., 1993; Піняжко О.Р., 1997; Нейко Е.М., 1998; Визир А.Д., 2002).
Препарат корвітин – натуральний екстракт із класу біофлавоноїдів з: антигістамінною дією (блокує вироблення гістаміну, серотоніну та лейкотрієнів); протизапальною та протинабряковою дією; антиоксидантною дією (блокує вільні радикали як ендогенного так і екзогенного походження); стабілізує клітинні мембрани, знижує проникність капілярів; (Визир В.А., 1999; Калиман П.Л., 2001, Мойбенко А.А., 1995; Марков А.Г., 2002). Ми використовували парентеральну форму «Корвітин»® , що випускає Борщагівський хімфармзавод.
Статистичний аналіз отриманих результатів проводився за допомогою методу варіаційної статистики (Минцер О.П., Угаров Б.Н., 1991) використовуючи t‑критерій Стьюдента для оцінки достовірності відмінностей груп даних. Статистично достовірними вважалися результати, для яких Р ≤ 0,05.
Основні результати досліджень та їх обговорення. При вивченні особливостей розвитку гострого імунокомплексного процесу (ГІКП) було виявлено достовірне зростання показників циркулюючих імунних комплексів малих розмірівна 21% (Р < 0,001) та середніх на 39% (Р < 0,001). Одночасно з цим, знизилися показники гемолітичної активності комплементу (ГАК) на 23% (Р < 0,001), що свідчить про залучення його у патологічний процес.
Розвиток гострої сироваткової хвороби викликав дисбаланс у системі пероксидне окиснення ліпідів – антиоксидантний захист. Як видно з табл. 1 достовірно зріс рівень малонового діальдегіду(МДА) на 44% (Р < 0,02), зросли індекс антиоксидантної активності (ІАОА ) на 60% (Р < 0,001) та активність каталази (Кат) на 11% (Р < 0,001), одночасно з цим, активність супероксиддисмутази(СОД) у крові знизилася на 29% (Р < 0,01). Кількість сульфгідрильних груп (-SH-груп) у тварин з гострою сироватковою хворобою зменшилася на 55% як в ендокарді (Р < 0,001), так і в міокарді (Р < 0,001), проте їх кількість у сироватці крові зросла на 25% (Р < 0,001).
Підвищений рівень патогенних циркулюючих імунних комплексів, компоненти комплементу та розбалансованість між процесами ліпопероксидації і антиоксидантною активністю викликали зміни у структурі мембран кардіоміоцитів, що супроводжується достовірним збільшенням у сироватці крові показників активності органоспецифічних ферментів. А саме активність креатинфосфокінази зросла в 1,9 разів (Р < 0,01), активність аспартатамінотрансферази – в 1,3 рази (Р < 0,01), і активність лактатдегідрогенази – у 1,5 рази (Р < 0,01).
Таблиця 1
Характеристика опосередкованих показників пошкодження клітинних мембран кардіоміоцитів у морських свинок за умов гострої сироваткової хвороби (М ± m; n = 20)
| Показник | Контроль | Дослід | Р |
| МДА, мкмоль/мл | 70,67 ± 0,74 | 102,0 ± 12,1 | 0,02 |
| ІАОА | 2,85 ± 0,04 | 4,57 ± 0,35 | 0,001 |
| СОД, од.акт./млЧхв | 458,47 ± 21,69 | 326,29 ± 12,90 | 0,001 |
| Каталаза, нмоль Н2 О2 /млЧгод. | 0,036 ± 0,001 | 0,040 ± 0,001 | 0,001 |
| SH-cироватка, мкмоль | 0,109 ± 0,005 | 0,136 ± 0,005 | 0,001 |
| SH-ендокард, мкмоль | 26,26 ± 1,33 | 11,72 ± 1,16 | 0,001 |
| SH-міокард, мкмоль | 10,57 ± 0,44 | 4,72 ± 0,72 | 0,001 |
| ПГЕ, % гемолізу | 8,82 ± 0,25 | 12,08 ± 0,29 | 0,001 |
| Примітка: Р – достовірність змін у порівнянні з контролем. | |||
Враховуючи, що еритроцитарні мембрани розглядаються як прототип плазматичних мембран всіх клітин організму, то зміна їх проникності може відображати зміни проникності мембран кардіоміоцитів. Стан мембран оцінювали за відсотком гемолізованих еритроцитів (ПГЕ) і було виявлено, що в дослідній групі цей показник зростає на 37% (Р < 0,001), отже проникність мембран кардіоміоцитів збільшилася.
Розвиток гострої сироваткової хвороби супроводжувався змінами в енергопостачанні кардіоміоцитів. Вміст у сироватці крові молочної кислоти зріс на 13% (Р < 0,05), а концентрація піровиноградної кислоти збільшилася на 70% (Р < 0,001) у порівнянні з інтактною групою тварин.
При морфологічному дослідженні тканин серця було виявлено нерівномірну за поширеністю дистрофію паренхіматозних структур. Переважно субендокардіально та в папілярних м’язах визначалися дистрофічно трансформовані кардіоміоцити аж до вакуолізації цитоплазми частини з них. Міжм’язові проміжки нерівномірно поширені за рахунок набряку інтерстицію та крововиливів.
При вивченні ультратонких зрізів тканини міокарда були виявлені наступні зміни (див. рис. 1).
Мітохондрії кардіоміоцитів з дещо підвищеною електронною щільністю, дезорганізовані, а саме, розпушені кристи внутрішньої мембрани. Частина мітохондрій містить значні ділянки електронно-світлих гомогенних мас. Саркоплазма має знижену електронну щільність внаслідок підвищеного вмісту рідини. Кількість рибосом та полісом знижена, у значній кількості наявні краплі ліпопротеїдів низької щільності. У саркомерах міофібрил Z-смуги не чіткі, а також порушена структурна орієнтація волокон актину та міозину. Сарколема, переважно, згладжена, а в окремих ділянках її електронна щільність підвищена. Каріотека ядер кардіоміоцитів на більшості ділянок дезорганізована, особливо тих, що прилягають до гіпертрофованого апарату Гольджі. Останній містить збільшену кількість розширених цистерн, мікроміхурців, первинних лізосом, мультивезикулярних тілець.
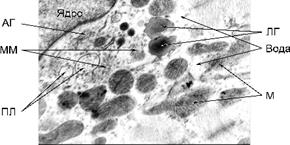
Рис. 1. Будова кардіоміоцита у морських свинок за умов гострої сироваткової хвороби (набряк мітохондрій та саркоплазми, релаксовані міофібрили): М – мітохондрії; ПЛ – первинні лізосоми; АГ – апарат Гольджі; ЛГ – ліпопротеїнові гранули; ММ – мікроміхурці; Зб. – Ч 21000
Отже, патогенний вплив на серце імунні комплекси здійснюють декількома шляхами. По-перше: активують систему комплементу, а по-друге звільняють численні біологічно активні речовини, які індукують надмірне пероксидне окиснення ліпідів. Недостатня активність антиоксидантного захисту призводить не лише до пригнічення окислювального фосфорилювання та гліколізу, а й до порушення структури і функції плазматичних та цитоплазматичних мембран, що в свою чергу спричинює порушення функції клітин, а можливо і їх загибель.
Питання терапії гострого імунокомплексного процесу є досить складним і суперечливим. Ми в експерименті намагалися оцінити вплив на цей процес тіотріазоліну (Т) та корвітину (К), попередньо дослідивши вплив цих препаратів на інтактний організм, щоб виключити можливий дисрегуляторний ефект на механізм імунної відповіді.
Було встановлено, що лише корвітин проявив
8-09-2015, 22:24
