Отримані результати досліджень статистично оброблені з використанням методів варіаційної статистики. Статистична обробка здійснювалася за допомогою програм “Exsel-2000” та “STATISTIKAforWindows” (StatsoftInc, США) на комп’ютері із процесором CPUAthlon 64-3200 Tray.
Результати досліджень та їх обговорення
Методом ПЛР у 100% обстежених хворихякісно виявлялася ДНК НВV.
Дослідження генетичної структури НВV у 76 хворих на ГГВ встановило, що у 71,1% випадків (54 особи) був виявлений генотип D, у 19,7% – генотип А (15 пацієнтів). Кількість хворих, у яких генотип вірусу встановити не вдалося, склала 9,2% (7 осіб). Серед65 хворих із середньотяжким перебігом ГГВ генотип D був встановлений у 67,7% (44 хворих), генотип А – у 21,5% (14 осіб), у 10,8% (7 осіб) генотип вірусу встановити не вдалося. При тяжкому перебігу ГГВ (11 хворих) генотип D HBV був виявлений у 90,9% (10 осіб), генотип А – у 9,1% (1 особа). Частота виявлення генотипів HBV у хворих на ГГВ та ХГВ представлена на рис.1.
При встановленні генетичної варіабельності HBV у 79хворих на ХГВ у 41,8% випадків (33 пацієнти)виявлявся генотип D, у 39,2% (31 пацієнт)– генотип А, генотип вірусу не вдалося встановити у 19% (15осіб). Із 67 хворих з мінімальною активністю ХГВ генотип D був встановлений у 44,8% (30 осіб), генотип А – у 34,3% (23 особи), у 20,9% (14 осіб) генотип вірусу встановити не вдалося. При слабковираженій активності ХГВ (12 пацієнтів) генотип DHBV був виявлений у 25,0% (3 особи), генотип А – у 66,7% (8 осіб), генотип не встановлено у 8,3% (1 особа).
Методом рестрикційного аналізу, досліджуючи субтипову характеристику НBV, було виявлено два генетичних варіанти генотипу DHBV (рис.2).
Серед 44 хворих з середньотяжким перебігом ГГВ I геноваріант генотипу D HBV був діагностований у 88,6% (39 осіб), тоді як ІІ геноваріант – у 11,4% (5 осіб). Із 10 хворих із тяжким перебігом ГГВ частота виявлення І геноваріанта становила 90% (9 осіб), II – у 10% (1 особа). При вивченні частоти геноваріантів генотипу D HBV у 33 хворих на ХГВ виявлено, що I геноваріант у хворих з мінімальною активністю процесу спостерігався у 96,7% (29 осіб), тоді як II геноваріант був виявлений у 3,3% (1 особа). Зі слабковираженою активністю ХГВ частота виявлення Iгеноваріанта становила 66,7% (2 пацієнти), II– у 33,3% (1 пацієнт).
Для виявлення можливих залежностей між генетичною структурою HBV та клінічними проявами хвороби нами проводилося порівняння частоти основних клінічних симптомів залежно від встановленого генотипу та геноваріанта вірусу у хворих на ГГВ та ХГВ.
У пацієнтів на ГГВ з генотипом А частіше зустрічався дискомфорт при пальпації в епігастрії – у 80%, тоді як у осіб з генотипом D – у 46,3% (р<0,05). Свербіж шкіри відзначався відповідно у 46,7% і 18,5% (р<0,05). У хворих з генотипом А частіше реєструвався диспепсичний синдром. При цьому важкість в ділянці правого підребер'я відзначалася у 100%, а у пацієнтів з генотипом D – у 75,9% (р>0,05), нудота – у 93,3% і 66,7% відповідно (р>0,05). При вивченні біохімічних показників (рівнів загального і прямого білірубіну, активності АлАТ) і тривалості стаціонарного лікування у хворих на ГГВ з різними генотипами HBV, статистичної вірогідності не встановлено, крім показників загального білка та протромбінового індексу, які у хворих з генотипом А були вірогідно меншими (68,9±3,2г/л, 70,5±2,1%), порівняно з відповідними показниками у хворих з генотипом D (79,5±2,9г/л, 79,8±1,3%) (р<0,05).
Порівнюючи частоту окремих клінічних проявів ГГВ залежно від встановленого геноваріанта генотипу D було виявлено, що у осіб з I геноваріантом генотипу D частіше зустрічалися диспепсичні прояви, зокрема нудота – у 91,7%, в той час, як у пацієнтів з II геноваріантом генотипу D– у 33,3% відповідно (р<0,05), тяжкість у правому підребер’ї відповідно у 100% і 16,7% (р<0,05). Такожу хворих на ГГВ з I геноваріантом генотипу D, на відміну від II геноваріанта, спостерігалися вірогідно вищі показники рівнів загального білірубіну та активності трансаміназ (р<0,05).
Нами вперше проводилося вивчення впливу різних генотипів вірусу на клінічні прояви ХГВ. Так, у хворих на ХГВ з встановленим генотипом А частіше спостерігалися зниження апетиту – у 96,8%, тоді як у осіб з генотипом D – у 39,4% (р<0,05), нудота – у 71% і 24,2% відповідно (р<0,05), тяжкість у правому підребер’ї – у 93,5% і 54,5% відповідно (р<0,05), тупий біль при пальпації у правому підребер’ї – у 61,3% і 18,2% відповідно (р<0,05). Крім того, у пацієнтів з генотипом А в періоді загострення хвороби вірогідно частіше зустрічалася жовтяниця, порівняно з хворими з генотипом D– 16,1% проти 3,03% (р<0,05). Аналізуючи біохімічні показники крові у хворих на ХГВ залежно від встановлених генотипів HBV виявлено, що рівні АлАТ були вищі у осіб з генотипом А – 2,9±0,8 ммоль/л·год проти 1,7±0,4 ммоль/л·год (р<0,05). Показники загального білірубіну теж були вищими у пацієнтів з генотипом А – 55,9±10,5 і 28,4±9,2 мкмоль/л відповідно (р<0,05), гамма-глобуліну – 31,4±2,6 г/л, проти 23,2±1,8 г/л при генотипі D (р<0,05), тоді як показники протромбінового індексу були вірогідно вищими у хворих на ХГВ з генотипом D – 72,2±3,1% проти 63,7±4,8% при генотипі А (р<0,05). При вивченні клініко-біохімічних особливостей у хворих на ХГВ залежно від геноваріантів генотипу D HBV достовірних результатів не отримано.
Активація імунної відповіді організму залежно від генетичної гетерогенності HBV вивчалася на основі аналізу синтезу прозапальних та протизапальних цитокінів у 36 хворих на ГГВ та у 54 на ХГВ. Серед обстежених хворих на ГГВ генотип А зустрічався у 41,7% (15 осіб), D – у 58,3% (21 особа). При цьому були виявлені деякі розбіжності в рівнях продукованих цитокінів: показники ІЛ-1β, ФНП-α та ІЛ-6 у хворих з генотипом А у розпалі ГГВ були більш високі порівняно з такими у хворих з генотипом D (рис.3А). Отримані концентрації відрізнялися статистичною вірогідністю, окрім ІЛ-6 (р>0,05). Рівні ІЛ-2 та протизапальних цитокінів ІЛ-4 і ІЛ-10 також були підвищені у групі хворих з генотипом А, але на відміну від прозапальних цитокінів їх показники не відрізнялися статистичною вірогідністю (р>0,05).
У подальшому, у періоді реконвалесценції (рис.3В), рівень ІЛ-1β у сироватці крові хоча і знижувався, але залишався більш високим у групі хворих з генотипом D – 159,1±9,1 пкг/мл, у хворих з генотипом А – 131,2±10,2 пкг/мл (р<0,05), тоді як концентрації ФНП-α і ІЛ-6 не відрізнялися вірогідністю у групах порівняння. У цьому ж періоді рівень ІЛ-2 залишався більш високим у хворих з генотипом D (р>0,05), на відміну від сироваткових концентрацій ІЛ-4 та ІЛ-10, що були більш високими у хворих з генотипом А: ІЛ-4 становив в середньому 98,8±10,2 і 70,2±11,0 пкг/мл; ІЛ-10 – 90,9±8,1 і 60,2±9,6 пкг/мл (р<0,05 в групах із різним генотипом НВV).
Досліджуючи синтез прозапальних та протизапальних цитокінів у 54 хворих на ХГВ залежно від генетичної варіабельності HBV (генотип А зустрічався у 51,9% (28 осіб), D – у 48,1% (26 осіб)) було встановлено, що як у періоді загострення, так і в періоді ремісії хвороби у пацієнтів з генотипом А рівні досліджуваних цитокінів були більш високі порівняно з такими ж у хворих з генотипом D (рис.4).

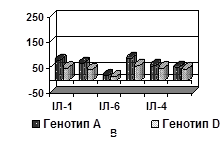
Рис. 1. Рівні досліджуваних цитокінів у хворих на ХГВ з різними генотипами НВV у періодах загострення (А) і ремісії (В)
Отримані показники ІЛ-1β (98,1±11,3 і 68,6±10,1 пкг/мл) та ФНП-α (79,4±6,0 і 60,7±5,2 пкг/мл) відрізнялися між собою статистичною вірогідністю в динаміці хвороби (р<0,05). Рівні ІЛ-6, регуляторного ІЛ-2 та протизапальних цитокінів ІЛ-4 і ІЛ-10 також були підвищені у групі хворих з генотипом А, але отримані результати не відрізнялися статистичною вірогідністю у групах порівняння в динаміці хвороби (р>0,05).
Аналізуючи показники цитокінемії у динаміці хвороби пацієнтів з різним ступенем тяжкості ГГВ було встановлено вірогідне підвищення рівнів прозапальних цитокінів у розпалі хвороби (рис.5А) як у хворих з середньотяжким, так і з тяжким перебігом хвороби порівняно з показниками контрольної групи (р<0,05). Так, у вищевказаному періоді рівень ІЛ-1β перевищував показники контролю в середньому у 6,5 раза у хворих з середньотяжким та у 8 разів – з тяжким перебігом; ФНП-α – у 5,8 та у 6,8 раза, ІЛ-6 перевищував у 4,7 та у 5,2 раза відповідно.
пкг/мл пкг/мл


Рис.2 Динаміка прозапальних та протизапальних цитокінів у хворих на ГГВ залежно від тяжкості перебігу у періодах розпалу (А) та реконвалесценції (В)
У періоді реконвалесценції ГГВ (рис.5В) спостерігалося вірогідне зниження показників прозапальних цитокінів як у хворих з середньотяжким, так і з тяжким перебігом, однак їх рівні ще продовжували перевищувати показники контролю: ІЛ-1β – у 4,3 і у 5,3 раза відповідно, ФНП-α – у 4 і 4,9 раза, ІЛ-6 – у 3,5 і 4,2 рази відповідно. Причому рівні ІЛ-1β та ФНП-α відрізнялися статистичною вірогідністю в групах порівняння із різним ступенем тяжкості ГГВ (р<0,05), окрім показників ІЛ-6 (р>0,05) та корелювали зі ступенем тяжкості ГГВ.
Активація регуляторного цитокіну ІЛ-2 у періоді розпалу ГГВ проявлялася вірогідним підвищенням його рівнів як у хворих з середньотяжким, так і з тяжким перебігом, що значно перевищувало контрольні значення – у 7,5 і 8,9 раза відповідно (р<0,05). У періоді реконвалесценції ГГВ показники ІЛ-2 у порівнювальних групах суттєво знижувалися, однак ще продовжували перевищувати контрольні значення, в середньому у 6,0 і 7,1 раза відповідно (р<0,05). Виявлена динаміка синтезу ІЛ-2 у хворих на ГГВ свідчить про активацію клітинної ланки імунітету у відповідь на втручання вірусного антигену, що в остаточному підсумку сприяло стабілізації інфекційного процесу та настанню реконвалесценції.
Синтез протизапальних цитокінів ІЛ-4 та ІЛ-10 у періоді розпалу ГГВ також підвищувалися у хворих досліджуваних груп з різним ступенем тяжкості, достовірно перевищуючи контрольні значення: ІЛ-4 – у 4,8 і 6,5 раза, ІЛ-10 – у 5,5 і 7,5 раза відповідно (р<0,05) (див. рис.5). В подальшому, у періоді реконвалесценції, показники ІЛ-4 та ІЛ-10 знижувалися, але продовжували перевищувати контрольні рівні: ІЛ-4 в середньому у 3,8 і 5,3 раза, ІЛ-10 – у 4,5 і 6,1 раза відповідно (р<0,05). Варто підкреслити, що середні рівні ІЛ-2, ІЛ-4 та ІЛ-10 у групах порівняння відрізнялися статистичною вірогідністю як у періоді розпалу, так і в періоді реконвалесценції хвороби та корелювали із ступенем тяжкості ГГВ (р<0,05).
Проведене дослідження синтезу прозапальних та протизапальних цитокінів у динаміці ХГВ з різною активністю процесу встановило, що порівняно з відповідними рівнями у хворих на ГГВ їх концентрації були значно нижчі. Так, у періоді загострення хвороби відмічено помірне вірогідне підвищення рівнів прозапальних цитокінів як у хворих з мінімальною, так і з слабковираженою активністю порівняно з показниками контрольної групи (рис.6А). Рівень ІЛ-1β у вищезазначений період перевищував показники контрольної групи в середньому у 2,8 раза у пацієнтів з мінімальною активністю та у 3 рази – з слабковираженою активністю, ФНП-α – у 2,2 і 2,6 раза, ІЛ-6 – у 2,4 і 2,7 раза відповідно (р<0,05).
У періоді ремісії ХГВ (рис.6В) спостерігалося незначне зниження рівнів прозапальних цитокінів як у хворих з мінімальною, так і з слабковираженою активністю процесу і їх показники продовжували перевищувати показники групи контролю: ІЛ-1β в середньому у 2,5 і 2,7 раза, ФНП-α – у 2,0 і 2,3 раза, ІЛ-6 – у 2,0 і 2,5 раза відповідно (р<0,05). Статистичної достовірності між отриманими показниками прозапальних цитокінів у групах хворих з різною активністю ХГВ у зазначені періоди встановлено не було (р>0,05).
У хворих у періоді загострення ХГВ активація регуляторного цитокіну ІЛ-2 була помірною (рис.6). Його показники у осіб з мінімальною активністю в середньому у 3,8 раза перевищували контрольні рівні, а у хворих з слабковираженою – у 3,5 раза (р<0,05), хоча достовірно не відрізнялися у групах порівняння з різною активністю ХГВ (р>0,05). У періоді ремісії рівні ІЛ-2 дещо знижувалися і продовжували перевищувати показники контрольної групи в середньому у 3,3 і 3 рази відповідно (р<0,05). Встановлена динаміка регуляторного цитокіну ІЛ-2 у хворих на ХГВ свідчить про низьку активацію клітинної ланки імунної відповіді на НВV, що призводить до неадекватності клітинного імунітету та подальшої персистенції вірусу.
Аналізуючи синтез протизапальних цитокінів при загостренні ХГВ відмічено вірогідне підвищення їх концентрацій як у хворих з мінімальною, так і з слабковираженою активністю процесу порівняно з відповідними рівнями у контрольній групі (див. рис.6). Так, показники ІЛ-4 перевищували рівні контролю, в середньому, у 4,4 раза у хворих з мінімальною та у 5,8 раза – з слабковираженою активністю ХГВ, ІЛ-10 – у 5,3 і 7 разів відповідно (р<0,05). У періоді ремісії ХГВ встановлено помірне зниження рівнів ІЛ-4 та ІЛ-10, однак їх показники продовжували перевищувати відповідні рівні контрольної групи: ІЛ-4 – у 4,0 і 5,5 раза, ІЛ-10 – у 4,9 і 6,3 раза відповідно (р<0,05). Слід відмітити, що показники рівнів ІЛ-4 та ІЛ-10 у групах порівняння з різною активністю ХГВ відзначалися статистичною вірогідністю і корелювали з ступенем активності запального процесу (р<0,05).
Отримані результати досліджень синтезу цитокінів у динаміці ГГВ у хворих з тяжким та середньотяжким перебігом хвороби відображають адекватну клітинно-гуморальну імунну відповідь організму, яка, частіше всього, призводить до елімінації вірусу з організму, і як наслідок, до реконвалесценції. Активація імунозапальних реакцій була більш вираженою у хворих з тяжким перебігом ГГВ і проявлялася високою поліклональною Т-хелперною клітинною відповіддю організму.
У хворих на ХГВ відмічено слабку активацію клітинно-гуморального імунітету, що проявлялося низьким синтезом досліджуваних цитокінів і вказує на імунологічну толерантність та неадекватність імунологічного реагування організму на HBV-інфекцію, що є домінуючою причиною вірусної персистенції. Крім того, зниження індукованої продукції ІЛ-2 у хворих із збільшенням активності ХГВ є однією з характерних ознак Т-клітинного імунодефіциту з переважанням у цих хворих синтезу цитокінів Т-хелперами 2-го типу, а саме ІЛ-4 та ІЛ-10, динаміка яких відображала активність запального процесу (р<0,05).
Проведений кореляційний аналіз встановив, що у періоді розпалу ГГВ виявляється помірна пряма кореляційна залежність між рівнем ІЛ-1β і ФНП-α у хворих з середньотяжким перебігом (r=0,45, р<0,05) та у групі хворих з тяжким перебігом (r=0,49, р<0,05). Більш виражений кореляційний зв'язок було встановлено у цей період між рівнем ІЛ-1β та ІЛ-2, який у пацієнтів з тяжким перебігом хвороби складав r=0,52, (р<0,05) і з середньотяжким – r=0,48, (р<0,05). У подальшому, у періоді реконвалесценції ГГВ, кореляційний зв´язок між даними прозапальними цитокінами тіснішав, що вказувало на спад інфекційного процесу у досліджуваних групах (ІЛ-1β/ФНП-α – r=0,56 (т), r= 0,53 (с-т); ІЛ-1β/ІЛ-2 – r=0,61 (т), r=0,58 (с-т); р<0,05). У хворих на ГГВ кореляційні зв’язки між ІЛ-1β та ІЛ-6 були слабкими та недостовірними в обох групах порівняння в динаміці хвороби. Проявом стимулюючого впливу ФНП-α на ІЛ-6 є виявлена пряма помірна кореляція між рівнями даних цитокінів у періоді розпалу ГГВ (r=0,41, р<0,05). Крім того, у періоді розпалу ГГВ нами встановлена пряма помірна кореляційна залежність між рівнем ІЛ-1β та АлАТ (r=0,6, р<0,05), між ІЛ-1β та рівнем загального білірубіну (r=0,51, р<0,05) та помірна зворотня кореляція між ФНП-α та рівнями протромбінового індексу (r=-0,42, р<0,05). Аналіз динаміки синтезу протизапальних цитокінів ІЛ-4, ІЛ-10 та прозапального ІЛ-1β у хворих на ГГВ дає можливість стверджувати про наявність прямого помірного кореляційного зв’язку між ними, що підтверджує здатність організму компенсувати дії прозапальних цитокінів. Так, у періоді розпалу ГГВ коефіцієнт кореляції між досліджуваними показниками складав: між ІЛ-1β та ІЛ-4 r=0,42 (р<0,05), ІЛ-1β та ІЛ-10 r=0,44 (р<0,05) і між ІЛ-2 та ІЛ-4 r=0,48 (р<0,05). Таким чином, пошук взаємозв’язків між досліджуваними показниками цитокінового профілю та проявами клініко-патогенетичних синдромів у хворих на ГГВ дозволив виявити існування помірної достовірної корелятивної залежності між ними (rs=0,44, р<0,05).
При встановленні кореляційних зв’язків у хворих на ХГВ з різною активністю запального процесу у періоді загострення був виявлений помірний прямий кореляційний зв'язок між рівнем ФНП-α та АлАТ (r=0,42, р<0,05), та слабкий кореляційний зв'язок між показниками ІЛ-1β та АлАТ (r=0,37, р<0,05). Тісніші кореляційні зв’язки виявлялися між ІЛ-4 та АлАТ (r=0,51, р<0,05) та ІЛ-10 та АлАТ (r=0,53, р<0,05). Крім того, у зазначеному періоді ХГВ відзначалися тісніші прямі кореляційні залежності між показниками протизапальних цитокінів та проявами мезенхімально-запального синдрому: ІЛ-4/гамма-глобуліну r=0,56, р<0,05; ІЛ-10/ гамма-глобуліну r=0,59, р<0,05, які певною мірою відображають ступінь дисфункції печінки. Взаємозв'язок між цими параметрами є проявом активації гуморальної ланки імунітету у хворих на хронічні форми HВV-інфекції і може свідчити про залежність гіперфункції гуморального імунітету і ступеня активності хвороби від тривалості хронічного гепатиту. Слід окремо зазначити, що у періоді загострення ХГВ, аналізуючи у хворих кореляційні залежності між вмістом ІЛ-2 та рівнями протизапальних цитокінів, була встановлена слабка зворотня кореляція: між ІЛ-2/ІЛ-4 r=–0,31 (р<0,05) та між ІЛ-2/ІЛ-10 r=–0,33 (р<0,05), що підтверджує
8-09-2015, 19:39
