Таблиця 1
Властивості виробничого штаму ВК–1М ВД
| Показники | Необхідні параметри | ||
| матраси | бутлі | ||
| Оптимальна доза зараження | співвідношення об’єму вірусу й підтримуючого середовища | 1:20 | 1:30 |
| Інфекційна активність вірусу в заражаючій дозі | ТЦД 50 /см3 | 1000 | 1000 |
| Множинність зараження | ТЦД50 /клітину | 0,01 | 0,01 |
| Час репродукції в моношаровій культурі клітин КСТ за ролерного культивування | годин | 40 | 40 |
| Титр інфекційності вихідної сировини | lg ТЦД 50 /см3 | 6,6 | 7,6 |
Після відпрацювання технології культивування й накопичення біомаси вірусу діареї ми здійснили дослідження щодо її звільнення від клітинного детриту.
Як засвідчили результати цих досліджень, виконаних на моделі штаму ВК–1М вірусу діареї, осадження клітинного детриту за методом спонтанної седиментації й центрифугування за 2500 g упродовж 30–ти хвилин забезпечувало відповідно отримання прозорої вірусовміщуючої рідини на 34–35 і 44–45 % порівняно з дистильованою водою (табл. 2).
У той же час очистка не впливала на інфекційну активність вірусу, яка залишалася фактично на одному рівні як до, так і після видалення клітинного детриту шляхом седиментації та центрифугування, й становила відповідно 7,55 і 7,6 lg ТЦД 50 /см3 .
Таблиця 2
Порівняльна оцінка способів очистки вірусу діареї M±n, n=3
| Спосіб очистки | Ступінь очистки за прозорістю,% | Кількість білка, мкг/см3 | Титр інфекційності, lg ТЦД50 /см3 | ||
| до очистки | після очистки | до очистки | після очистки | ||
| Седиментація | 34–35 | 2185 | 1845 | 7,60±0,15 | 7,55±0,25 |
| Центрифугування | 44–45 | 2185 | 1148 | 7,60±0,15 | 7,60±0,10 |
Однак отримані дані свідчать про те, що центрифугування за 2500 g протягом 30‑ти хвилин сприяє більш швидкому та ефективному очищенню вірусовмісної суспензії від клітинного детриту й загального білка, на підставі чого в подальшому застосовували цей метод під час виготовлення дослідних зразків живої вакцини проти вірусної діареї, хоча цей спосіб є більш затратним порівняно із седиментацією, що впливає на собівартість препарату.
Вивчення антигенних властивостей виробничого штаму ВК–1М вірусу діареї. Відомо, що в процесі конструювання вакцинних препаратів на основі атенуйованих штамів вірусу важливим є визначення їхніх антигенних властивостей. Здатність атенуйованого штаму ВК-1М вірусу діареї, обраного нами як виробничий, індукувати в організмі тварин вірусоспецифічні антитіла вивчалась у порівняльному аспекті із штамами 25 і Oregon C 24 V як можливими компонентами для створення вакцини. Дослід здійснено на кроликах, які були сформовані в групи по 5 голів з розрахунку на штам вірусу діареї, який вводили одноразово внутрішньом’язово у відповідній дозі, а саме: Oregon C 24 V – 2Ч105,7 і 2Ч107 ТЦД50 /гол., 25 – 2Ч105,7 і 2Ч107 ТЦД50 /гол. і ВК-1М – 2Ч106,6 і 2Ч107,6 ТЦД50 /гол. відповідно першого та п’ятого їх пасажів у культурі клітин.
Установлено, що як у першому, так і в п’ятому пасажах у культурі перещеплюваних клітин КСТ досліджувані штами зберігають здатність індукувати в організмі кроликів вірусонейтралізуючі антитіла, які виявлялися вже на 7 добу після введення та фактично утримувалися на одному рівні до 14 доби (термін спостереження) у титрах 6,0–6,7 lоg2 і 6,3–6,8 lоg2 . Отримані дані свідчать про антигенну стабільність досліджуваних штамів, зокрема атенуйованого штаму ВК‑1М, як у процесі адаптації до нових умов культивування, так і в пасажах у перещеплюваній культурі клітин КСТ.
Конструювання живої вакцини проти вірусної діареї великої рогатої худоби. Для виготовлення вакцини використовували культуральну суспензію, отриману в результаті репродукції штаму ВК–1М вірусу діареї в моношаровій культурі клітин КСТ, вирощеній у ролерних 3-літрових бутлях. Після одноразового заморожування – відтавання вірусовміщуючу суспензію центрифугували 30 хвилин за 2500 g для видалення клітинного детриту й визначали інфекційний титр шляхом зараження моношарової культури клітин десятикратними розведеннями вірусу. Титр інфекційної активності вірусу в цій культурі був на рівні 7,6 ± 0,1 lg ТЦД50 /см3 .
Нами було виготовлено два дослідних зразки вакцини, один з яких був висушений методом ліофілізації в умовах ННЦ «ІЕКВМ». У процесі виготовлення ліофілізованого зразка вакцини використовували захисне середовище, яке готували з рівних об’ємів 50 % сахарози і 25 % желатину, після змішування яких із вірусовміщуючою культуральною суспензією у співвідношенні 1:9 кінцева концентрація становила 5,6 % і 2,8 %, відповідно. Під час вивчення інфекційної активності встановлено, що в процесі ліофілізації вона зменшувалася на 2,15 lg ТЦД50 /см3 порівняно з вихідним показником (табл. 3). Проте антигенна активність вірусу не змінювалася. Титри вірусонейтралізуючих антитіл у пробах сироватки крові, відібраної у кроликів через 7 і 14 діб після щеплення досліджуваних зразків рідкої та сухої вакцин, були фактично однаковими (6,5 ± 0,2 і 6,3 ± 0,3 log2 ).
Таблиця 3
Вплив ліофілізації вакцини на інфекційність та антигенну активність вакцинного вірусу діареї n=3
| Зразок вакцини | Титр інфекційності, lg ТЦД50 /см3 | Титр ВН-антитіл, log2 (М±м) | |
| 7 діб | 14 діб | ||
| Рідка (нативна) | 7,6±0,1 | 6,2±0,1 | 6,5±0,2 |
| Ліофілізована | 5,45±0,3 | 6,0±0,2 | 6,3±0,3 |
Вивчення вакцини за показниками якості. Кожний зразок вакцини (рідкої і сухої) проти ВД ВРХ перевіряли на контамінацію сторонніми мікроорганізмами, нешкідливість, антигенну та імуногенну активність. Контроль на контамінацію бактеріями та грибами здійснювали відповідно до ГОСТ 28085-89 «Препараты биологические. Метод контроля стерильности» та згідно з ДСТУ 4483:2005 «Препарати ветеринарні імунобіологічні. Методи визначення бактеріальної і грибкової контамінації». Проростів у вигляді помутніння, змін кольору або газоутворення в інокульованих бактеріологічних середовищах не спостерігали у всіх трьох послідовних пасажах досліджуваних проб, що свідчило про відсутність забрудненості бактеріями й грибами. Контамінацію досліджуваних зразків вакцини мікоплазмами виключали за результатами висівів у середовище Едварда. У трьох послідовних пересівах кожного зразка вакцини в напіврідкому агарі не виявлено завислих, напівпрозорих, у вигляді крапель, а на напівтвердому агарі - росту випуклих соскоподібних колоній мікоплазм.
З урахуванням вимог Європейських стандартів здійснювали контроль вакцини на контамінацію сторонніми вірусами. Відсутність ЦПД у моношаровій культурі клітин у трьох послідовних пасажах суміші вірусу діареї й специфічної сироватки крові вказувало на те, що дослідні зразки були вільними від сторонніх цитопатогенних вірусів.
Нецитопатогенні віруси визначали за методом гемадсорбції. У жодному випадку не спостерігали адсорбцію еритроцитів морської свинки на моношарі клітин, які попередньо інокулювали сумішшю вакцини й специфічної до вірусу діареї сироватки крові.
Отже, розроблена технологія забезпечувала накопичення вихідної вірусовміщуючої культуральної суспензії з високою інфекційністю та виготовлення сухої форми вакцини, не контамінованих сторонніми мікроорганізмами.
Вивчення реактогенності вакцини. Реактогенність виготовлених зразків вакцини проти вірусної діареї, виготовлених із штаму ВК-1М, вивчали в дослідах на кроликах. Зразки середніх проб рідкої та сухої культуральної вакцин вводили підшкірно в об’ємі 2 мл, що відповідало 2Ч107,6 і 2Ч105,45 ТЦД50 /гол., дворазово з інтервалом у 14 діб. У кроликів, щеплених сухим зразком вакцини із штаму ВК-1М і вірусовміщуючою культуральною суспензією штамів 25, Oregon C 24 V, не спостерігали відхилень від нормального клініко-фізіологічного стану, температура тіла була в межах норми.
За результатами гематологічних досліджень у тварин, яким вводили культуральну суспензію штамів 25 і Oregon C 24 V, установлено деяке зниження кількості лейкоцитів у межах 0,5–0,6 тисяч/мм3 , а починаючи від 14 доби вона поступово поновлювалась і на 24 добу після щеплення сухої вакцини чи то вірусовміщуючої суспензії досліджуваних штамів 25 і Oregon C 24 V досягала вихідних показників.
Збільшення кількості нейтрофілів супроводжувалося підсиленням фагоцитарної реакції у кроликів у перші доби і її зменшенням та послабленням фагоцитарної реакції на 7–14 доби після щеплення сухого зразка вакцини із штаму ВК–1М і вірусовміщуючої культуральної суспензії штамів 25 і Oregon C 24 V.
У кроликів, яким щепили сухий зразок вакцини проти вірусної діареї зі штаму ВК‑1М, ці показники були виражені менше. Фагоцитарне число та фагоцитарний індекс у цих тварин знижувалися лише на 4,4 % і 0,4 одиниці порівняно з вихідними показниками, що свідчить про слабко виражену реактогенність вакцини з атенуйованого штаму ВК–1М вірусу діареї, тим більше, що він не призводив до проявлення вираженої лейкопенії.
Перевірка нешкідливості сухого зразка вакцини проти вірусної діареї. Нешкідливість вакцини культуральної живої проти вірусної діареї перевірялася на білих мишах і серонегативних до вірусу діареї телятах. Установлено, що вона нешкідлива для піддослідних тварин, у яких у місцях введення препарату не виявлено набряку, припухлості, затвердіння тканин або болісної реакції при пальпації. За підшкірного введення білим мишам вакцини в дозі 0,2Ч105,45 ТЦД50 /гол. під час спостереження впродовж 14 діб (інтервал між дворазовим щепленням вакцини) не спостерігали відхилення у їх загальному стані. У той же час у телят 5‑кратна доза (10Ч105,45 ТЦД50 /гол.) вакцинного вірусу викликала незначне зниження кількості лейкоцитів. Зокрема, у теляти, в якого було виявлено одноразове підвищення температури тіла (на другу добу увечері) на 1 °С, кількість лейкоцитів понизилась від 7180±96 до 6685±114 кл./мм3 (на 495 кл./мм3 ), а в теляти, в якого не встановлено температурної реакції, від 7768±123 до 7463±110 (на 305 кл./мм3 ), що підтверджує слабку реактогенність вакцинного вірусу.
Перевірка антигенної активності вакцини. Антигенну активність сухого зразка вакцини вивчали на кроликах, з яких формували 3 групи по 5 голів у кожній. Вакцину вводили одноразово в дозах 2Ч105,45 ТЦД50 /гол. і 5Ч105,45 ТЦД50 /гол. внутрішньом’язово кроликам першої та другої груп відповідно. А третя група залишалась інтактним контролем.
Установлено залежність рівня продукованих вірусонейтралізуючих антитіл від дози (об’єму) щепленої вакцини. Так, у кроликів другої групи, яким вводилася вакцина в дозі 5Ч105,45 ТЦД50 /гол., титр вірусоспецифічних антитіл уже на 7 добу був вищим на 1,0 log2 порівняно з показниками у тварин, щеплених вакциною в дозі 2Ч105,45 ТЦД50 /гол., хоча в подальшому процесі імунної відповіді титри антитіл до вакцинного вірусу діареї фактично вирівнювалися. На підставі отриманих даних зроблено висновок, що досліджуваний зразок сухої вакцини є антигенно активним.
Вивчення імуногенних властивостей вакцини живої проти вірусної діареї. Як повідомляють Сюрин В. Н. із співавт. (1983), ІРТ, ПГ–3 і ВД з характерними клінічними ознаками неможливо відтворити в експерименті в лабораторних умовах. У зв’язку з цим імуногенність, а також захисні властивості вакцинних препаратів прийнято оцінювати за їхньою антигенною активністю. На підставі зазначеного ми вивчали показники специфічного та неспецифічного імунітетів у щеплених вакциною тварин. На першому етапі цих досліджень зразки вакцини були випробувані на морських свинках, для чого було сформовано 4 групи по 10 голів у кожній. У процесі вивчення імуногенної активності вакцини, виготовленої з атенуйованого штаму ВК‑1М ВД ВРХ, на морських свинках підтверджено високу антигенність. Вакцина викликала активну індукцію специфічних вірусонейтралізуючих антитіл. У той же час вакцина у випробуваних дозах була нешкідливою для морських свинок, серед яких не спостерігали захворювання або загибелі. У морських свинок вже на 7 добу після введення вакцини в дозах 0,5 і 1,0 см3 одно- і дворазово титр вірусонейтралізуючих антитіл був на рівні 4,33; 5,75 і 5,5 log2 , поступово зростаючи на 14 добу до 5,45; 6,7 і 5,75 log2 відповідно. Після повторного введення вакцини спостерігали подальше зростання титрів вірусонейтралізуючих антитіл до 6,4 і 7,3 log2 відповідно, у той час як після одноразового введення їх титр фактично залишався на попередньому рівні (5,8 log2 ).
На підставі отриманих результатів з визначення антигенної активності сухого зразка вакцини на кроликах та вивчення імуногенної активності вакцини на морських свинках була підтверджена значущість дози і необхідність дворазового застосування вакцини живої проти ВД, що сприяло підвищенню титрів вірусонейтралізуючих антитіл. Отримані позитивні результати щодо нешкідливості та імуногенності для лабораторних тварин дозволили нам здійснити її випробування на сприйнятливих до вірусної діареї тваринах в умовах неблагополучного господарства. Враховуючи ті обставини, що вірус діареї є досить потужним імуносупресором і в організмі здатний пригнічувати імунологічну реактивність, перед тим, як застосувати вакцину живу проти ВД на ВРХ, ми випробували імуномодулятор з культури Bacіllus alvei.
Вивчення імуномоделюючої активності ліпополісахариду з Bac. аlvei. Як відомо, бактеріальні ліпополісахариди є поліклональними активаторами В-системи лімфоцитів (Карпуть І. М., 1993) і суттєво стимулюють неспецифічні гуморальні та клітинні ланки імунної системи (Дранкин Г. Н. и др., 1994). А якщо взяти до уваги, що фактично більша кількість скотарських господарств є неблагополучними щодо вірусної діареї, то під час застосування живої вакцини, хоча і з атенуйованого штаму, на можливо інфікованому поголів’ї не виключаються випадки біотичної взаємодії вакцинного та епізоотичного штамів вірусу і негативний вплив утворених рекомбінацій вірусу на імунну систему щеплених тварин. З урахуванням цих обставин, а також з метою пом’якшення імуносупресивної дії вірусу діареї ми використали ліпополісахарид з культури Bacіllus alvei.
Токсичність бактеріального ліпополісахариду визначали на білих мишах (по 10 голів на пробу), яким перорально вводили 0,5 см3 (162,5 мг ЛПС–1), 1 см3 (325 мг ЛПС‑1) і 2 см3 (650 мг ЛПС‑1), що становило відповідно 8,125; 16,25 і 32,5 мг/г маси тіла миші. Під час нагляду впродовж 10 діб не було виявлено змін у загальному стані піддослідних мишей, у тому числі й контрольної групи. У групі мишей, яким підшкірно вводили 0,5 мл ЛПС–1, у місцях ін’єкцій препарату не спостерігали ні набряків, ні інших локальних змін. Отримані результати засвідчили, що виготовлений ЛПС‑1 нетоксичний як за перорального, так і підшкірного введення тваринам, у яких не встановлено клініко-фізіологічних порушень у загальному стані. Миші залишалися здоровими. На підставі цих даних було проведено дослід на кроликах з метою вивчення імуномоделюючих властивостей ЛПС-1, результати якого оцінювали за трансформацією та функціональною активністю мононуклеарних попередників макрофагів, зокрема макрофагальною трансформацією мононуклеарів периферичної крові, показниками фагоцитарного індексу та фагоцитарного числа. Установлено, що ЛПС‑1 здатний підвищувати трансформативну активність попередників макрофагів, яка зростала в 1,5 рази.
Отже, результати вивчення властивостей виготовленого ЛПС‑1 свідчать про те, що він є нешкідливим для тварин, має виражені стимулюючі властивості.
З метою визначення оптимальної дози ЛПС‑1, яка б забезпечувала активізацію імунної відповіді, здійснено подальші досліди на 6 групах кроликів (по 5 голів у кожній), яким вводили внутрішньом’язово препарат у дозах 1, 2, 5, 7 і 10 мкг/кг маси тіла тварин. Нагляд за піддослідними тваринами здійснювали впродовж 14 діб. Контрольній групі вводили фізіологічний розчин.
Установлено, що ЛПС‑1 активізує ланки клітинного імунітету. Імуномодулююча дія ЛПС‑1 виявлялась уже на 7 добу в тварин усіх груп, які отримували препарат незалежно від його дози, але різною мірою щодо реакції імунокомпетентних клітин. Найбільш виражена стимулююча активність ЛПС‑1 спостерігалася у групах кроликів, які отримували 5 і 7 мкг препарату з розрахунку на кілограм маси тіла. Зокрема стабільно й достовірно підвищувалася фагоцитарна активність, де фагоцитарне число й фагоцитарний індекс зростали до 9,05–9,08 і 9,05–10,45 одиниць відповідно проти 4,46 (у середньому) в контролі. Ці показники стимулювання імунокомпетентних клітин були близькими до результатів дії ЛПС‑1 у дозі 10 мкг/кг маси тіла кроликів. Виходячи з цього, було визнано доцільним застосування ЛПС‑1 у дозі 7 мкг/кг маси тіла тварини.
Отже, результати визначення оптимальної дози ЛПС‑1 дозволили встановити, що цей препарат може застосовуватися із розрахунку 7 мкг/кг маси тіла для підвищення резистентності організму тварин і стимуляції післявакцинального імунітету.
Вивчення імуногенності вакцини живої культуральної проти вірусної діареї на телятах. Імуногенність вакцини живої культуральної з атенуйованого штаму ВК‑1М вірусу діареї вивчали на телятах у неблагополучному щодо вірусної діареї дослідному господарстві «Українка Слобідська» згідно з наказом директора ІЕКВМ УААН № 7-б від 20 січня 2004 року.
Випробування запропонованої вакцини здійснювали за методикою, що була розглянута й схвалена методичною комісією ІЕКВМ УААН (протокол № 1 від 2 лютого 2004 року), згідно з якою в господарстві було сформовано 5 груп телят 3–4-місячного віку (по 5 голів у кожній). До застосування вакцини в телят усіх дослідних груп виявлені специфічні до вірусу діареї антитіла в титрах від 3,5 до 4,5 log2 (рис. 1).
Першій групі телят вакцину щепили внутрішньом’язово дворазово з інтервалом у 14 діб у дозі 2Ч105,45 ТЦД50 /гол., а другій – 5Ч105,45 ТЦД50 /гол., що відповідно містились у щепних об’ємах 2 і 5 см3 . Телятам третьої групи вакцина в дозі 2Ч105,45 ТЦД50 /гол. була введена одночасно з ЛПС-1 із розрахунку 7 мкг/кг маси тіла тварин. Телята четвертої групи отримували лише ЛПС-1 у дозі 7 мкг/кг маси тіла. П’ята група телят була контрольною, якій ні вакцина, ні ліпополісахарид не щепили. Отримані дані свідчать про те, що вакцина позитивно впливала на динаміку імунної відповіді незалежно від вихідної серопозитивності телят до її застосування.
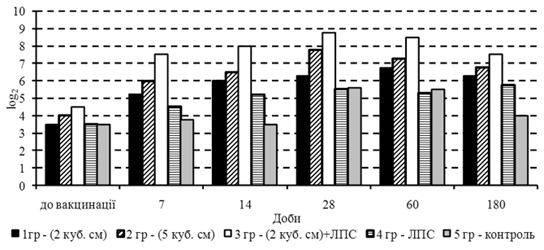
Рис. 1. Динаміка специфічних антитіл у телят, щеплених вакциною проти вірусної діареї в комплексі з ЛПС-1
Інтенсивність приросту титрів специфічних до вакцинного вірусу антитіл у телят залежала від щепної дози. Так, на 7 добу після введення вакцини в дозах 2 і 5 см3 /гол. їх титр зростав на 1,75 і 2,0 log2 відповідно, а на 28 добу він був вищим на 2,8 і 3,75 log2 порівняно з вихідним (3,5 і 4,0 log2 ).
Застосування ліпополісахариду суттєво підсилювало приріст титру антитіл за одночасного щеплення вакцини в дозі 2Ч105,45
ТЦД50
/гол. у середньому на 2,0 log2
відносно титрів антитіл у разі застосування однієї вакцини в цій дозі. Перевагу застосування вакцини в комплексі з ЛПС-1 підтверджено також стабільним утриманням високого рівня титру специфічних антитіл упродовж 60 діб з поступовим зниженням його до 7,5±0,23 log2
на 180 добу, а також даними щодо титру нейтралізуючих антитіл у разі застосування однієї вакцини в дозі 5Ч105,45
ТЦД50
/гол., де він був у
8-09-2015, 23:45
