скорость обратного процесса:
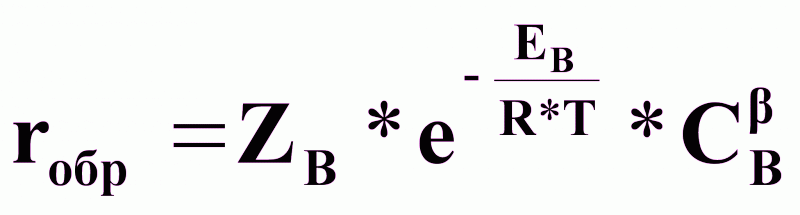 (3б).
(3б).
Уравнение гидродинамики процесса.
Уравнение гидродинамики процесса характеризует давление в потоке как сложную функцию:
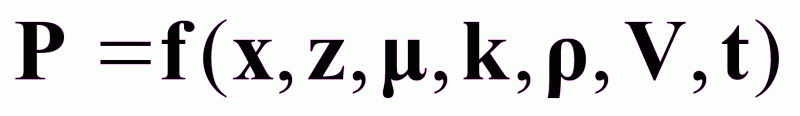 (4)
(4)
где
x, z - координаты потока;
- ламинарная вязкость, характеризующая силы внутреннего трения;
k - турбулентная вязкость;
- плотность реакционной массы;
V - объем реакционной массы;
t - текущее время.
Материальный баланс реакторного процесса
по всему веществу.
Уравнение динамики:
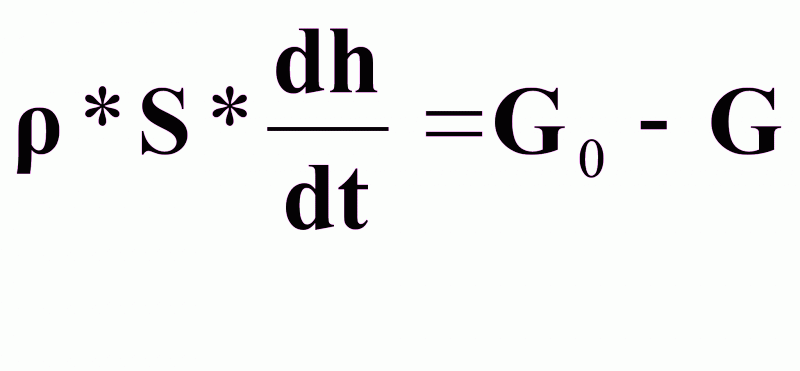 (1),
(1),
где
Уравнение
статики при
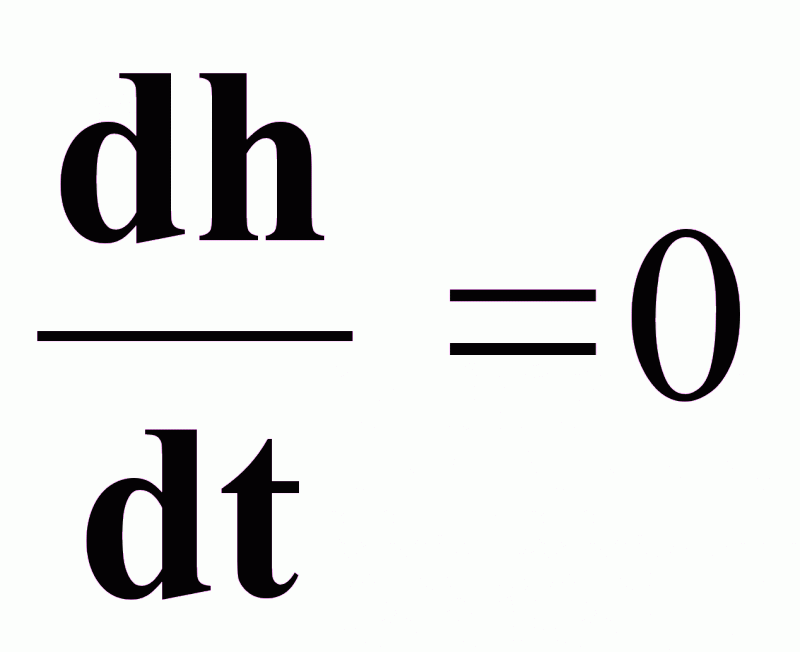 :
:
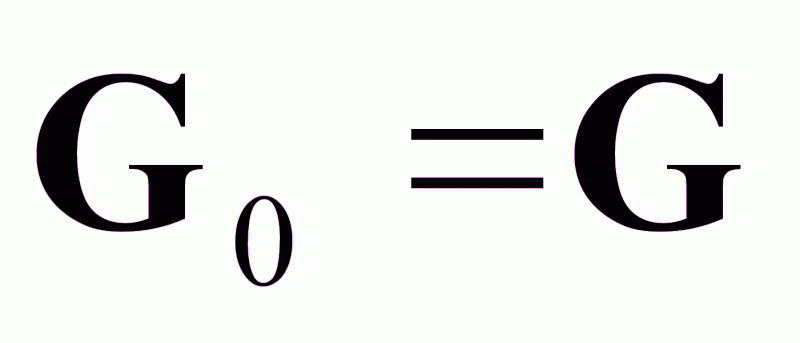 (2).
(2).
На основе(1) и (2):
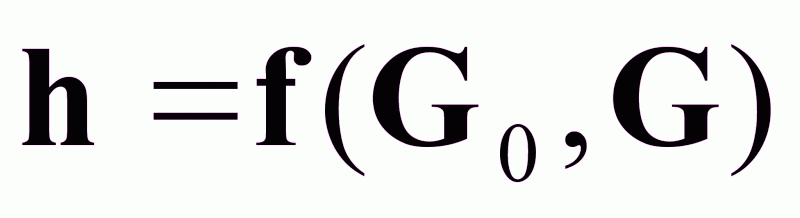 (3).
(3).
Материальный баланс реакторного процесса
по расходуемому веществу А.
Уравнение динамики:
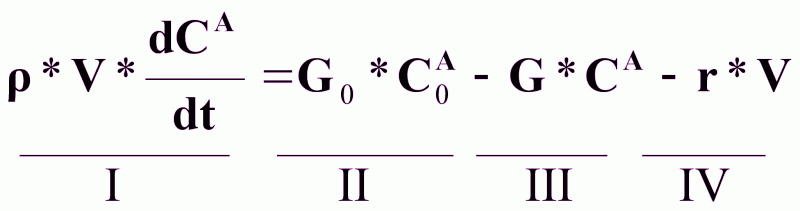 (4),
(4),
где
I - изменение количества вещества А в реакторе в единицу времени;
II - количество вещества А, поступающего в реактор в единицу времени;
III - количество вещества А, отводимого из реактора в единицу времени;
IV - количество вещества А, расходующегося в реакторе на химическую реакцию в единицу времени, где V=S*h.
Уравнение
статики при
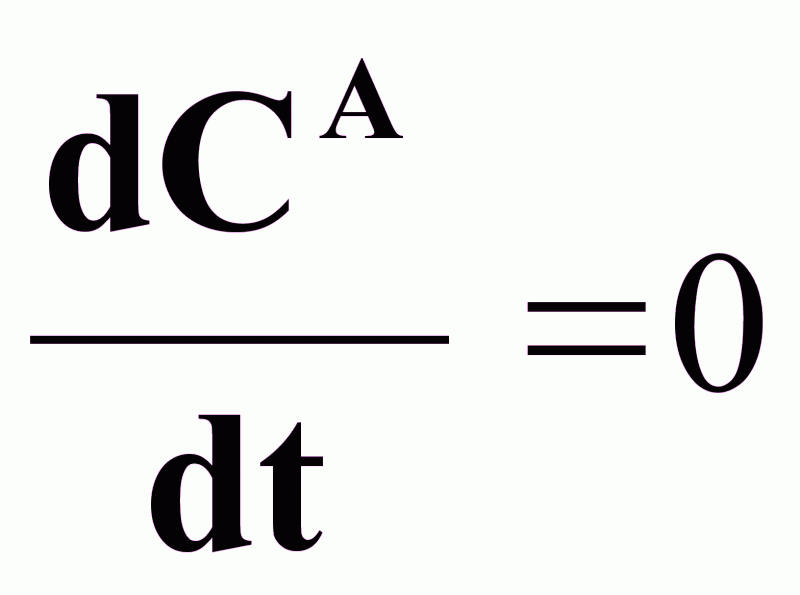 :
:
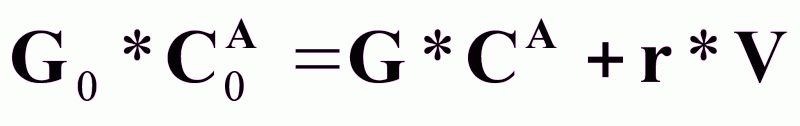 (5).
(5).
На основе (4) и (5):
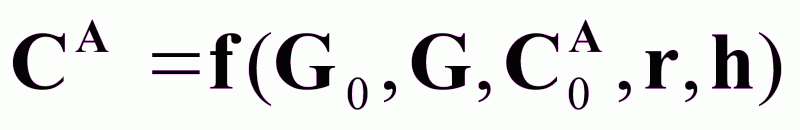 (6).
(6).
Тепловой баланс реакторного процесса.
Уравнение динамики:
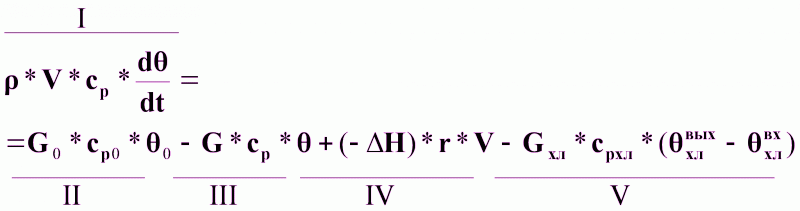 (7),
(7),
где
I - изменение количества тепла в реакторе в единицу времени;
II - количество тепла, поступающего в реактор с исходным реагентом в единицу времени;
III - количество тепла, отводимого из реактора с реакционной массой в единицу времени;
IV - количество тепла, выделяющегося в реакторе в результате химической реакции в единицу времени;
V - количество тепла, отводимого из реактора с хладоагентом в единицу времени.
Уравнение
статики при
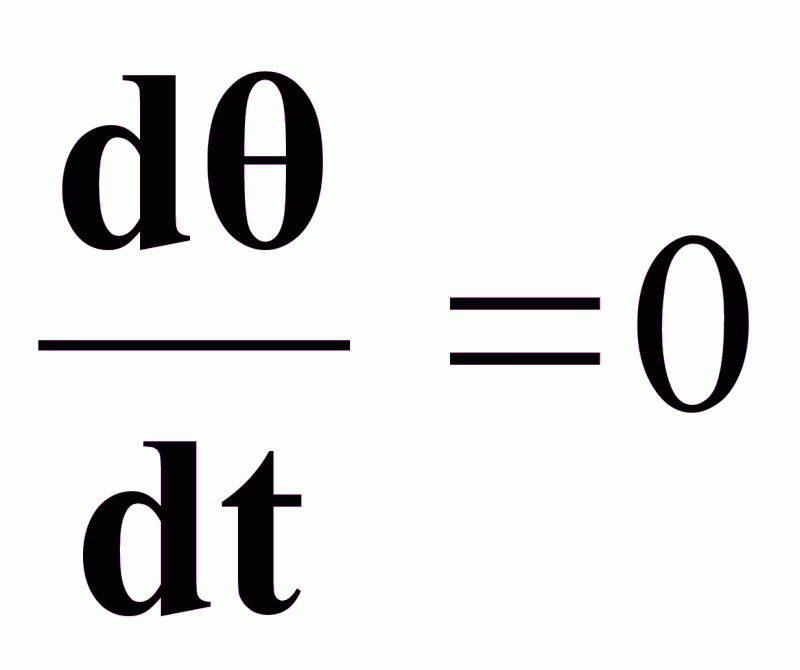 :
:
![]() (8).
(8).
На основании (7) и (8):
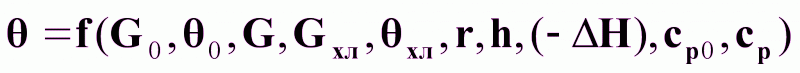 (9).
(9).
Информационная схема реактора на основе балансовой модели.
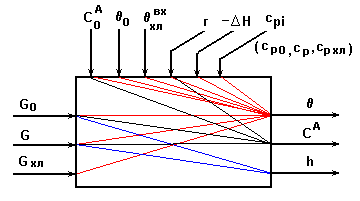
Рис.6.1.
Возможные управляемые переменные:
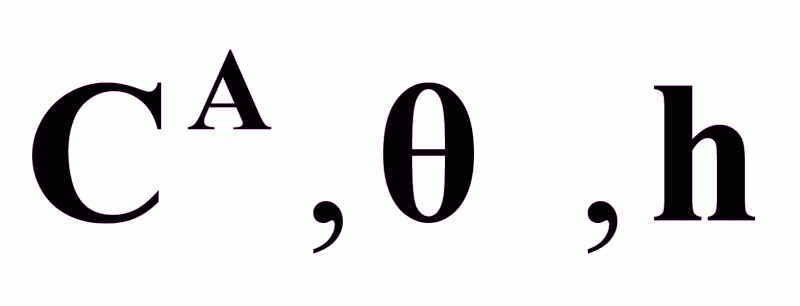 .
.Возможные управляющие воздействия:
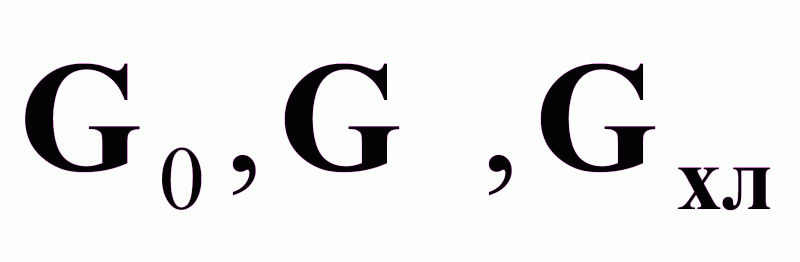 .
.Возможные контролируемые возмущения:
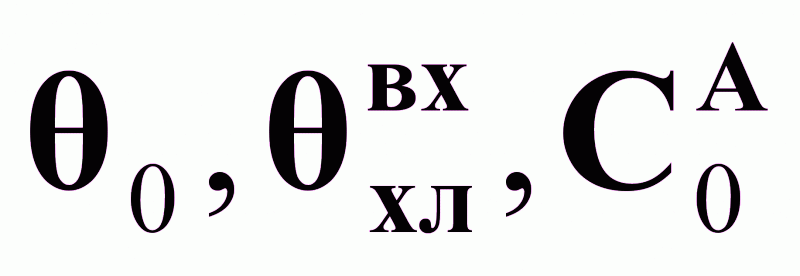 .
.Возможные неконтролируемые возмущения:
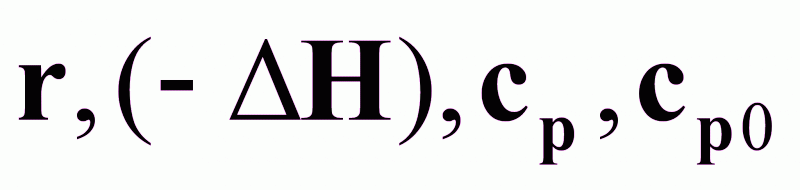 .
.
8. Материалы к лекции №16
Автоматизация реакторных процессов (ч.2)
Диаграмма
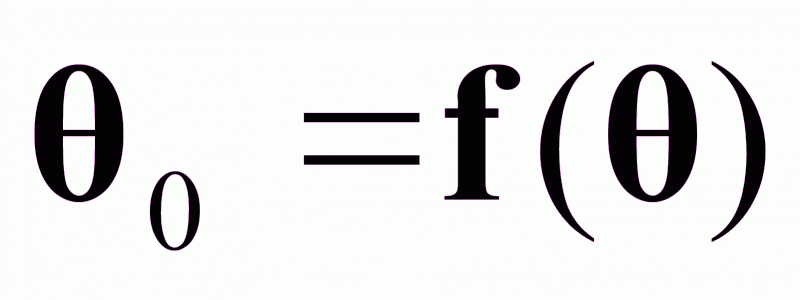
реакторного процесса в адиабатическом режиме.
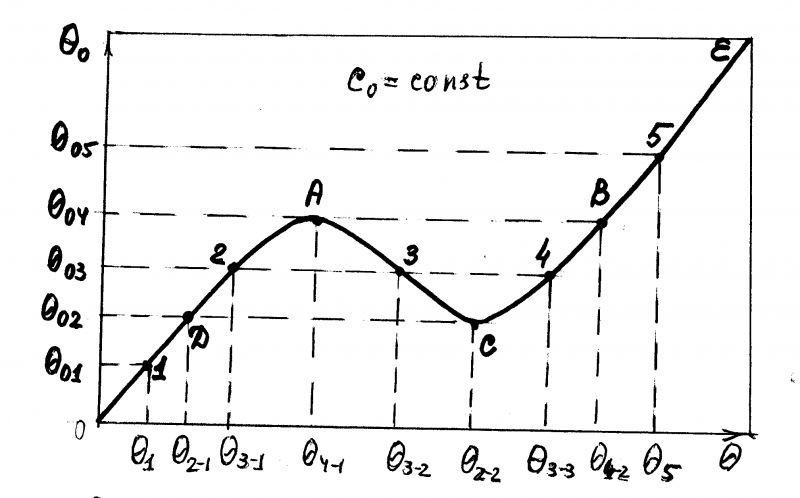
Рис.1.1.
Влияние изменения температуры 0 на температуру реакторного процесса .
При изменении входной температуры 0 в пределах от 02 до 04 работа реактора осуществляется по петле гистерезиса D-A-B-C-D.
Участок статической характеристики А-3-С - путем изменения входной температуры не реализуется.
Возможные стационарные состояния реактора.
При 01 - одно устойчивое состояние в ()1, но температура в реакторе низкая и реакция идет слабо.
При 02 - два стационарных состояния в ()D и ()С:
()D - устойчивое состояние, но при низкой температуре;
()С - неустойчивое состояние с возвратом в ()D при уменьшении начальной температуры.
При 03-три стационарных состояния в ()2, ()3, ()4:
()2 - устойчивое состояние, но с низкой скоростью реакции;
()4 - устойчивое состояние, почти полное превращение реагентов, но реакция идет с высокой температурой – вне рабочего диапазона;
()3 - изменением начальной температуры не реализуется.
При 04 - два стационарных состояния в ()А и ()В:
()А - неустойчивое состояние, с проскоком в ()В при увеличении начальной температуры;
()В - устойчивое состояние, почти полное превращение реагентов, но реакция идет с высокой температурой – вне рабочего диапазона.
При 05 - одно устойчивое состояние в ()5, но температура в реакторе вне рабочего диапазона.
Зависимость
статической
характеристики
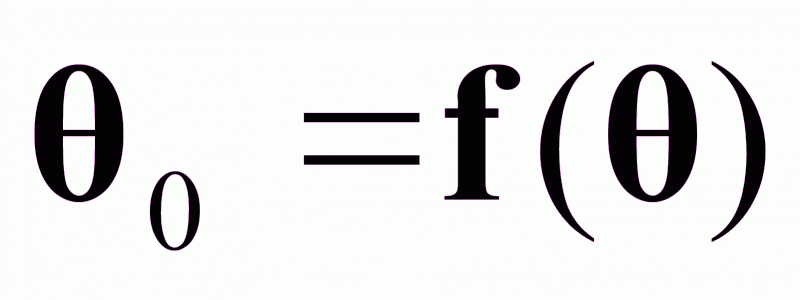
от концентрации С0 исходного реагента.
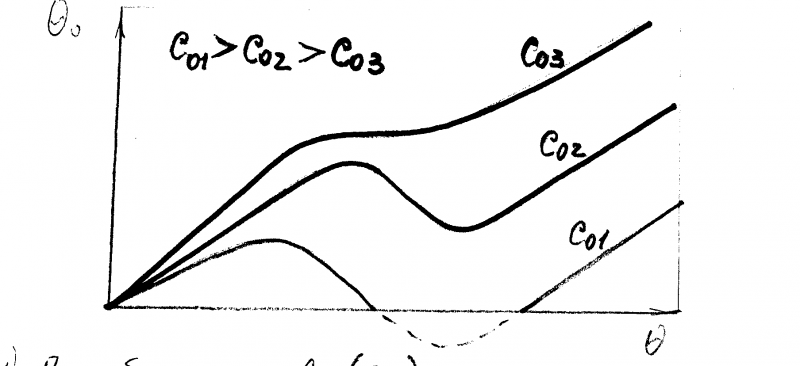
Рис.1.2.
При больших значениях С0 (С01 ) - статическая характеристика неоднозначна даже при низких температурах.
Единственность стационарного состояния возможна только при высоких значениях 0 .
Область отрицательных значений 0 практического смысла не имеет, поэтому показана пунктиром.
Уменьшение входных концентраций (С02 и С03) вызывает смещение неоднозначности статической характеристики в область более высоких температур.
Зависимость
статической
характеристики
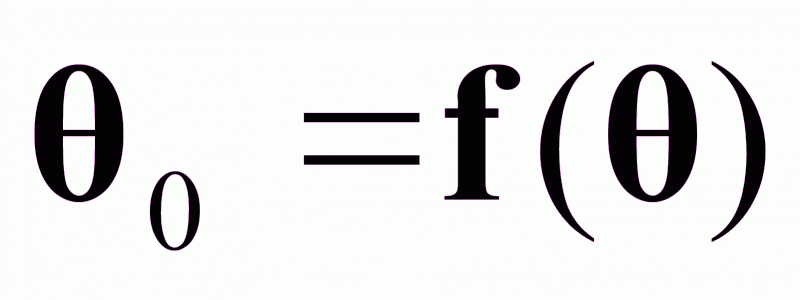 от концентрации
С0 исходного
реагента.
от концентрации
С0 исходного
реагента.

Рис.1.2.
При больших значениях С0 (С01) - статическая характеристика неоднозначна даже при низких температурах.
Единственность стационарного состояния возможна только при высоких значениях 0 .
Область отрицательных значений 0 практического смысла не имеет, поэтому показана пунктиром.
Уменьшение входных концентраций (С02 и С03) вызывает смещение неоднозначности статической характеристики в область более высоких температур.
Определение стационарных состояний
по диаграмме «выделения – отвода тепла».
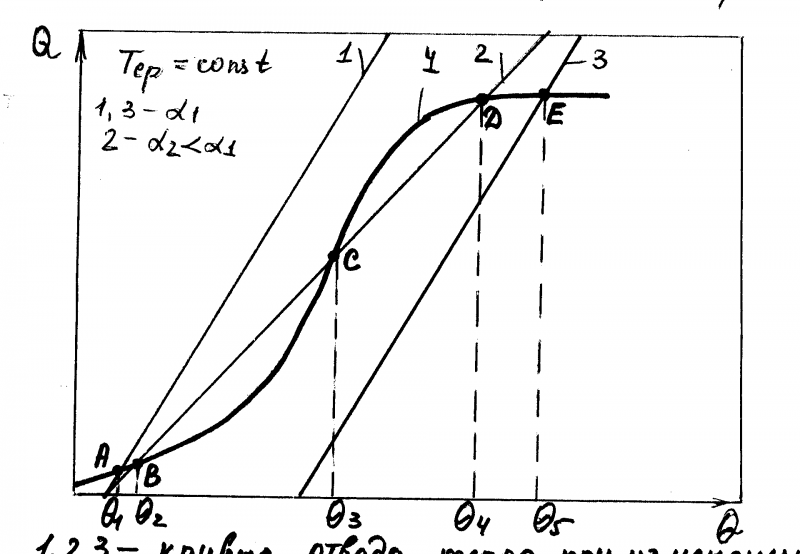
Рис.2.1.
1, 2, 3 - кривые отвода тепла Q при изменении температуры в реакторе c различными значениями коэффициента теплопередачи : 1 = 3 и 2 < 1,3.
4 - кривая выделения тепла
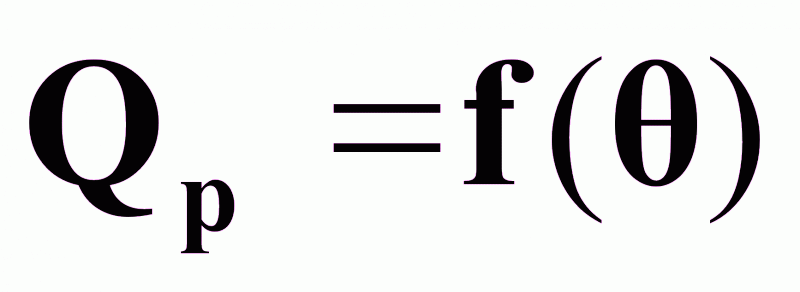 .
.
Система 1-4:
одно стационарное состояние в ()А;
очень низкая температура в реакторе 1 ;
низкая скорость реакции.
Система 3-4:
одно стационарное состояние в ()Е;
практически полное превращение реагента;
очень высокая температура 5 , которая может быть вне рабочей зоны реактора.
Система 2-4:
три стационарных состояния в ()В, С, D;
()В - очень низкая температура в реакторе 2; низкая скорость реакции; стационарное состояние устойчивое;
()D - практически полное превращение реагента; но очень высокая температура 4 , которая может быть вне рабочей зоны реактора; стационарное состояние устойчивое;
()С - температура в рабочей зоне реактора 3; но стационарное состояние - неустойчивое.
Зависимость характеристики выделения тепла
от времени пребывания реакционной массы в реакторе.
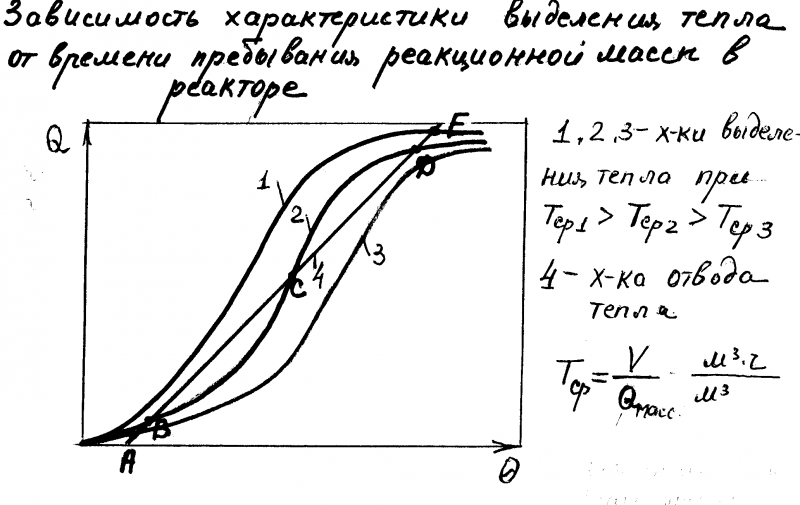
Рис.2.2.
1, 2, 3 - характеристики выделения тепла при Тср1 > Тср2 > Тср3 .
4 - характеристика отвода тепла.
Среднее время пребывания определяется по соотношению:
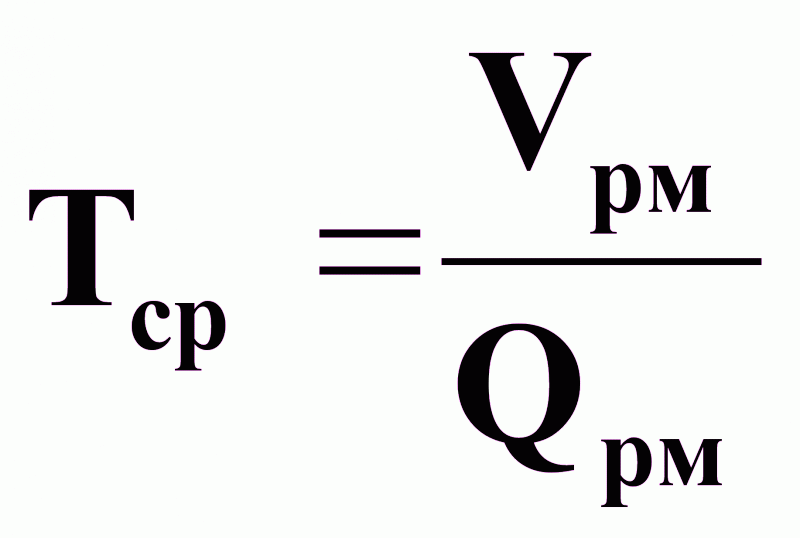 ,
где Vрм
и Qрм
- объем и объемный
расход реакционной
массы.
,
где Vрм
и Qрм
- объем и объемный
расход реакционной
массы.
При увеличении времени пребывания характеристика выделения тепла смещается влево.
Система 1-4:
одно устойчивое стационарное состояние в ()Е;
практически полное превращение реагента;
но очень высокая температура, которая может быть вне рабочей зоны реактора;
Система 3-4.
одно устойчивое стационарное состояние в ()А;
очень низкая температура в реакторе;
низкая скорость реакции.
Система 2-4.
три стационарных состояния в ()В , D и С;
()В - очень низкая температура в реакторе; низкая скорость реакции, стационарное состояние устойчивое;
()D - практически полное превращение реагента; но очень высокая температура, которая может быть вне рабочей зоны реактора; стационарное состояние устойчивое;
()С - температура в рабочей зоне реактора; но стационарное состояние - неустойчивое.
Оценка устойчивости стационарных состояний
по диаграмме «выделения – отвода тепла».
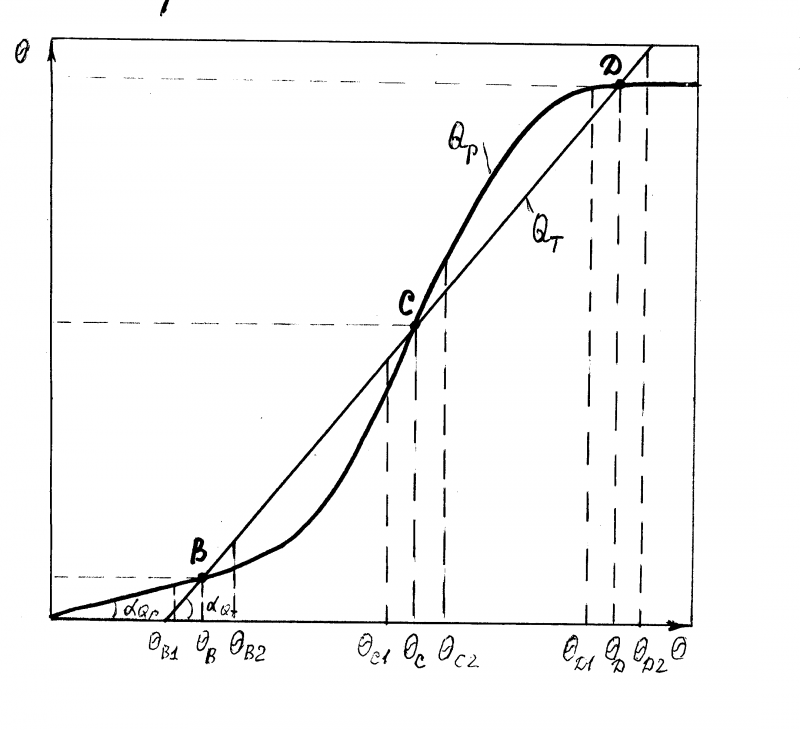
Qр = f() - характеристика выделения тепла реакции;
Qт = f() - характеристика отвода тепла.
Рис.2.3.
Устойчивость реактора в стационарном состоянии В:
при
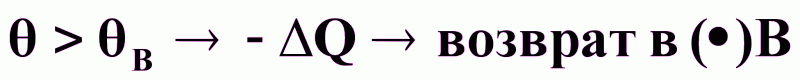 ;
;при
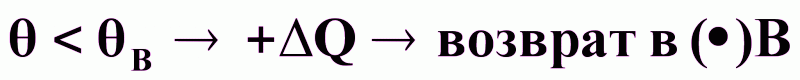 ;
;стационарное состояние в ()В - устойчивое.
Устойчивость реактора в стационарном состоянии D:
при
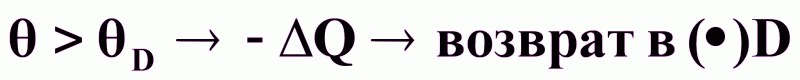 ;
;при
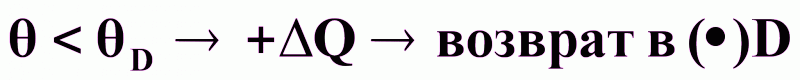 ;
;стационарное состояние в ()D - устойчивое.
Устойчивость реактора в стационарном состоянии C:
при
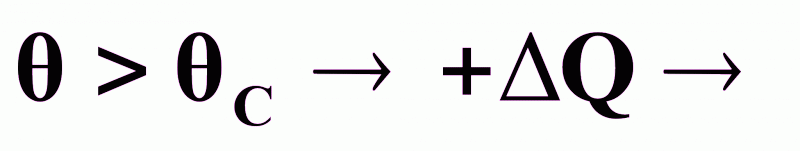 переход
в()D;
переход
в()D;при
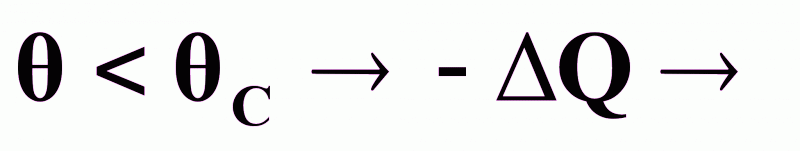 переход
в ()В;
переход
в ()В;
стационарное состояние в ()С - неустойчивое.
9. Материалы к лекции №17
Автоматизация реакторных процессов (ч.3).
Схема для реакции типа А(ж) + В (г) D (г-ц.пр)+С (ж).
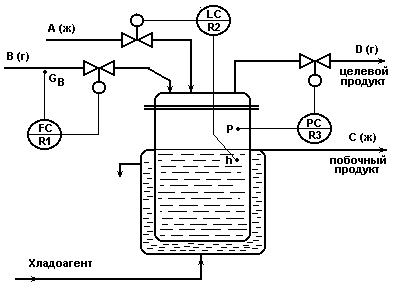
Рис.1.1.
Схема для реакции типа А(ж) + В (г) D (г)+С (ж-ц.пр).
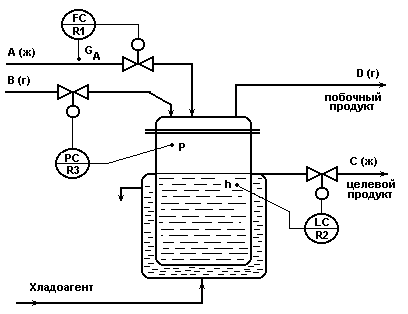
Рис.1.2.
Схема автоматизации для реакции типа
А(ж) + В{Всв(ж) + Врец(ж)} С(ж- ц.пр)+В(ж).
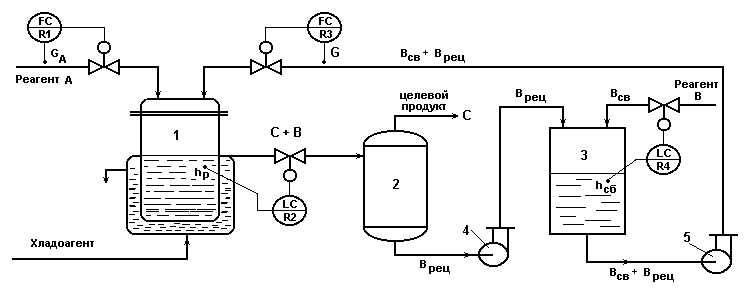
1- реактор; 2 - сепаратор; 3 - сборник; 4, 5 - насосы;
А, В - исходные реагенты; С - целевой продукт; Врц - возвратный (рецикловый) поток реагента В; Всв - свежий поток реагента В.
Рис.1.3.
Система регулирования концентрации
из двух одноконтурных АСР.
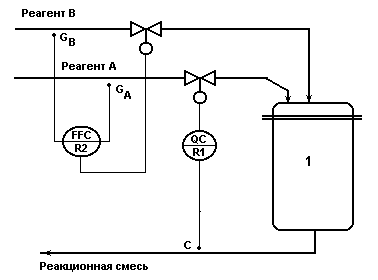
Рис.1.5.
Каскадная АСР концентрации со вспомогательным контуром
стабилизации соотношения расходов исходных реагентов.
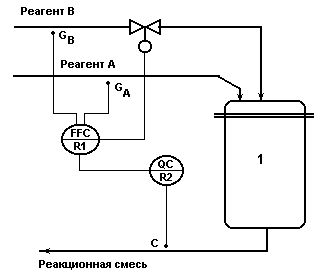
Рис.1.6.
Каскадная АСР концентрации со вспомогательным контуром
стабилизации температуры исходного реагента.
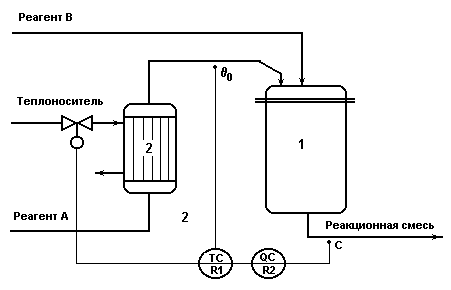
Рис.1.7.
Каскадная АСР концентрации со вспомогательным контуром
стабилизации температуры хладоагента.
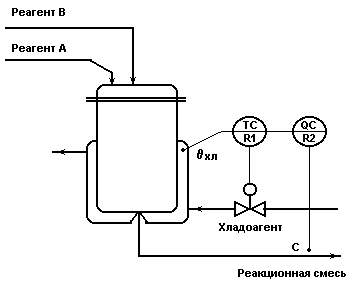
Рис.1.8.
Одноконтурная АСР температуры в реакторе
по подаче исходного реагента.
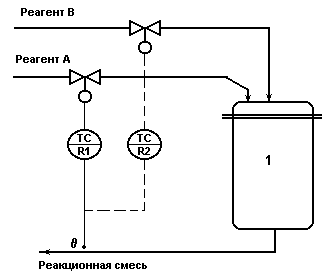
Рис.2.1.
Каскадная АСР температуры в реакторе со вспомогательным контуром
стабилизации температуры исходного реагента.
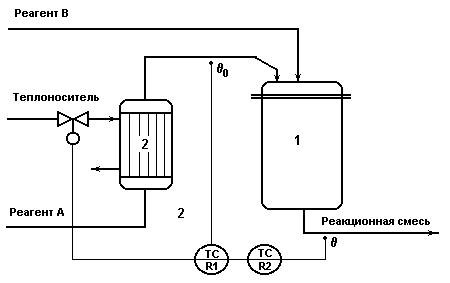
Рис.2.2.
Каскадная АСР температуры в реакторе со вспомогательным контуром
стабилизации температуры хладоагента.
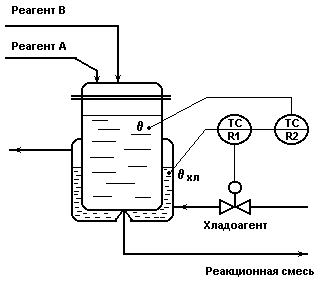
Рис.2.3.
Каскадная АСР температуры в реакторе со вспомогательным контуром
стабилизации давления хладоагента.
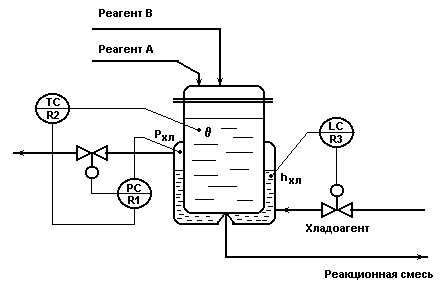
Рис.2.4.
10. Рекомендуемая литература
Основная литература
1. Дудников Е.Г. Автоматическое управление в химической промышленности. - М.: Химия, 1987.- 368 с.
2. Полоцкий Л.М., Лапшенков Г.И. Автоматизация химических производств. - М.: Химия, 1982.- 295 с.
3. Автоматизация технологических процессов легкой промышленности: Учеб пособие для вузов по спец. «Автоматизация технологических процессов и производств» / Под ред. Л.Н. Плужникова. - 2-е изд., перераб. и доп. - М.: Легпромбытиздат, 1984.- 366с.
4. Мамиконов А.Г. Проектирование АСУ.- М.: Высшая школа, 1987.- 303 с.
5. Стефани Е.П. Основы построения АСУ ТП.- М.: Энергоиздат, 1982.- 352с.
6. Пиггот С.Г. Интегрированные АСУ химических производств. - М.: Химия, 1985.- 410 с.
7. Кафаров В.В., Макаров В.В. Гибкие автоматизированные системы в химической промышленности: Учебник для вузов. - М.: Химия, 1990.- 320с.
8. Плютто В.П. Управление химико-технологическими процессами. Процессы массообмена: [Учеб. пособие].- М.: МХТИ, 1984.-48с.
9. Плютто В.П. и др. Автоматизированные системы управления периодическими пролцессами химической технологии. – М.: МХТИ, 1985.-48с.
10. Ицкович Э.Л., Сорокин Л.Р. Оперативное управление непрерывным производством. – М..: Наука, 1989.-155с.
Дополнительная литература
11. Автоматизация технологических процессов легкой промышленности: Учеб пособие для вузов по спец. «Автоматизация технологических процессов и производств» / Под ред. Л.Н. Плужникова. - 2-е изд., перераб. и доп. - М.: Легпромбытиздат, 1993 .
12. Уланов Г.М. и др. Методы разработки интегрированных АСУ промышленными предприятиями. - М.: Энергоатомиздат, 1983.- 320 с.
13. Практикум по автоматике и системам управления производственными процессами: Учеб. пособие для вузов / Под ред. И.М. Масленникова - М.: Химия,1986.- 336 с.
14. Плютто В.П., Путинцев В.А., Глумов В.М. Практикум по теории автоматического управления химико-технологическими процессами: Цифровые системы - М.: Химия,1989.- 168 с.
15. Голубятников В.А., Шувалов В.В. Автоматизация производственных процессов в химической промышленности. - М.: Химия, 1985.-352с.
16. Шувалов В.В. Огаджанов Г.А., Голубятников В.А. Автоматизация производственных процессов в химической промышленности. - М.: Химия, 1991.-480с.
17. Процессы и аппараты химической технологии. Учебник для вузов./ Н.Н. Смирнов, М.И. Курочкина, А.И. Волжинский, В.А. Плессовских. - СПб.: Химия, 1996.-400с.
18. Математическое моделирование основных процессов химических производств. Учеб. пособие для вузов. / В.В. Кафаров, М.Б. Глебов. - М.:Высш.шк., 1991.-399с.
19. Математическое моделирование химико-технологических систем: Учеб. пособие в 3ч./ под ред Л.С. Гордеева. - М.:РХТУ, 1999- 48с.( ч1); 47с.( ч2), 67с.( ч3)
.
СОДЕРЖАНИЕ
1. Материалы к лекции №9 3
2. Материалы к лекции №10 8
3. Материалы к лекции №11 17
4. Материалы к лекции №12 25
5. Материалы к лекции №13 34
6. Материалы к лекции №14 41
7. Материалы к лекции №15 51
8. Материалы к лекции №16 59
9. Материалы к лекции №17 65
10. Рекомендуемая литература 71
29-04-2015, 04:00
