У пацієнтів на ІМ і ЦД 2 типу в дебюті захворювання при виникненні у них гострої лівошлуночкової недостатності ІІ-ІІІ класу за Killip середній рівень МДА і ЦП був достовірно вищий, ніж у хворих на ІМ і ЦД 2 типу без вираженої гострої СН (І клас за Killip) (МДА відповідно 5,48±0,17 нмоль/мл і 4,83±0,08 нмоль/мл (p<0,01), а ЦП – 614,9±19,9 мг/л і 492,3±27,4 мг/л (p<0,001)). Також зазначено, що у жінок прояви оксидативного стресу важчі, порівняно із чоловіками. Зокрема, якщо у жінок середній рівень МДА становив 5,46±0,14 нмоль/мл, то в групі хворих чоловіків – 5,02±0,08 нмоль/мл (р<0,01), рівень ЦП відповідно 619,7±29,1 мг/л і 494,1±20,9 мг/л (р<0,001). Вміст показників оксидативного стресу – МДА та ЦП у крові хворих на ІМ і ЦД 2 типу суттєво підвищувався в залежності від погіршення вуглеводного обміну. Тобто зі наростанням рівня НbА1С вміст МДА збільшується: у крові хворих із концентрацією НbА1С >8% він достовірно вищий (5,40±0,10нмоль/мл), ніж у хворих із НbА1С <8% (4,92±0,10нмоль/мл), р<0,01). Проте, щодо ЦП відмінність у залежності від умісту НbА1С виявилась статистично недостовірною. Проаналізовано рівень показників оксидативного стресу в залежності від вираженості ІР. Виявилось, що у хворих із ЦД 2 типу концентрація АДА у крові значно вища при рівні індекс HOMA більше 2.9 ум.од. При цьому, якщо із ІР середній рівень МДА становить 5,47±0,12 нмоль/мл, то в групі пацієнтів без ІР – 4,93±0,06 нмоль/мл (p<0,01). Аналіз середнього значення ЦП залежно від наявності ІР, загалом не виявив достовірної міжгрупової різниці, хоч його підвищення відзначали у групі хворих із ІР.
Встановлено прямий достовірний зв’язок між МДА та показниками системного запалення: концентрацією СРБ (r=0,23; p<0,05), ФНП-б (r=0,37; p<0,05), ЗФ (r=0,34; p<0,05). Щодо показника системного запалення ІЛ-4, то між ним та МДА зазначили достовірний обернений кореляційний зв’язок (r= –0,24; p<0,05). Проте найвищий рівень взаємозв’язку спостерігався між МДА і Total NO (r=0,78; p<0,01).
У результаті дослідження виявлено достовірний прямий зв’язок між МДА та концентрацією в крові холестеринзв’язаних та тригліцеридзв’язаних показників: із ЗХС (r=0,50; p<0,01), ХС ЛПНГ (r=0,49; p<0,01), КА (r=0,52; p<0,01), ТГ (r=0,39; p<0,01), ХМ (r=0,46; p<0,01), ХС не-(ЛПВГ) (r=0,51; p<0,01), індексом ЗХС/ХС ЛПВГ (r=0,52; p<0,01), індексом ТГ/ХС ЛПВГ (r=0,41; p<0,01), апо-В (r=0,54; p<0,01), відношенням апо-В/апо-А (r=0,47; p<0,01). Крім того, відзначали достовірний зворотний зв’язок між МДА та антиатерогенним показником ліпідного спектру крові – ХС ЛПВГ (r= –0,31; p<0,05).
В обстежених хворих на гострий ІМ із ЦД 2 типу активація системи ПОЛ та пригнічення антиоксидантного захисту відповідає істотному погіршенню вуглеводного обміну та наростанню ІР, про що свідчить позитивна або негативна кореляція між показником вільнорадикального окислення ліпідів – МДА та концентрацією у крові основних показників вуглеводного обміну: глюкозою (r=0,42; p<0,01), НbА1С (r=0,31; p<0,01), інсуліном (r=0,23; p<0,05), індексами HOMA (r=0,29; p<0,05), QUICKI (r= –0,22; p<0,05) та McAuley (r=– 0,23; p<0,05). Важливим для усвідомлення ролі процесів ПОЛ у патогенетичних механізмах пришвидшеного розвитку атеросклерозу у хворих на ЦД 2 типу є встановлення прямої достовірної кореляції між МДА у 1-шу добу госпіталізації та вмістом у крові сечової кислоти (r=0,48, р<0,01). Водночас, на відміну від показників ліпідного, вуглеводного обміну та системного запалення, не виявлено достовірного взаємозв’язку між рівнем МДА та показниками жирового обміну – лептином (r=0,08, р>0,05) та ІМТ (r=0,16, р>0,05). Таким чином, у хворих на ІМ і ЦД 2 типу прояви оксидативного стресу пов’язані із вираженістю порушення метаболізму NO, системного запалення, ліпідного та вуглеводного обміну. Тому в клінічній практиці для покращання прогнозу у пацієнтів на ІМ і ЦД 2 типу слід оцінювати й корегувати весь цей комплекс патологічних змін.
Корекція вуглеводного обміну у хворих на ІМ і ЦД 2 типу із ІР.
На сьогодні немає однозначного підходу до корекції гіперглікемії у хворих із ЦД 2 типу при виникненні гострого ІМ (P. Deedwania et al., 2008),. Переважно у більшості спеціалізованих установ із лікування ІМ хворих із ЦД переводять на дробне три-чотиразове введення невеликих доз інсуліну короткої дії. Такий підхід зумовлений тим, що інсулін при ІМ не тільки знижує рівень глікемії, а й проявляє метаболічну, фібринолітичну, антиоксидантну, протизапальну, вазодилатуючу дію (F. Gao et al., 2002; V.W. Wong et al., 2004; R. Lautamдki et al., 2006). Однак у деякої частини хворих, а саме – при ожирінні, метаболічному синдромі, традиційне призначення інсуліну у відповідності до рівня глікемії не завжди дозволяє ефективно її корегувати через наявність у пацієнтів ІР.
Для вивчення ефективності корекції гіперглікемії та ІР обстежені пацієнти були розподілені на дві групи. Основну (1-шу) групу (19 пацієнтів) склали хворі на ІМ і ЦД 2 типу, яким з 9–10-го дня разом із інсуліном короткої дії (у середньому 34,0±2,2 Од на добу) призначали метформін у початковій дозі 500 мг 2 рази на добу (в обід і ввечір). Надалі поступово впродовж 2–3-х днів підвищували дозу до підтримуючої – 2000 мг на добу у 2 приймання. До контрольної (2-ї) групи увійшли 22 пацієнти з ІМ і ЦД 2 типу, які продовжували отримувати монотерапію інсуліном. Оцінка показників вуглеводного обміну та ІР, ліпідного спектру крові, маркерів системного запалення, метаболізму NO, лептину, оксидативного стресу, антропометричних вимірів (ІМТ, ІАО), функціонального стану печінки достовірної різниці між групами не зазначила.
Вивчення впливу різних схем фармакотерапії на показники гіперглікемії та ІР у пацієнтів на ІМ і ЦД 2 типу засвідчило істотні переваги комбінованої терапії. У групі пацієнтів, яким призначали інсулін у поєднанні з метформіном (1-а група), через три тижні від початку лікування спостерігалось достовірне зниження концентрації глюкози в крові – на 17,0% (p<0,05), а у 2-й групі – на 12,6% (p<0,05), інсуліну – на 45,7% (p<0,05) і 43,3% (p>0,05), індексу HOMA – на 61,2% (p<0,05) і 39,1% (p<0,05), індексу Bennetta – на 34,0%(p<0,05) і 8,5% (p>0,05). Інший показник ІР – індекс McAuley у 1-й групі достовірно покращився на 30,3% (p<0,05), у 2-й групі – на 9,7% (p>0,05), вміст С-пептиду – на 42,9% (р<0,05) і 29,0% (р<0,05). Отже, кількісне значення індексів HOMA McAuley вказувало на збереження проявів ІР у пацієнтів 2-ї групи на кінець стаціонарного етапу лікування. Рівень С-пептиду в цій групі хворих зріс теж несуттєво і перед випискою зі стаціонару залишався у двічі нижчим від контролю.
Отримані у даному дослідженні результати показали, що в кінці стаціонарного етапу лікування на фоні комбінованої фармакотерапії відбулось достовірне покращення процесів, пов’язаних із ПОЛ. Зокрема, рівень МДА у пацієнтів 1-ї групи достовірно знизився на 9,2% (з 5,53±0,20 ммоль/л до 5,02±0,12 ммоль/л, р<0,05), тоді як у хворих 2-ї групи змінювався недостовірно.
На фоні комбінованої терапії інсуліном і метформіном, на відміну від монотерапії інсуліном, у хворих на ІМ і ЦД 2 типу із ІР істотно знижувався рівень показників обміну тригліцеридів. Показники обміну тригліцеридів до і після лікування інсуліном у комплексі з метформіном (1-а група) змінювались наступним чином: концентрація ТГ знизилась на 21,4% (р<0,05); ХС ЛПДНГ, які містять значну кількість ТГ, – на 20,6% (p<0,05); ХМ – на 20,0% (p<0,05); індекс ТГ/ХС ЛПВГ – на 22,5% (p<0,05). У пацієнтів 2-ї групи, які протягом 3-х тижнів отримували монотерапію інсуліном, зазначалась тенденція лише до поліпшення тригліцеридного ліпідного обміну: середній рівень ТГ знизився на 10,3 %, ХС ЛПДНГ – на 10,3 %,ХМ – на 13,0 %, індекс ТГ/ ХС ЛПВГ – на 13,0 %.
Призначення метформіну не викликало погіршення функції печінки. Навпаки, рівень г-ГТП, що є найбільш чутливим її показником, у хворих 1-ї групи, які додатково вживали метформін, в середньому знизився вдвічі (з 68,75±16,29 од/л до 35,73±3,7 од/л, р<0,05). Лише в одного пацієнта (5,3%) у кінці дослідження відмічалось збільшення г-ГТП з 18,1 од/л до 32,4 од/л, що суттєво не відрізнялось від контрольного значення (28,35±5,11 од/л).
Поєднання інсуліну з метформіном у більшості хворих переноситься задовільно. На початку лікування лише у трьох хворих виникли побічні реакції з боку травного тракту: нудота, дискомфорт у ділянці шлунку, діарея. Через кілька днів без корекції доз ЛЗ всі ці явища зникли. Позитивним ефектом запропонованої комбінованої терапії є зменшення дози інсуліну вдвічі та покращання клінічного перебігу у хворих 1-ї групи.
Вивчення впливу поєднаної терапії інсуліном із метформіном на вуглеводний, жировий, ліпідний обмін та системне запалення, метаболізм NO, оксидативний стрес дало можливість розробити диференційований підхід до призначення цих ЛЗ. Комбіновану терапію інсуліном із метформіном перш за все слід призначати хворим на ІМ і ЦД 2 типу при виявленні у них вираженої ІР. Інформативними маркерами ІР і ступеня її вираженості є розрахункові індекси HOMA (більше 2,9 ум. од.), McAuley (нижче 6 ум. од.), QUICKI (нижче 0,33 ум. од), рівень імунореактивного інсуліну (більше 10-12 мкОД/мл), індекс ІАО (відношення об’єму талії до об’єму стегон – ОТ/ОС більше 1,0), ІМТ більше 30 кг/м2 , а також високий вміст ТГ у крові (вище 2-2,3 ммоль/л) (схема 1).
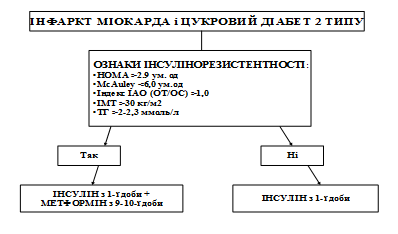
Схема 1. Алгоритм ведення хворих на ІМ і ЦД 2 типу із ІР.
При призначенні метформіну слід врахувати прямі протипоказання до його застосування. Через загрозу виникнення молочнокислого ацидозу метформін з 1-ї доби гострого ІМ не використовувався. В середньому на 9-10-й день виникнення ІМ стан хворих стає стабільним і небезпека розвитку молочнокислого ацидозу зникає. Саме із цього часу є всі підстави додавати до інсуліну ЛЗ із групи бігуанідів – метформін із метою корекції не лише гіперглікемії, але й ІР.
Корекція порушень обміну тригліцеридів у хворих на ІМ і ЦД 2 типу. Одним із завдань дослідження було шляхом поєднаного застосування із симвастатином препаратів щ3 -ПНЖКу хворих на ІМ і ЦД 2 типу з помірно порушеною функцією печінки (г-ГТП – 69,78±7,56 од/л), досягти бажаного гіполіпідемічного ефекту у зниженні показників обміну ТГ при використанні нижчих доз симвастатину, запобігти погіршенню її функції. Методом випадкової виборки сформовані дві групи хворих. Основна (1-а група) складалась із 21 особи, які отримували комбіновану фармакотерапію препаратами щ3 -ПНЖК (1500 мг на добу) та симвастатином (у середньому 15,2±2,1 мг на добу). Група порівняння (2-а група) – із 22 особи, які приймали лише симвастатин (у середньому 15,6±2,2 мг на добу).
Через три місяці лікування у пацієнтів 1-ї групи спостерігалось достовірне зниження рівня ТГ, порівняно з 2-ю групою. Вкінці терміну фармакотерапії практично однаковий у двох групах початковий рівень ХС ЛПДНГ знизився у 1-й групі на 21,0%, а в 2-й групі – на 12,5% (р<0,05); ТГ – на 25,5% і 14,2% (р<0,05); індекс ТГ/ХС ЛПВГ – 31,8 % і 19,6 % (р<0,05); ХС не-(ЛПВГ) – на 32,3 % і 19,1% (р<0,05); ХМ – на 29,7 % і 16,6 % (р<0,05). Рівень ХС ЛПНГ знизився достовірно у 1-й групі на 24,6 %, у 2-й спостерігалась лише чітка тенденція до його зниження (на 13,7%). Загалом за цим показником через три місяці фармакотерапії не встановлено статистично достовірної міжгрупової відмінності. Ймовірно ліпідознижуюча терапія у пацієнтів з ІМ і ЦД 2 типу повинна бути більш тривалою. Нормальні рівні показників тригліцеридного ліпідного обміну були досягнуті у третини хворих, які приймали симвастатин (2-а група), та в половини пацієнтів, які отримували комбіновану гіполіпідемічну терапію (1-а група). У решти хворих обох груп показники ліпідного спектру крові мали чітку тенденцію до покращення.
У результаті трьохмісячного курсу фармакотерапії симвастатином у поєднанні з щ3 -ПНЖК у хворих після перенесеного ІМ з помірним порушенням функції печінки (1-а група) відбулось достовірне зниження вмісту г-ГТП у крові з 69,46±10,24 од/л до 36,27±4,09 од/л, р<0,05. У хворих 2-ї групи, які впродовж трьох місяців отримували симвастатин, показник функціонального стану печінки – г-ГТП в середньому зменшився незначно, лише на 9% (з 70,64±10,16 од/л до 64,27±4,09 од/л), і практично не відрізнявся від початкового рівня.
У групі хворих, які крім симвастатину одержували препарати щ3 -ПНЖК значно покращились результати тримісячної реабілітації у порівнянні з монотерапією статином, істотніше покращилось загальне самопочуття та толерантність до навантаження.
Для з’ясування предикторів підвищеного ризику виникнення ускладнень на стаціонарному етапі лікування хворих на гострий ІМ із супутнім ЦД 2 типу проведено аналіз бази даних у вибірці із 223 пацієнтів. Монофакторний аналіз якісних, рангових і параметричних характеристик дав можливість виділити низку предикторів, які достовірно (р<0,05) пов’язані із погіршенням прогнозу і розвитком ускладненого перебігу ІМ. Визначали міру інформативності Кульбака – показник, який дає змогу кількісно оцінити інформативність кожного критерію. Для кількісних характеристик було визначено порогові точки, при поділі за якими інформативність була найвища. Для виявлених предикторів виникнення ускладнень ІМ було також визначено відносний ризик (ВР – RR).
На основі проведеного однофакторного аналізу (рис. 3) з використанням міри інформативності Кульбака і показника ВР виникнення подій встановлено, що у хворих на ІМ і ЦД 2 типу важливим прогностичним фактором виникнення ускладнення, були: індекси ІР – MсAuley (<7 ум.од) і HOMA (≥3 ум.од), рівень ЦП у крові (≥500 мг/л), креатинін (>0,14 ммоль/л), сечовина (≥8 ммоль/л), дилатація лівого передсердя (>4 см), ФВ (<45%). Дещо менший, але також статистично достовірний вплив на прогноз мали вік (>55 років), важкість АГ (2-3 ступінь), тривалість АГ (>6 років), рівень інсуліну (>9 мклОД/мл ), а-, дискінезія ЛШ, приналежність до жіночої статі.
ВР(95% ДІ)
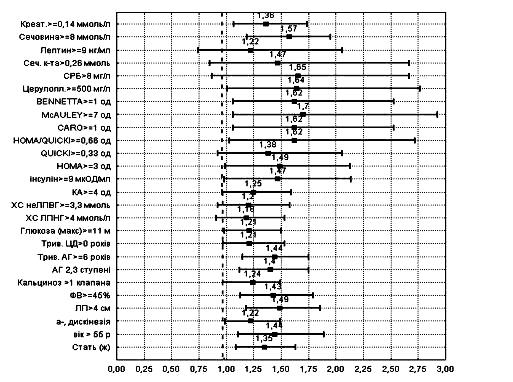
краще гірше
Рис. 3. Відносний ризик виникнення ускладнень ІМ, поєднаного із ЦД 2 типу.
Характеристики, які при монофакторному аналізі засвідчили статистично значущий зв’язок із виникненням ускладнень ІМ у хворих на ЦД 2 типу, було включено у багатофакторний покроковий дискримінантний аналіз. У результаті створено модель, яка включала 5 незалежних значущих предикторів щодо передбачення ускладненого перебігу ІМ . До цих факторів належали: рівень креатиніну (порогове значення >0,14 ммоль/л), вміст ЦП (>500 мг/л), індекс MсAuley (<7,0 ум.од), ФВ (<45%), вік більше 55 років. Чутливість цієї моделі сягає 83,3%, специфічність – 85,7%, загальна точність – 84,4%. Важливо, що 4 із 5-ти наведених предикторів можна цілеспрямовано корегувати і, тим самим, профілактично попереджувати виникнення ускладнень ІМ.
Результати проведеного однофакторного аналізу і показника ВР виникнення подій (рис. 4) засвідчили, що найбільш значущими прогностичними факторами розвитку застійної СН у хворих на ІМ із супутнім ЦД 2 типу є: креатинін(>0,13 ммоль/л); СРБ (>8 мг/л); г-ГТП (>50 од/л); ФВ (<40%); максимальний рівень глюкози (>15,0 ммоль/л); ФНП-б (>60 пг/мл); вік понад 55 років. Крім того, дещо менший, але також достовірний вплив на прогноз мають НвА1С , тривалість ЦД, Total NO, дискінезія ЛШ та приналежність до жіночої статі.
ВР(95% ДІ)
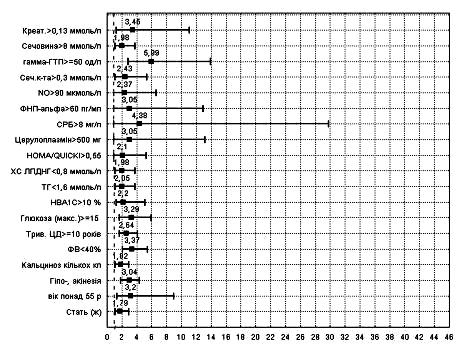
Рис. 4. Відносний ризик виникнення застійної СН у хворих на ІМ і ЦД 2 типу.
Проведений багатофакторний аналіз дозволив створити модель розвитку застійної СН , що включає 5 предикторів (вік понад 55 років, максимальний рівень глюкози понад 15 ммоль/л, тривалість ЦД понад 10 років, ФВ менша 40% та рівень креатиніну понад 0,13 ммоль/л) із передбачуваною точністю моделі 90,2%.
Предиктори розвитку постінфарктної стенокардії були іншими, ніж у загальній моделі прогнозування ускладнень ІМ та у моделі прогнозування застійної СН. Міра інформативності Кульбака прогностичних предикторів для постінфарктної стенокардії, подібно до моделі прогнозування застійної СН, була значно вищою від загальної моделі прогнозу ускладнень.
Найвагомішим предиктором виникнення ранньої постінфарктної стенокардії виявилась ІР, а саме показники, що її характеризують: індекс HOMA більше 4 ум.од (міра інформативності (МІ) Кульбака 2,5, р<0,001); індекс McAuley нижче 6 ум. од (МІ 2,06, р<0,05); рівень інсуліну у крові більше 10 мкОД/мл (МІ 1,32, р<0,0001). У модель також були вибрані наступні критерії: наявність АГ (МІ 0,42, p<0,05) та її тривалість більше 5 років (МІ 0,58, р<0,01), основні показники оксидативного стресу – МДА більше 5 нмоль/мл (МІ 1,68, р<0,0001), ЦП вище 500 мг/л (МІ 1,41, p<0,05) та холестеринвмісні показники – (ХС не-(ЛПВГ) більше 6 ммоль/л (МІ 1,33, р<0,001), ХС ЛПНГ більше 3 ммоль/л (МІ 0,57, р<0,01), ЗХС більше 5 ммоль/л (МІ 0,57, р<0,05)).
На основі проведеного нами одновимірного аналізу з використанням міри інформативності Кульбака
8-09-2015, 22:13
